Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формул сполуки за відомими степенями окиснення
Тема: Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формул сполуки за відомими степенями окиснення.
Мета:
Освітня: дати пояснення про валентність та ступінь окиснення. Закріпити та вдосконалити вміння визначати валентність та ступінь окиснення елементів у сполуках та складати структурні формули.
Розвиваюча: розвивати навички складання хімічних формул за допомогою ступеня окиснення. Розвивати пізнавальний інтерес до навчальної дисципліни, вміння застосовувати свої знання на практиці.
Виховна: виховувати увагу, акуратність, розширювати кругозір учнів.
Основні поняття та терміни: валентність, ступінь окиснення, позитивні значення ступенів окиснення, негативні значення ступенів окиснення.
Обладнання: періодична система хімічних елементів Д.І.Менделєєва, мультимедійна дошка.
Тип уроку: комбінований.
Хід уроку:
І. Організаційний момент (привітання 2 хв., відмічання присутніх)
Доброго дня , діти! Сьогодні на уроці ми будемо працювати разом. Який у вас настрій на початку уроку? На ваших партах лежать смайлики: веселий, сумний та байдужий. Виберіть той який відповідає вашому настрою на початку уроку.
Девіз уроку: (слайд 1)
Зібратися разом – це початок,
Триматися разом – це прогрес,
Працювати разом – це успіх. Г.Форд
Тож давайте побажаємо один одному успіхів на сьогоднішньому уроці.
ІІ. Повторення вивченого матеріалу (7-10 хв)
Пригадаємо, що ми вчили на минулих уроках.
Самостійна робота на листках(тест) і деяким учням робота на картках
Опитування:
1) Які типи зв'язків ви знаєте?
2) Який зв’язок називають ковалентним?
3) Який зв’язок називають ковалентним полярним?
4) Який зв’язок називають ковалентним неполярним?
5) Який зв’язок називають йонним?
6) Що таке електронегативність?
ІІІ. Повідомлення теми і мети уроку (3 хв)
Сьогодні в нас буде цікаве завдання.
До свята (наприклад свята Миколая) ми будемо робити подарунки. У кожного з вас є подарункові пакети та цукерки. Ваше завдання: зробити якнайбільшу кількість подарунків. Але, є дві умови:
- В подарунку має бути тільки дві цукерки
- Ви не можете нікому віддавати пусті подарункові пакети .
Які ваші дії? Чому ви об’єдналися саме в такі групи для виконання завдання? Якщо уявити, що ви- атоми, подарункові пакети- квантові комірки, а цукерки- електрони зовнішнього електронного шару…
Як ви вважаєте яка характеристика атома є важливою при складанні хімічних формул і при утворенні зв’язків у молекулах речовин? (валентність)
Як ви вважаєте, що означає цей запис?(на слайді)
III II +3 -2
Al2O3 Al2O3
Тож ми сьогодні на уроці з’ясуємо, що означають ці записи і навчимося їх використовувати.
Тема нашого уроку - Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формул сполуки за відомими степенями окиснення.
Що ми повинні розглянути на уроці:
- Поняття валентність і ступінь окиснення
- Правила для визначення ступеня окиснення
- Чим відрізняється валентність від ступені окиснення
- Визначення валентності і ступеня окиснення в речовинах
- Написання формули речовини за вказаними ступенями окиснення
IV. Вивчення нового матеріалу
Валентність – це властивість атома елемент утворювати хімічні зв’язки.
Під числом хімічних зв’язків розуміють число спільних електронних пар. Спільні електронні пари утворюються тільки у випадку ковалентного зв’язку, тому валентність атомів можна визначити тільки в ковалентних сполуках.
Валентність немає знакуі неможе бути 0.
Валенність О=2, Н=1, луж. Ме=1
Визначити валентність в сполуках( завдання на слайді)
ІІІ ІІ ІІ ІІ VI II IV II IV II III II VIII II III I IV I I II
Cr2O3 CuO SO3 NO2 MnO2 Mn2O3 XeO4 NH3 СH4 K2O
Під числом хімічних зв’язків розуміють число спільних електронних пар. Спільні електронні пари утворюються тільки у випадку ковалентного зв’язку, тому валентність атомів можна визначити тільки в ковалентних сполуках.
Ступінь окиснення – це умовний заряд, якого набув би атом, якби всі зв’язки в данній сполуці були йонні.
Карбон частково губить контроль над 4 електронами, тому його ступінь окиснення дорівнює +4
Кожен атом Оксигену набуває додаткового контролю над двома електронами, тому його ступінь окиснення дорівнює -2
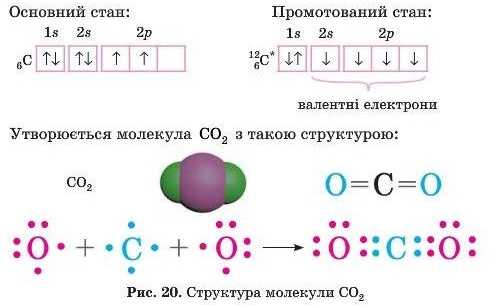
Ступінь окиснення як ви бачете складається з двох частин. Яких?
- Зі знаку:
- Якщо «+» атом віддав електрони
- Якщо «- « атом приєднав електрони
- З числа – воно вказує число електронів, зміщених від атома одного елемента до атома іншого елемента.
+1 -2 0 +5 -2 0 0 0 +3 -2
Na2O H2 P2O5 O2 Cl2 N2 Fe2O3
- C.О. елементів у простих речовинах дорівнює нулю (Cl2, H2, Zn, Fe)
+1 -1 +1 -2 +1 -2 -3+1 -4 +1
HCl H2S H2O NH3 CH4
- C.O. Гідрогену в більшості сполук +1, і лише в сполуках з металами він дорівнює –1. (Na+1H-1, Ca+2H2-1)
+1 -2 +2 -2 +3 -2 +5 -2 +4 -2
Na2O CaO Fe2O3 P2O5 SiO2
- C.O. Оксигену в більшості сполук –2, і лише в деяких сполуках йому приписують ступінь окиснення –1 (Na2O2,H2O2 або +2 (OF2).
+1-1 +1-1 +2 -1 +1-1 +1 -1 +1-1
HF KF CaF2 HCl NaBr AgJ
- C.O. галогенів у сполуках (-1)
+1 -2 +1-1 +1-1 +1 -2 +1 -1 +1 -2
K2O KCl NaH Na2O RbBr Cs2S
- C.O. лужних металів +1
+1 -2
Na2O 2·(+1)+1·(-2)=0
- Cума всіх ступенів окиснення в сполуці дорівнює 0
- С.О. атома металу побічної підгрупи в сполуках позитивний і чисельно дорівнює його валентності.
- Вищий додатній С.О. дорівнює номеру групи і буває коли в утворенні зв’язків беруть участь усі валентні електрони атома.
- Нижчий від’ємний С.О. буває у неметалів і дорівнює (№групи-8) 4-8=-4
V. Закріплення знань учнів (завдання на слайдах)
- Правда чи неправда (3хв. – підняття руки)
Сs+1Br-1 – правда тому, що Cs+1 – бо він стоїть в першій групі, а Br-1 – бо він галоген.
Аl-3Cl3+1 – неправда тому, що Al це метал і в нього с.о. +3, і Cl-1 – бо він галоген.
H2+1S-2 –правда тому, що Н завжди +1.
К+1Н-1 – правда тому, що К+1 він лужний метал
N2+2O3-3 – неправда тому , що О-2
N+2O-2 – правда
S+4O2-2 – правда
S0 – правда тому, що проста речовина
Ca+2 – неправда тому, що у простої речовини с.о. 0
Na2-1O+2 – неправда тому, що Na+1 бо він лужний метал, а у О завжди -2
- Визначення невідомого С.О.
SxO3-2 x=+6 Mg+2Sx x=-2 AgxH-1 x=+1
N2xO3-2 x=+3 PxH3+1 x=-3 AlxF3-1 x=+3
- Визначити валентность , ступінь окиснення і складіть структурну формулу сполук.
І ІІ +1 -2 ІІІ І -3 +1
H2O H2O H – O – H NH3 NH3 H – N – H
H
III 0 IV I -4+1 H
N2 N2 N=N CH4 CH4 H – C – H
VI II +6-2 IV II +4 -2
SO3 SO3 O = S = O SO2 SO2 O = S = O
О
I VI II +1+6-2 V II +5 -2
H2SO4 H2SO4 H – O O P2O5 P2O5 O O
S P – O – P
H – O O O O
I V II +1+5-2 I V II +1+5-2
H3PO4 H3PO4 H – O – P =O HNO3 HNO3 H – O – N =O
H – O – O
VI. Узагальнення
Підведемо підсумок уроку. Згадаємо наші питання на початку уроку, чи можемо ми дати на них відповідь?
VII. Рефлексія (3хв.) на листочках
- Я розумію, що таке валентність.
- Я вмію визначати валентність.
- Я розумію, що таке ступінь окиснення.
- Я розумію як визначати ступені окиснення.
- Я запам’ятав правила ступенів окиснення.
- Я зрозумів чим відрізняється валентність від ступенів окиснення.
- Я міг би розв’язати задачі на визначення ступеня окисненя.
VIII. Домашнє завдання
Опрацювати § 21, завдання № 67 с. 119, скласти формули сполук Гідрогену з Кальцієм, Нітрогеном, Силіцієм, Карбоном, проект «Залежність фізичних властивостей речовин від типів кристалічних ґраток»
Гімназія №9
Кіровоградської міської ради
Кіровоградської області
План – конспект уроку з хімії у 9 – А класі з теми:
«Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формул сполуки за відомими степенями окиснення.»
Підготувала
Вчитель хімії і біології
Гаянська Юлія Петрівна
ПРАВИЛА ВИЗНАЧЕННЯ СТУПЕНЯ ОКИСНЕННЯ.
- C.О. елементів у простих речовинах дорівнює нулю (Cl2, H2, Zn, Fe)
- C.O. Гідрогену в більшості сполук +1, і лише в сполуках з металами він дорівнює –1. (Na+1H-1, Ca+2H2-1)
-
C.O. Оксигену в більшості сполук –2, і лише в деяких сполуках йому приписують ступінь окиснення –1 (
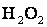 ,
, 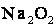 або +2 (
або +2 (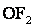 ).
).
- C.O. галогенів у сполуках (-1)
- C.O. лужних металів +1
- Cума всіх ступенів окиснення в сполуці дорівнює 0
- С.О. атома металу побічної підгрупи в сполуках позитивний і чисельно дорівнює його валентності.
- Вищий додатній С.О. дорівнює номеру групи і буває коли в утворенні зв’язків беруть участь усі валентні електрони атома.
- Нижчий від’ємний С.О. буває у неметалів і дорівнює (№групи-8) 4-8=-4

про публікацію авторської розробки
Додати розробку
