Презентація до уроку з теми "Види спектрів. Спектральний аналіз"
Презентація до уроку виконана з використанням матеріалів сайту https://www.fizikanova.com.ua/



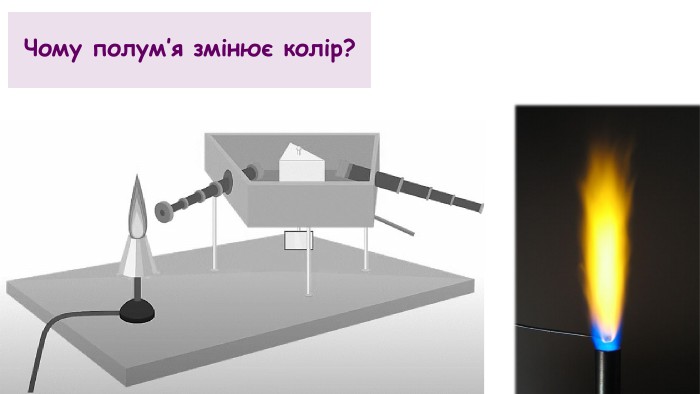
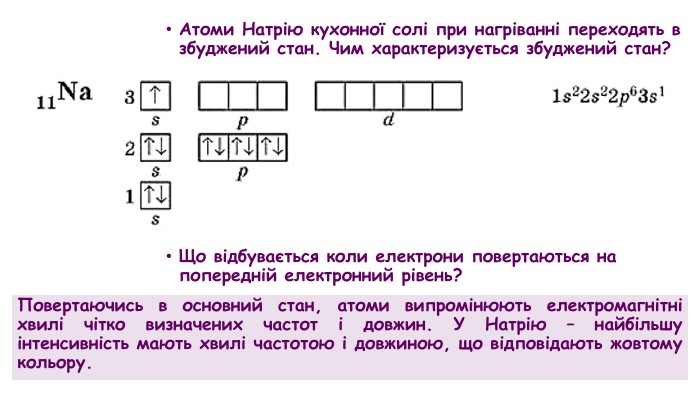










Атоми Натрію кухонної солі при нагріванні переходять в збуджений стан. Чим характеризується збуджений стан?Що відбувається коли електрони повертаються на попередній електронний рівень?Повертаючись в основний стан, атоми випромінюють електромагнітні хвилі чітко визначених частот і довжин. У Натрію – найбільшу інтенсивність мають хвилі частотою і довжиною, що відповідають жовтому кольору.
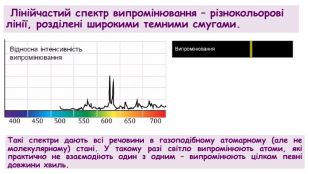
Такі спектри дають всі речовини в газоподібному атомарному (але не молекулярному) стані. У такому разі світло випромінюють атоми, які практично не взаємодіють один з одним – випромінюють цілком певні довжини хвиль. Лінійчастий спектр випромінювання – різнокольорові лінії, розділені широкими темними смугами.
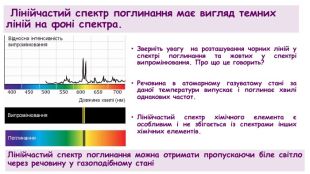
Лінійчастий спектр поглинання можна отримати пропускаючи біле світло через речовину у газоподібному стані Лінійчастий спектр поглинання має вигляд темних ліній на фоні спектра. Зверніть увагу на розташування чорних ліній у спектрі поглинання та жовтих у спектрі випромінювання. Про що це говорить?Речовина в атомарному газуватому стані за даної температури випускає і поглинає хвилі однакових частот. Лінійчастий спектр хімічного елемента є особливим і не збігається із спектрами інших хімічних елементів.
Лінійчастий спектр поглинання можна отримати пропускаючи біле світло через речовину у газоподібному стані Лінійчастий спектр поглинання має вигляд темних ліній на фоні спектра. Зверніть увагу на розташування чорних ліній у спектрі поглинання та жовтих у спектрі випромінювання. Про що це говорить?Речовина в атомарному газуватому стані за даної температури випускає і поглинає хвилі однакових частот. Лінійчастий спектр хімічного елемента є особливим і не збігається із спектрами інших хімічних елементів.
Смугасті спектри утворюються молекулами, що слабо зв’язані або не зв’язані між собою. Для спостереження молекулярного спектра, так само як і для лінійчастих спектрів, використовують світіння пари в полум’ї або світіння газового розряду. Смугасті спектри складаються з окремих смуг, розділеними темними проміжками. За допомогою досконалого спектрального апарата можна виявити, що кожна смуга – це сукупність багатьох щільно розміщених ліній.
Непервніі спектри утворюються стисненими газами, рідинами, твердими тілами, нагрітими до високої температури, високотемпературною плазмою. Неперервний спектр випромінювання містить всі довжини хвиль - від червоного до фіолетового. У спектрі немає розривів. На екрані спектрального апарата можна побачити суцільну різнокольорову смугу.
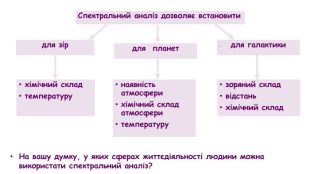
Спектральний аналіз — сукупність методів визначення хімічного складу речовини, заснований на вивченні спектрів. Метод запропоновано Кірхгофом та Бунзеном у 1859 роціДля одержання спектрів застосовують спектроскоп та спектрограф. У спектроскопі його розглядають, а за допомогою спектрографа - фотографують. Спектрограма — фотографія спектра. Переваги спектрального аналізу: висока чутливість, простота та швидкість аналізу.
Якщо сфотографувати спектр сонячного світла, то на знімку будуть спостерігатись чіткі лінії поглинання: Уперше ці лінії описав Йозеф Фраунгофер. Тому вони отримали назву - лінії Фраунгофера. Поява цих ліній пов’язана з проходженням сонячного проміння через атмосферу Сонця та Землі. За цими лініями було встановлено, що на Сонці є усі хімічні елементи, присутні на Землі, а також відкрито Гелій. На Землі його виявили лише через 26 років.
-
 Варшкевич Олена 25.02.2024 в 22:55Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Варшкевич Олена 25.02.2024 в 22:55Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку