Методичний посібник з хімії у 11 класі - "Природні джерела вуглеводнів"
Посібник містить методичні матеріали: плани-конспекти уроків з хімії до теми "Природні джерела вуглеводнів", у тому числі бесіди, презентацію. Матеріали посібника можуть бути використані для підготовки до уроків.


 Автор: Кикоть В.П. – викладач хімії ДНЗ «Черкаський професійний автодорожній ліцей», кваліфікаційна категорія «спеціаліст вищої категорії», педагогічне звання « викладач - методист»
Автор: Кикоть В.П. – викладач хімії ДНЗ «Черкаський професійний автодорожній ліцей», кваліфікаційна категорія «спеціаліст вищої категорії», педагогічне звання « викладач - методист»
Рецензенти: Скрипник В.С. – заступник директора з НР ДНЗ “Черкаський професійний автодорожній ліцей”
Посібник містить методичні матеріали: плани-конспекти уроків, презентації, відеоматеріали до проведення уроків хімії з теми «Природні джерела вуглеводнів».
Пропонується працівникам ПТНЗ: викладачам хімії з метою впровадження в навчально – виховний процес передового педагогічного досвіду.
Схвалено: на засіданні методичної комісії природничо-математичного циклу (протокол № 5 ///// від //// 2016 р.)
Підготовлено до друку навчальною частиною ДНЗ «Черкаський професійний автодорожній ліцей”
Черкаси, вул. Онопрієнка, 4
ПЕРЕДМОВА
Посібник містить методичні матеріали: плани-конспекти уроків, презентаційні матеріали з хімії з теми “Природні джерела вуглеводнів”. Матеріали можуть бути використані для підготовки до проведення уроків з хімії для учнів ІІ курсу ПТНЗ.
Даний посібник відповідає розділам програми Міністерства освіти і науки України з хімії для стандартного та академічного рівнів.
Наведені в посібнику матеріали будуть корисними в процесі підготовки спеціалістів з професій автомобільного транспорту.






 План – конспект уроку № 1
План – конспект уроку № 1
Тема програми: Природні джерела вуглеводнів
Тема уроку: Природні джерела органічних речовин
Мета уроку: формувати в учнів знання про природні джерела органічних речовин; розширити знання про органічні сполуки на прикладі вуглеводневої сировини; географічне місцезнаходження головних природних джерел вуглеводнів; показати використання їх як палива та важливого джерела синтезу органічних сполук; ознайомити зі складом, фізичними властивостями, головними способами переробки й використання природного й супутнього нафтових газів;
Тип уроку: формування нових знань
Методи та методичні прийоми: бесіда, розповідь, робота з інтерактивною дошкою, демонстрація слайдів, робота з опорними конспектами, лабораторний експеримент, самостійна робота з колекціями, демонстрація відеоматеріалів.
КМЗ уроку: презентація “Природні джерела вуглеводнів”, зразки органічних речовин: нафта, торф, буре вугілля, природний газ, кам’яне вугілля, відеоматеріали.
ХІД УРОКУ
І. Організаційний момент.
ІІ. Актуалізація навчальної діяльності учнів.
Бесіда
1. Наведіть приклади корисних копалин.
2. На які групи поділяються корисні копалини?
ІІІ. Мотивація навчальної діяльності. Повідомлення теми, мети уроку.
Звертається увага, на те, що на цьому уроці учні познайомляться з природними джерелами органічних речовин.
IV. Засвоєння нових знань учнів.
1. Природні джерела вуглеводнів, їх класифікація (розповідь)


|
Газоподібні |
Рідкі |
Тверді |
|
Природний і супутній нафтові гази |
Нафта |
Кам'яне вугілля |
Природні джерела органічних речовин відомі вам ще з уроків географії, природознавства. До них належать:

ТОРФ
НАФТА ПРИРОДНИЙ ГАЗ


БУРЕ ВУГІЛЛЯ КАМ’ЯНЕ ВУГІЛЛЯ


Кам’яне вугілля, газ, нафта, торф – найважливіші природні джерела вуглеводневої сировини. Вуглеводнева сировина належить до вичерпних природних ресурсів. Ця обставина змушує розвідувати нові родовища і разом з тим експлуатувати вже відкриті таким чином, щоб максимально вилучати з них копалини і раціонально, з найбільшою користю використовувати їх. Існує два способи використання цих вуглеводнів: перший – у вигляді палива, як джерела енергії, другий – у вигляді сировини для подальшої переробки. Просте спалювання нафти, газу, вугілля економічно не вигідне. Крім цього, продукти спалювання природних вуглеводнів забруднюють атмосферу. Тому з кожним роком усе активніше йде пошук альтернативних джерел енергії.
2. Альтернативні джерела енергії. Які альтернативні джерела енергії вам відомі? (прогнозовані відповіді учнів)
-біопаливо;
-сонячна енергія;
-енергія морських припливів.
Існують різні погляди на походження горючих копалин.
1. Теорія органічного походження.
2. Теорія мінерального походження.
3. Космічна теорія.
V. Узагальнення та систематизація знань учнів.
Робота з таблицею
|
Природні джерела органічних речовин |
Застосування |
|
|
|
VI. Підсумки уроку.
VII. Домашнє завдання.
Вивчити конспект;
§ 7 (с.36 – 37);
Підготувати реферат та презентацію “Природні джерела вуглеводнів”
 План – конспект уроку № 2
План – конспект уроку № 2
Тема програми: Органічні сполуки. Природні джерела вуглеводнів.
Тема уроку: Природний і супутній нафтові гази, їх склад, використання.
Мета: вивчити склад природного та супутного нафтового газу, Їх використання цих газів в народному господарстві.
Тип уроку: комбінований.
Методи та методичні прийоми: бесіда, лабораторний експеримент, ознайомлення з різними видами палива (колекція), демонстрація зразків продуктів. відеоматеріали.
КМЗ уроку: зразки продуктів, які одержують з природного газу та супутного нафтового газу, презентації учнів, мультимедійний комплекс.
ХІД УРОКУ
І. Організаційний момент.
ІІ. Актуалізація навчальної діяльності учнів.
1. Бесіда
Назвіть найважливіші природні джерела вуглеводнів.
Які альтернативні джерела енергії вам відомі?
Як можна використовувати природні джерела вуглеводнів?
2. Презентація “Природні джерела вуглеводнів”.
ІІІ. Мотивація навчальної діяльності. Повідомлення теми, мети і завдань уроку.
Звертається увага, на те, що на цьому уроці учні познайомляться з продуктами переробки природного та супутного нафтового газів.
ІV. Вивчення нового матеріалу.
1. Природний газ як суміш речовин (розповідь)
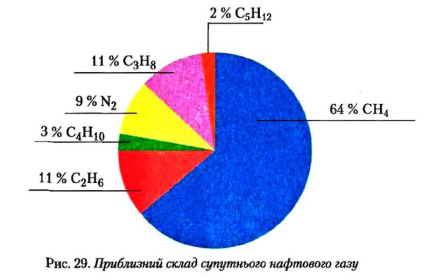
Природний газ добувають із земних надр за допомоги свердловин.

2. Супутні нафтові гази (розповідь викладача)
Супутний нафтовий газ розчинений у нафті і виділяється при її видобутку. Склад супутного нафтового газу відрізняється від складу природного газу меншим вмістом метану, підвищеним вмістом етану, пропану,вищих вуглеводнів. Крім того, у ньому присутні в основному ті самі домішки, що й в природному газі, а саме: азот, вуглекислий газ, благородні гази, водяна пара.

3. Застосування і переробка газу (демонстрація схеми)
V. Узагальнення та систематизація знань учнів.
1. Який газ називають супутнім нафтовим?
2. Робота з підручником § 7 с.38 – 40 . Заповніть таблицю.
|
Продукти переробки газів |
Застосування |
VI. Підсумки уроку. VIІ. Домашнє завдання. Вивчити конспект; § 7 ( с.37 – 40), № 1- 5 (достатній рівень), № 8 (середній рівень), підготувати презентацію, реферат “Природний і супутній нафтові гази”
 План – конспект уроку № 3
План – конспект уроку № 3
Тема програми: Органічні сполуки. Природні джерела вуглеводнів.
Тема уроку: Нафта. Склад, властивості нафти.
Мета уроку: вивчити склад та властивості одного з природних джерел вуглеводнів нафти, ознайомити учнів з основними процесами видобутку з нафти вуглеводнів, необхідних у народному господарстві.
Тип уроку: засвоєння нових знань.
Методи та методичні прийоми: бесіда, розповідь, робота з інтерактивною дошкою, демонстрація слайдів, робота з опорними конспектами, лабораторний експеримент, самостійна робота з колекціями, демонстрація відеоматеріалів.
КМЗ уроку: зразки нафти та продуктів переробки, колба з водою, нафта, презентація «Нафта», опорні конспекти, слайди до уроку, мультимедійний проектор.
ХІД УРОКУ
І. Організаційний момент.
ІІ. Актуалізація пізнавальної діяльності учнів.
Бесіда
1. Що таке природний газ?.
2. Що таке супутній нафтовий газ?
3. Як переробляють природний та супутний нафтовий гази?
ІІІ. Мотивація навчальної діяльності учнів, повідомлення теми та мети уроку.
Про цю корисну копалину людям було відомо здавна. Згадування про темну рідину зі специфічним запахом, що сочиться з каменів, знаходили в працях давньогрецьких та давньоримських істориків: Геродота, Плутарха, Плінія. Уже в ті часи її використовували під назвою “кам’яне масло”. В Єгипті і Вавілоні - як дезинфікуючу мазь, речовину для бальзамування. На близькому Сході нею заправляли ліхтарі, а візантійці змішували з сіркою і виготовляли запальні снаряди. Ця зброя ввійшла в історію під назвою “грецький вогонь”. Що ж це за дивна речовина? Про це ми й дізнаємося з сьогоднішнього уроку.
ІV. Осмислення нового матеріалу.
- Нафта як корисна копалина (розповідь, повідомлення учнів.)
Існує ряд думок про походження нафти:
1. Органічна теорія
Згідно з цією теорією, нафта утворилася із залишків морських організмів і рослин, що осідали протягом мільйонів років на морське дно.
2. Неорганічна теорія
Автором цієї теорії є Д.І.Менделєєв, відповідно до цієї теорії, нафта могла утворитися з карбідів металів, що знаходилися в надрах Землі, і води, яка просочилася туди.
3. Космічна теорія
За цією теорією, нафта могла утворитися з водню і вуглецю при формуванні нашої планети. Поклади нафти трапляються на глибині від десятків метрів до 10 км. На суходолі від 1 - 3 км. Проте нафтоносні пласти є на дні морів та океанів. Промислове добування нафти налагоджено з морських глибин. Добувають нафту через свердловини. Для витискування нафти у свердловину закачують воду чи повітря.
- Склад нафти (фронтальна бесіда, демонстрація зразків, презентації учнів)

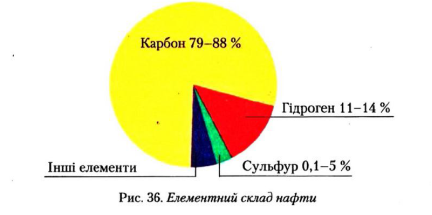
У нафті налічується приблизно 1000 компонентів. Це речовини переважно органічного походження. Вуглеводнева частина складається: парафіни (насичені вуглеводні) – 30-35% циклопарафіни(циклічні вуглеводні) – 25-75%, арени (ароматичні вуглеводні) – 10-20%. Елементарни склад показано на малюнку. У нафтовій фракції, розрізняють такі основні види нафти: метанова нафта, нафтенова нафта, змішана нафта. Також нафту класифікують за фізичними властивостями: легка нафта (густина 0,9г/мл), важка нафта ( густина більша за 0,9г/мл)
- Фізичні властивості нафти (демонстраційний дослід, опорні конспекти)
Нафта – це густа масляниста рідина, має специфічний запах. Нафта різних родовищ має чорний, червоно – коричневий, жовто – зелений, майже не має кольору. Нерозчинна у воді, на поверхні утворює плівку. На нафту як найважливіше джерело сировини одним з перших указав Д. І. Менделєєв. На початку XX ст., ще за життя Д. І. Менделєєва, почалося переведення кораблів військово-морського флоту найбільших держав з вугільного палива на нафтове.
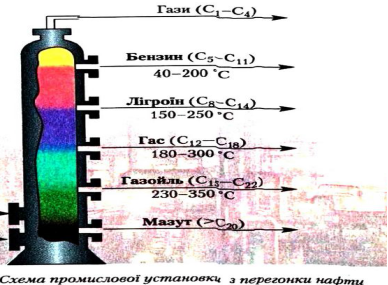
4. Способи переробка нафти (демонстрація промислової установки з перегонки нафти, )
І спосіб: пряма перегонка. Грунтується на фізичних методах розділення сумішей, а тому хімічний склад не змінюється.
Продукти:
ІІ спосіб: крекінг - високотемпературна переробка нафти для одержання продуктів із меншою молекулярною масою. Термічний крекінг проводять при нагрівання вихідної сировини, наприклад, мазуту, до температури 450–550 °С при тиску 20–70 атм. Крекінгу піддають гас, мазут, газойль. При цьому молекули вуглеводнів із великим числом атомів Карбону розщеплюються на дрібніші молекули насичених і ненасичених вуглеводнів. Таким способом добувають здебільшого автомобільний бензин. Каталітичний крекінг поводять при наявності каталізаторів (АL2О3 та Sі2О3) при температурі 480°С – 490 та атмосферному тиску 1-5 атм. Крекінгу піддають газойль Під час каталітичного крекінгу разом із реакціями розщеплення відбуваються реакції ізомеризації. Якість бензину під час такого крекінгу краща.
V. Узагальнення та систематизація знань учнів.
1) Поясніть зміст вислову Д. І. Менделєєва: «Нафта — не паливо. Палити можна й асигнаціями».
2) Чим відрізняється крекінг-процес від фракційної перегонки нафти?
3) Які необхідні людям матеріали синтезують на основі продуктів переробки нафти?
4) Яка фракція первинної переробки нафти використовується для виготовлення бензину?
VІ. Підсумки уроку. Домашнє завдання.
Вивчити конспект;
§ 8 ( с.42);
Підготувати повідомлення про «Cпособи переробки кам'яного вугілля”.
 План – конспект уроку № 4
План – конспект уроку № 4
Тема програми: Органічні сполуки. Природні джерела вуглеводнів
Тема уроку: Продукти перегонки нафти, їх застосування. Детонаційна стійкість бензину.
Мета: вивчити основні наукові принципи й технологічні процеси переробки нафти, показати широку сферу використання нафтопродуктів; сформувати поняття про детонаційну стійкість бензину
Тип уроку: комбінований
Методи та методичні прийоми: бесіда, розповідь, робота з інтерактивною дошкою, демонстрація слайдів, робота з опорними конспектами, лабораторний експеримент, самостійна робота з колекціями, демонстрація відеоматеріалів.
КМЗ уроку: презентація «Застосування нафтопродуктів», зразки нафти та продуктів переробки, схема ректифікаційної колони, мультимедійний комплекс, слайди до теми, опорні схеми.
ХІД УРОКУ
І. Організаційний момент.
ІІ. Перевірка домашнього завдання
Розв’язування кросвордів, які склали учні,обговорення рефератів.
ІІІ. Актуалізація навчальної діяльності учнів
Бесіда
1. Які види нафти вам відомі?
2. Назвіть основні теорії походження нафти.
3. Опишіть фізичні властивості нафти.
IV. Мотивація навчальної діяльності
Сьогодні ми продовжуємо вивчати продукти переробки нафти.
V. Засвоєння нових знань
1. Продукти переробки нафти (розповідь, демонстрація ректифікаційної колони)
Сира нафта звичайно не застосовується. Для одержання з нафти технічно цінних продуктів її піддають переробці. Як ви знаєте, існує два способи переробки нафти: первинна переробка, яка полягає в перегонці нафти; вторинна переробка: крекінг та риформінг. Перегонку нафти здійснюють на нафтопереробних заводах. Нафтопереробні заводи виготовляють нафтопродукти й сировину для промисловості – нафтохімії. В Україні переробку нвфти здійснюють нафтопереробні заводи: Лисичянськ (Луганська обдл.), Херсонський, Одеський, Кременчуцький (Полтавська обл.), Дрогобицький (Львівська обл.), Надвірнянський (Іванофранківська обл.).


2. Застосування нафтопродуктів.
У процесі перегонки нафти одержують світлі нафтопродукти: бензин, лігроїн, гас, солярове масло, а в залишку- чорну рідину- мазут
Продукти перегонки нафти мають різне застосування.
Лігроїн використовують як пальне для дизельних двигунів, а також як розчинник у лакофарбовій промисловості.


ГАС БЕНЗИН


ЛІГРОЇН ДИЗЕЛЬНЕ ПАЛИВО


МАЗУТ ГУДРОН
Великі кількості його перероблють на бензин. Гас застосовують як пальне для реактивних ідизельних двигунів, а також для побутових потреб. Він складається з вуглеводнів, що містять у молекулах у середньому від 9 до 16 атомів Карбону.
Бензин застосовують як пальне для двигунів внутрішнього згорання, розчинник масел, каучуку, окисник тканин від жиру.
Газойль (або солярове масло) використовується як моторне пальне, а мастила - для змазування механізмів.
Мазут, як паливо для теплових електростанцій, кораблів, заводів, як котельне рідке пальне. В останні роки нафту та продуктидедалі більше використовують як цінну сировину для хімічної промисловості: пластмаси, синтетичні волокна, синтетичний каучук, метанол, аміак. Азотні добрива, стимулятори росту, протруйники.
- Детонаційна стійкість бензину характеризує здатність вуглеводнів у його складі протистояти самозайманню за стискання. Це найважливіша кількісна характеристика палива, за якою визначають його сортність і застосування у двигунах різних конструкцій. Мірою детонаційної стійкості пального служить ОЧ; воно чисельно дорівнює вмісту (в об’ємних %) ізооктану (ОЧ= 100) в його еталонній суміші з н – гептаном (ОЧ=0), при якому ця суміш має однакові, антидетонаційні властивості з пальним, яке випробовують. Очевидно, для поліпшення якості пального доцільно застосовувати такі процеси переробки нафти, завдяки яким утворюються вуглеводні розгалуженої будови, зокрема процес каталітичної ізомеризації.
VI. Узагальнення та систематизація знань учнів.
Робота з таблицею «Нафта»
|
Що я знав (знала) з підручників, TV, інтернет- ресурсів |
Що дізнався (дізналася), на уроці |
Про що хочу дізнатися |
|
|
|
|
VII. Підсумки уроку. Домашнє завдання. Вивчити конспект;
§ 8 ( с.42), № 8 (с.48); Скласти кросворд « Нафта»
 План – конспект уроку № 5
План – конспект уроку № 5
Тема програми: Органічні сполуки. Природні джерела вуглеводнів
Тема уроку: Кам’яне вугілля, продукти його переробки
Мета уроку: поглибити знання учнів про джерела вуглеводнів, показати роль кам'яного вугілля як джерела різних хімічних речовин; ознайомити учнів з головними принципами процесу коксування кам'яного вугілля; використання продуктів коксування.
Тип уроку: комбінований
Методи та методичні прийоми: евристична бесіда, лабораторна робота, демонстрація колекції зразків продуктів коксування кам'яного вугілля .
КМЗ уроку: таблиця «Склад кам'яного вугілля і продукти його переробки», опорні конспекти, колекції кам’яного вугілля, презентації, відеоматеріали, мультимедійний комплекс.
ХІД УРОКУ
І. Організаційний момент.
ІІ. Перевірка домашнього завдання. Розв’язування кросворду «Нафта»
ІІІ. Актуалізація опорних знань. Мотивація навчальної діяльності.
1. Назвіть головні родовища кам'яного вугілля у світі, в Україні.
2. Подумайте, які речовини входять до складу кам'яного вугілля різних родовищ.
3. Назвіть відомі вам галузі використання вугілля і продуктів його переробки.
ІV. Вивчення нового матеріалу
1. Склад кам’яного вугілля (розповідь, презентація) Згідно з біогенною гіпотезою походження вугілля, воно утворилося з відмерлих рослин в результаті життєдіяльності мікроорганізмів. Утворення вугілля з рослиних залишків відбувалося через кілька стадій:
Торф – Буре вугілля – Кам’яне вугілля – Антрацит
Кам’яне вугілля – природна суміш вуглецю - 10%, органічних сполук- 80:%, вологи, неорганічних домішок у вигляді - шлаку - 20%.
Вугілля — тверда горюча корисна копалина органічного походження. Вугілля дешевше від нафти й більш рівномірно поширене в земній корі. Його природні запаси набагато перевищують запаси нафти.
2. Види вугілля. (демонстрація зразків колекції вугілля).
Основними видами вугілля є: антрацит, кам'яне вугілля, буре вугілля.
Основні види вугілля
 АНТРАЦИТ КАМ’ЯНЕ ВУГІЛЛЯ
АНТРАЦИТ КАМ’ЯНЕ ВУГІЛЛЯ

БУРЕ ВУГІЛЛЯ ТОРФ


3. Переробка кам’яного вугілля (демонстрація схеми переробки).
Є декілька способів переробки вугілля: коксування, газифікація, гідрування.
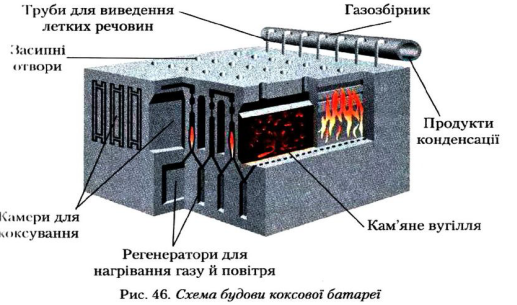
1. Коксування – термічна переробка вугілля, що полягає в його нагріванні без доступу повітря при 900 – 1100 градусіві витримуванні при цій температурі 20 годин. Вугілля розкладається з утворенням: твердого коксу, летких органічних і неорганічних речовин.
Кокс - на 96-98% складається з вуглецю. Є сировиною для виробництва ацетилену.
Кам’яновугільна смола – є сировиною для добування ароматичних вуглеводнів, фенолу, нафталіну і т. д.
Коксовий газ – містить 60% водню, 25% метану, 5% карбон (ІV)оксиду, 4% азоту, 2% нітроген (ІV) оксиду, 2% етену та інших газів. Його використовують для обігрівання печей. Надсмольна вода – водний розчин аміаку, який обробляють сульфатною кислотою і одержують мінеральне добриво амоній сульфат.
2. Газифікація – обробка низькосортного вугілля, бурого вугілля і торфу сумішшю повітря, водяної пари і вуглекислого газу. Одержують генераторний газ.
3. Гідрування – каталітичний процес обробки твердого палива при температурі 500 градусів і тиску 20-70 МПа. Цей процес дає можливість одержувати синтетичний бензин.

V. Узагальнення та систематизація знань учнів.
Розгляньте колекцію продуктів коксування кам’яного вугілля і визначте для кожного: агрегатний стан, зовнішній вигляд, колір, запах, розчинність у воді. Результати запишіть у таблицю
|
Кам’яне вугілля |
|||
|
Ознаки порівняння |
Коксовий газ |
Кокс |
Кам’яновугільна смола |
|
Формули компонентів |
|
|
|
VІ. Підсумки уроку. Домашнє завдання.
Вивчити конспект;
§ 9 с.49-53; №8 с.57;
Підготувати реферат та презентацію на тему «Основні види палива»
 План – конспект уроку № 6.
План – конспект уроку № 6.
Тема програми: Органічні сполуки. Природні джерела вуглеводнів.
Тема уроку: Основні види палива та їх значення в енергетиці країни.
Мета уроку: узагальнити знання учнів про склад та властивості основних джерел вуглеводнів, їх застосування як палива у різних галузях господарства; розвивати вміння учнів класифікувати хімічні об’єкти за різними ознаками, формувати дбайливе ставлення до енергетичних ресурсів своєї країни.
Тип уроку : узагальнення та систематизація знань
Методи та методичні прийоми: фронтальна бесіда, розповідь викладача, демонстрація видів палива, відеоматеріалів, самостійна робота.
КМЗ уроку: комп’ютерна презентація «Основні види палива в енергетиці країни», мультимедійний комплекс, мережа Інтернет – ресурси, підручники, опорні схеми.
ХІД УРОКУ
І. Організаційний момент.
ІІ. Мотивація навчальної діяльності. Постановка мети та завдань уроку ( евристична бесіда)
Що мав на увазі Д. І. Менделєєв, коли говорив «Нафта не паливо, палити можна і асигнаціями» ?
( Справа в тому, що довгий час нафту використовували в якості палива, а Д.І. Менделєєв разом зі своїми однодумцями сприяли розвитку її переробки і раціонального використання продуктів переробки).
Які ж види палива існують в наш час, яке місце посідають в енергетиці країни і чому? Які існують екологічні проблеми, пов’язані з видобуванням і використанням вуглеводневої сировини , способи захисту. Це основні питання, відповідь на які ми сформуємо на протязі нашого уроку. Отже, відкриваємо зошити та записуємо: П’яте грудня, класна робота, тема «Основні види палива та їх значення в енергетиці країни». (Учні записують тему).
Сьогодні ми узагальнимо ті знання, які ви отримали на протязі вивчення розділу « Природні джерела вуглеводнів».
ІІІ. Узагальнення знань та систематизація знань учнів.
1. Основні види палива (розповідь, демонстрація зразків колекції “Основні види палива”, лабораторна робота)
Людина з давніх часів використовувала різні види природного палива для приготування їжі та обігріву житла, а згодом і для виготовлення предметів побуту, зброї тощо. Давайте разом сформулюємо поняття « паливо»
Паливо – це природні або синтетичні речовини, спалювання яких супроводжується виділенням великої кількості теплової енергії.
А тепер розподілимо різні види палива за агрегатним станом та походженням. Порівняйте склад природного і супутнього нафтового газів. Згадаймо застосування продуктів, які одержують з цих газів . Давайте згадаємо склад, фізичні властивості та способи переробки .

 Лабораторна робота « Ознайомлення зі зразками продуктів коксування кам’яного вугілля та різних видів палива»
Лабораторна робота « Ознайомлення зі зразками продуктів коксування кам’яного вугілля та різних видів палива»
Завдання. Розгляньте видані вам зразки продуктів коксування вугілля та різних видів палива. З’ясуйте агрегатний стан, колір, запах, застосування (за інформаційними джерелами). Результати оформіть у вигляді таблиці.
2. Охорона навколишнього середовища. (постановка проблемного питання)
- Які шкідливі речовини утворюються під час переробки вуглеводневої сировини і використання продуктів, одержаних з неї?
- Чим вони небезпечні для довкілля?
- Як можна звести до мінімуму їхню негативну дію?
- Що можемо зробити для цього ми?
Фронтальна бесіда
Проблема зміни клімату планети є найбільш значущою з-поміж глобальних проблем біосфери, зумовлених антропогенним впливом: навіть незначні зміни клімату можуть істотно вплинути на господарську діяльність людини. Незначні, на перший погляд, антропогенні зміни клімату, що розвиваються на тлі його природної мінливості, можуть призвести до порушення стійкості клімату, перетворитися на катастрофічні.
- Назвіть головні екологічні проблеми, зумовлені видобуванням і використанням вуглеводневої сировини.
- Запропонуйте способи захисту навколишнього середовища від продуктів переробки вуглеводневої сировини.
Повідомлення учнів з питань охорони навколишнього середовища в процесі переробки вуглеводневої сировини
Учням за кілька уроків до міні-конференції пропонується підготувати повідомлення (презентації, проекти та інші творчі роботи) з питань:
- Сучасні методи очищення газоподібних викидів в атмосферу.
- Головні методи очищення стічних вод нафтогазових виробництв і шахтних вод.
- Охорона ґрунту від забруднень нафтопродуктами, відходами вуглевидобувної промисловості.
- Безвідходна й маловідходна технології в нафтогазовій галузі.
- Утилізація і знешкодження відходів.
- Національні й міжнародні екологічні стандарти.
Мозковий штурм «Що робити?» Завершуючи попереднє вивчення і обговорення матеріалу, учителем ставиться питання: «Яким чином особисто ви можете запобігти негативному впливу на довкілля, зумовленому використанням вуглеводневого палива і продуктів переробки вуглеводневої сировини?»
Застосування енергозберігаючих технологій.
- утеплення вікон, утеплення стін пінопластом, пластикові вікна, вікна обтягнуті плівкою;
- сортування сміття, здача в пункти збору вторинної сировини: скло, металолом, папір;
- предмети ужитку багаторазового використання: стаканчики, тарілки, сумки;
- ходити пішки чи їздити на велосипеді, гужовий транспорт замість автотранспорту
Після висловлення всіх пропозицій і обговорення підводиться підсумок. Необхідно використовувати всі можливі шляхи для запобігання негативного впливу на довкілля.
ІV. Підбиття підсумків уроку.
Отже, на сьогоднішньому уроці ми з вами узагальнили знання про склад та властивості основних джерел вуглеводнів, їх застосування як палива у різних галузях господарства, розглянули який вплив чинять продукти спалювання вугілля, нафтопродуктів та газу на навколишнє середовище.
Оцінювання роботи в групах та індивідуальної роботи .
А тепер я хочу, щоб ви на декілька хвилин замислились над своїм майбутнім та майбутнім ваших дітей, і зробили правильні висновки, переглянувши цей фільм.
V. Домашнє завдання.
Підготувати презентаційні матеріали по темі “Основні види палива та їх значення в енергетиці країни»;
Реферативні матеріали з теми «Охорона навколишнього середовища від забруднень при переробці вуглеводневої сировини»;
Зберіть інформацію про техногенні аварії, що сталися наприкінці ХХ – поч. ХХІ ст., що призвели до забруднення навколишнього середовища природними джерелами вуглеводнів та продуктами їх переробки. Які їх наслідки? Продумайте способи презентації зібраної інформації.
 План – конспект уроку № 7
План – конспект уроку № 7
Тема програми: Органічні сполуки. Природні джерела вуглеводнів
Тема уроку: Охорона навколишнього середовища від забруднень при переробці вуглеводневої сировини та використанні продуктів її переробки.
Мета уроку: розглянути екологічні проблеми переробки вуглеводневої сировини й використання продуктів її переробки, а також можливі шляхи розв'язання питань охорони навколишнього середовища в процесі переробки й використання вуглеводневої сировини; формувати екологічну свідомість учнів; дати поняття про спектральні методи визначення структури органічних речовин.
Тип уроку: комбінований
Методи та методичні прийоми: міні-конференція, демонстрація схем, презентацій.
КМЗ уроку: презентації учнів з теми міні-конференції, проектор, мультимедійна дошка, підручники, схеми, відео.
ХІД УРОКУ
І. Організаційний момент.
ІІ. Актуалізація опорних знань. Мотивація навчальної діяльності
Фронтальна бесіда за питаннями
1) Назвіть головні джерела вуглеводневої сировини.
2) Згадайте головні способи переробки нафти.
3) Перелічіть головні продукти переробки нафти.
4) Назвіть галузі використання вугілля і продуктів його переробки.
5) Сировиною для яких галузей промисловості є природний газ?
Розв'язування задач
Задача 1. Порівняйте об'єм вуглекислого газу, що виділиться в результаті спалювання: 1 т вугілля і 1 т природного газу (0,90 метану, 0,05 етану, 0,03 пропану й 0,02 об'єми азоту). Яка кількість тепла при цьому виділиться?
Задача 2. Приблизний елементний склад нафти: 82-87 % — С; 1114,5 % — Н; 0,01-6,0 % — 8 (зрідка — до 8 %); 0,001-1,8 % — N5 0,005-0,35 % — О (зрідка — до 1,2 %) та ін. Які речовини потрапляють в атмосферу внаслідок спалювання вугілля, нафтопродуктів і природного газу? Складіть їхні формули. Укажіть, який вплив вони чинять на навколишнє середовище й організм людини.
III. Вивчення нового матеріалу.
Розповідь викладача
1. Охорона навколишнього середовища під час переробки
Звернемо увагу на органічні забруднювачі навколишнього середовища. В атмосферу потрапляє все більше продуктів неповного згоряння бензину, інших видів моторного палива. Повітря також забруднюється технологічними газовими викидами металургійних і хімічних підприємств. Особливе занепокоєння викликає стан атмосфери у великих промислових регіонах, де концентрація вуглеводнів, фенолу, формальдегіду, аніліну, інших небезпечних органічних речовин нерідко перевищує ГДК у десять і більше разів. Руйнівниками озонового шару є фреони (ССl3F, СНClF2, С2С12F4 та ін.),які потрапляють у повітря із несправної холодильної техніки, аерозольних упаковок. Істотного забруднення зазнає і гідросфера. Великої шкоди морській фауні завдають аварії танкерів, які перевозять нафту і нафтопродукти, аварії на нафтовидобувних платформах . У світовий океан щороку виливається ~10 млн т нафти. Кожна тонна розтікається по поверхні води площею 12 км2, створюючи плівку, яка ізолює воду від атмосфери і порушує екологічні рівноваги. Річки сильно забруднюються стічними водами нафтохімічних та нафтопереробних заводів, підприємств, які виробляють галогенопохідні вуглеводнів, органічні кислоти, альдегіди, фенол та його аналоги, ароматичні сполуки, барвники. Зростає рівень засмічення природних водойм механічними забруднювачами, серед яких переважають відходи полімерних матеріалів і пластмас (використані поліетиленові та поліпропіленові пляшки, мішечки тощо). Негативно впливають на живі істоти, які мешкають в річках і озерах, синтетичні мийні засоби. Земна поверхня потерпає від забруднень відходами полімерних матеріалів та виробів із дах, засобами захисту рослин від хвороб і шкідників. Щороку накопичується у ґрунті, а також потрапляє в озера й річки 4 млн т пестицидів. Досягнення хімії впевнено увійшли в наше життя. Ми використовуємо їх навіть у харчуванні. Нині відомо сотні штучних харчових добавок, частина з яких є консевантами, інші поліпшують смакові якості продуктів. Однак чимало цих речовин шкідливі, особливо для молодого організму. Вони порушують функції шлунку, печінки, загострюють хронічні вороби, викликають алергії, вражають імунну систему. Екологічні проблеми породжує не розвиток хімії та хімічної технології, а недостатній рівень знань людей, які проектують підприємства, дозволяють їх будувати і керують ними. Сучасні хімічна наука і технологія покликані створити безпечні для людини виробничі процеси, зробити вагомий внесок у справу оздоровлення природи і ліквідації негативних наслідків впливу на неї цивілізації.

Фронтальна бесіда з учнями
Проблема зміни клімату планети є найбільш значущою з-поміж глобальних проблем біосфери, зумовлених антропогенним впливом: навіть незначні зміни клімату можуть істотно вплинути на господарську діяльність людини. Незначні, на перший погляд, антропогенні зміни клімату, що розвиваються на тлі його природної мінливості, можуть призвести до порушення стійкості клімату, перетворитися на катастрофічні.
- Назвіть головні екологічні проблеми, зумовлені видобуванням і використанням вуглеводневої сировини.
- Запропонуйте способи захисту навколишнього середовища від продуктів переробки вуглеводневої сировини.
Повідомлення учнів з питань охорони навколишнього середовища в процесі переробки вуглеводневої сировини
Учням за кілька уроків до міні-конференції пропонується підготувати повідомлення (презентації, проекти та інші творчі роботи) з питань:
- Сучасні методи очищення газоподібних викидів в атмосферу.
- Головні методи очищення стічних вод нафтогазових виробництв і шахтних вод.
- Охорона ґрунту від забруднень нафтопродуктами, відходами вуглевидобувної промисловості.
- Безвідходна й маловідходна технології в нафтогазовій галузі.
- Утилізація і знешкодження відходів.
- Національні й міжнародні екологічні стандарти
.
ІV. Підбиття підсумків уроку. Оцінювання роботи в групах та індивідуальної роботи.
V. Домашнє завдання.
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи;
Реферативні матеріали з теми «Охорона навколишнього середовища від забруднень при переробці вуглеводневої сировини».
Підготуватися до контролю навчальних досягнень з теми.
 План – конспект уроку № 8
План – конспект уроку № 8
Тема програми: Органічні сполуки. Природні джерела вуглеводнів
Тема уроку: Тематичне оцінювання навчальних досягнень
Мета уроку: узагальнити знання учнів з теми «Природні джерела вуглеводнів», визначити рівень навчальних досягнень учнів; розуміння головних понять, уміння використовувати їх на практиці.
Тип уроку: контролю знань, умінь і навичок.
Методи та методичні прийоми: письмова контрольна робота за варіантами, тестовий контроль.
КМЗ уроку: періодична система хімічних елементів Д. І. Менделєєва; картки з завданнями, колекції «Кам’яне вугілля», «Основні види палива», «Нафта», зошит тест-контроль.
ХІД УРОКУ
І. Організаційний етап:
Перевірка готовності учнів до уроку.
ІІ. Тестова контрольна робота.
Варіант 1.
Завдання 1-9 мають по чотири варіанти відповідей. У кожному завданні лише ОДНА ПРАВИЛЬНА відповідь. Оберіть правильну відповідь та позначте її у бланку відповідей.
1. Згадайте для чого проводиться перегонка нафти
а) для отримання тільки ароматичних вуглеводнів
б) отримання різних нафтопродуктів
г) отримання тільки метану і бензину
2. Вирізнити основний компонент природного газу
а) метан б) азот в) водень г) аміак
3. Згадайте, який продукт можна отримати при коксуванні кам’яного вугілля
а) амоніак б) кисень в) газойль г) гас
4. Вирізніть, що використовують як паливо для тракторів
а) бензин б) мазут в) лігроїн г) бензин
5. Згадайте в результаті переробки чого добувають сажу, водень, синтез-газ, ацетилен
а) алканів б) нафти в) природного газу г) кам’яного вугілля
6. Згадайте при переробці чого залишком є мазут
а) кам’яного вугілля б) гасу в) супутнього газу
7. Вкажіть, що можна добути з нафти:
а) лігроїн, газойль, мазут
б) бензин, гас, газойль
в) бензин, ліг роти, гас, газойль, мазут
г) бензин, газойль, мазут
8. Впізнайте, який із процесів розщеплення нафтопродуктів дає якісніший бензин:
а) термічний
б) каталітичний
в) з використанням пониженої температури
г) крекінг
9. Згадайте: нафта – це:
а) водний розчин органічних речовин
б) суміш продуктів окиснення
в) суміш високомолекулярних сполук
г) суміш вуглеводнів
Завдання 10-14 мають на меті встановлення відповідності. До кожного стовпчика, позначеного цифрами, доберіть відповідник, позначений буквою, і впишіть їх у бланк.
10. Встановіть відповідність між фракціями перегонки нафти та температурами кипіння:
1. Бензин а від 180 до 3000С
2. Лігроїн б від 2700С до 3500С
3. Гас в від 400С до 2000С
4. Газойль г від 1200С до 2400С
11. Встановіть відповідність між джерелами вуглеводнів та продуктами їх переробки:
1. Природний газ а гас
2. Кам’яне вугілля б метан
3. Нафта в газолін
4. Супутні гази г кокс
12. Встановіть відповідність між фракціями мазуту та їх використання:
1. Вазелін а. дизельне паливо
2. Солярове масло б. для косметичних ліків
3. Парафін в. дорожне будівництво
4. Гудрон г. виробництво свічок
13. Встановіть відповідність між вихідними речовинами та продуктами крекінгу нафтопродуктів.
1. С14Н30 а. С5Н12 + С5Н10
2. С10Н22 б. С3Н8 + С3Н6
3. С6Н14 в. С7Н16 + С7Н14
4. С4Н10 г. С2Н6 + С2Н4
Завдання 14-26 передбачають певні обчислення і мають чотири варіанти відповідей. Оберіть правильну відповідь та позначте їх у бланку відповідей.
15. Розрахуйте скільки літрів карбон (IV) оксиду утвориться в результаті згоряння 5 моль октану.
а) 89,6 л б) 896 л в) 22,4 л г) 44,8 л
16. Вкажіть масу кисню потрібного для повного спалювання 22,4 л метану:
а) 6,4 г б) 4,6 г в) 64 г г) 164 г
17. Розрахуйте, яка маса вуглецю утвориться при термічному розкладі 4 моль метану:
а) 48 г б) 46 г в) 56 г г) 96 г
18. Допишіть рівняння реакції
2С2Н6 + ? О2 4СО2 + 6Н2О
а) 5 б) 7 в) 9 г) 11
19. Визначити яку масу ацетилену необхідно для добування 268,8 л етану при реакції гідрування ацетилену.
а) 3,12 г б) 312 г в) 31,2 г г) 0,312 г
20. Обчисліть кількість речовини етену об’ємом 44,8 л
а) 4 моль б) 3 моль в) 2 моль г) 1 моль
21. Визначіть масову частку вуглецю в антрациті, якщо 10 г антрациту спалили у кисні з утворенням карбон (IV) оксиду об’ємом 18 л (н.у.)
а) 96,43% б) 95,5% в) 98% г) 94,4%
22. Розрахуйте, який об’єм етану знадобиться для одержання 1 т ацетилену, якщо практичний вихід становить 10% від теоретичного:
а) 861,54 кг б) 0,86154 кг в) 86,154 кг г) 8,6154 кг
23. Визначіть який об’єм етилену можна добути при дегідруванні етану, що міститься в 2240 м3 супутних нафтових газах з масовою часткою етану 20%
а) 224 м3 б) 448 м3 в) 44,8 м3 г) 22,4 м3
24. Розрахуйте,який об’єм ацетилену можна добути з 15 кг кальцій карбіду масова частка домішок в якому 25,8%
А) 5,250м3 б) 38,9 м3 в) 52,5м3 г)3,895м3
25. Визначіть яку масу толуолу можна добути з 2,5т вугілля, якщо 1м3 коксового газу містить 10 г толуолу, а при нагріванні 1 т вугілля до 10000С утворюється 250 м3коксового газу
А)6,25кг б) 3,05 кг в)6кг г)10 кг
26. Визначіть яку масу бензолу можна добути при нагріванні вугілля масою 3 т, якщо з вугілля масою 1 т утворюється 250 м3 газу, а при промисловому добуванні бензолу з коксового газу,1м3 газу містить 30 г бензолу
А) 11,5 кг б)22,5кг б) 10кг г) 5,5 кг
Повторити конспект; підготувати реферати до теми “Органічні сполуки і здоров’я людини».


![]()
![]()





![]()









![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()




1
-
дякую за методрозробку


про публікацію авторської розробки
Додати розробку
