Конспект уроку "Речовина і поле"
Тема: Речовина і поле. Початкові відомості про будову речовини. Молекули. Атоми.
Мета: формувати в учнів уявлення про речовину та поле, фізичні тіла; розвивати добросовісне відношення до навчання, комунікативних умінь; виховувати дисциплінованість, естетичне сприйняття світу.
Тип уроку: урок вивчення нового матеріалу.
Зміст нового навчального матеріалу:
- Фізичні тіла. Речовина і поле. Матерія.
- Молекули. Початкові відомості про будову атома.
- Ознайомлення з розвитком атомно-молекулярного вчення про будову речовини.
Список використаних літературних джерел:
- Фізика. Підручник для 7 класу загальноосвітніх навчальних закладів / Головко М.В., Засєкін Д.О., Засєкіна Т.М., Коваль В.С., Крячко І.П., Непорожня Л.В., Сіпій В. К.: Педагогічна думка, 2015. С. 248: іл.
Хід роботи
І. Актуалізація опорних знань.
Інтерактивна вправа.
Учнів по черзі читають запитання і відповідають на них.
- Які ви знаєте природничі науки? (фізика, хімія, біологія…)
- Що вивчає фізика? (фізика вивчає загальні властивості матерій та явищ у природі)
- Як фізики пізнають світ? (за допомогою наукових досліджень та експериментів)
- Чим досліди відрізняються від спостережень? (тим, що в спостереження не втручається людина, воно відбувається в природних умовах, досліди відбуваються в штучно створеному середовищі за участю людини)
ІІ. Виклад нового навчального матеріалу.
- Фізичні тіла. Речовина і поле. Матерія.
Коли ми вивчаємо різноманітні фізичні явища, то звертаємо увагу на те, що всі вони розглядаються відносно різних предметів або їх утворень (наприклад, танення льоду, свічення монітора, рух футбольного м’яча). Давайте пригадаємо, як ми називаємо ці всі об’єкти в фізиці? Правильно, для позначення всіх цих об’єктів у фізиці використовують науковий термін «фізичне тіло». Наведіть приклади фізичних тіл. Фізичними тілами є Земля, Місяць, Сонце та зорі, вода, лід, комп’ютер, велосипед і т. ін.). У природі спостерігається величезна розмаїтість фізичних тіл, так само як і фізичних явищ. Тіла можуть мати однаковий об’єм та різну форму (наприклад, шматки свинцю та виплавлений з них свинцевий брусок). Тіла можуть мати однакову форму, але різний об’єм (наприклад, повітряна куля та кулька для прикрашання свят). Форма та об’єм тіл можуть змінюватися під дією інших тіл. Так, розплавивши мідний дріт, отримаємо шматок міді неправильної форми. Повітряна кулька на морозі зменшується в об’ємі.
Пояснити особливості перебігу фізичних явищ та властивості тіл можливо лише тоді, коли відомо, з чого вони складаються і як внутрішня будова тіл впливає на їх властивості. Але людину цікавлять не тільки самі фізичні тіла, а й те, з чого вони складаються. Знання про будову речовини необхідні людині для того, щоб уміти їх якнайкраще використовувати. Так, люди помітили, що для полегшення оброблення заліза його слід добре нагріти. До цього часу ковалі в кузнях розігрівають металеві заготовки в спеціальних печах і лише потім виковують з них потрібні деталі. Щоб надати міцності глиняному посуду, його обпалюють, а потім покривають поливою – спеціальним склоподібним сплавом. Для виготовлення автомашин і літаків використовують легкі та міцні матеріали, а для виробництва реактивних двигунів, атомних реакторів використовують жаростійкі матеріали, які не змінюють своїх властивостей за високих температур.
Потреба у речовинах зі спеціально заданими властивостями постійно зростає. Якщо у природному стані потрібних речовин немає або їх недостатньо, вони створюються штучно. Широке застосування в техніці та побуті знайшли такі речовини як пластмаса, гума, капрон, лавсан. До речі, як ці речовини ще називають? (матеріалами). Колись гумові вироби виготовляли з каучуку, який отримували із соку спеціальних дерев. Але потреби в цій речовині з часом настільки зросли, що була створена спеціальна технологія виробництва штучного каучуку.
Для означення всього, що є у Всесвіті, використовують термін «матерія». Теплове випромінювання, яке ми не бачимо, але відчуваємо, наближаючись до радіатора водяного опалення в квартирі, теж є матеріальним, або реально існуючим. Матеріальними є також і радіохвилі, випромінювання мобільного телефону. Людина не відчуває їх за допомогою органів чуттів, але вони існують: їх сприймають радіоприймачі, телевізори, мобільні телефони. Ми не помічаємо випромінювання, що йде від пульта дистанційного керування, але підтвердженням його існування є те, що за його допомогою вмикається телевізор. А ще це випромінювання можна «побачити» за допомогою цифрової відеокамери.
- Молекули. Початкові відомості про будову атома.
Для дослідження будови речовини фізики використовують спеціальні пристрої та обладнання. Але навіть і деякі прості досліди можуть дати певні уявлення про особливості будови речовини.
Демонстрації. Шматок крейди ви можете розламати навпіл, потім ще раз і ще. Зовсім маленький шматочок можна розтерти в руках – на пальцях залишаться дрібні частинки речовини, з якої складається крейда. Якщо крапельку фарби помістити у склянку з водою, вона розчиниться і зафарбує воду. Відливши частину розчину в іншу склянку і доливши її чистою водою, помітимо, що розчин буде мати світліше забарвлення. Зробивши так декілька разів, переконаємося, що з кожним разом розчин стає світлішим.
Демонстрації. Про те, яким чином розташовані частинки речовини, з якої складається тіло, можна дізнатися з таких дослідів. Легенько затиснувши в руці резервуар побутового термометра будемо спостерігати, як стовпчик рідини піднімається вгору. Оскільки температура людського тіла зазвичай більша, ніж температура в кімнаті, то рідина стовпчика термометра нагрівається і її рівень збільшується. Отже, які можна зробити з цього досліду висновки? (під час нагрівання рідина розширюються).
Чи можете ви навести приклади розширення тіл від нагрівання в природі та побуті? Влітку під час нагрівання на сонці розширюються залізничні рейки, тому між ними залишають проміжки. Поршневі кільця для двигунів автомобілів виготовляють таким чином, щоби вони могли розширюватися під час роботи двигуна. Отже, при нагріванні залізо розширюється, а при охолодженні звужується. Яким чином можна пояснити ці явища? З попередніх дослідів ви знаєте, що речовини складаються з частинок дуже малих розмірів. Коли частинки віддаляються одна від одної за певних умов (наприклад, під час нагрівання тіла), об’єм тіла збільшується. А коли частинки речовини зближаються, то об’єм тіла зменшується.
Демонстрація моделі молекули води.
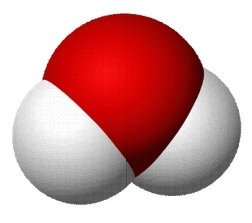 Як дослідили фізики, величина проміжків між частинками визначає властивості фізичних тіл, які можуть перебувати у твердій, рідкій, газоподібній формі. У твердих тілах і рідинах відстані між частинками значно менші, ніж в газах. Частинки, з яких складається більшість речовин, у фізиці називають молекулами. Вода складається з молекул води, а найменшими частинками цукру є молекули цукру. Молекули різних речовин мають різні розміри. Але всі вони надзвичайно малі. Якби молекули речовин, з яких складається яблуко, можна було би збільшити до розмірів яблука, то саме яблуко збільшилося би до розмірів Землі. Навіть надзвичайно тонка наноплівка алмазоїда складається з декількох шарів молекул. Отже, розміри молекул є надзвичайно малими. Навіть розміри «гігантських» молекул, отриманих людиною, у тисячі разів менші від товщини людського волосся. Розмір фулеренів (модифікація молекул вуглецю) не перевищує один нанометр (1 нм = 10-9 м).
Як дослідили фізики, величина проміжків між частинками визначає властивості фізичних тіл, які можуть перебувати у твердій, рідкій, газоподібній формі. У твердих тілах і рідинах відстані між частинками значно менші, ніж в газах. Частинки, з яких складається більшість речовин, у фізиці називають молекулами. Вода складається з молекул води, а найменшими частинками цукру є молекули цукру. Молекули різних речовин мають різні розміри. Але всі вони надзвичайно малі. Якби молекули речовин, з яких складається яблуко, можна було би збільшити до розмірів яблука, то саме яблуко збільшилося би до розмірів Землі. Навіть надзвичайно тонка наноплівка алмазоїда складається з декількох шарів молекул. Отже, розміри молекул є надзвичайно малими. Навіть розміри «гігантських» молекул, отриманих людиною, у тисячі разів менші від товщини людського волосся. Розмір фулеренів (модифікація молекул вуглецю) не перевищує один нанометр (1 нм = 10-9 м).
Науковим результатом, отриманим фізиками та хіміками під час вивчення молекулярної будови речовини, став висновок про те, що однакові властивості найменших частинок будь-якої речовини, яка не містить домішок, надають їй специфічних ознак, за якими вона відрізняється від інших речовин. Саме тому вода, виділена із солодкого чаю, апельсинового соку, мильного розчину не буде відрізнятися за основними властивостями від звичайної чистої води. Молекули води однакові у різних сполуках, і вони є характерними тільки саме для такої речовини. Як ви побачили, молекули є надзвичайно маленькими частинками речовини. Але дослідження показали, що й вони також є подільними. Щоб зобразити, наприклад, молекулу води, яка складається з двох атомів Гідрогену (частинок речовини, яку називають воднем) та одного атома Оксигену (частинки речовини, яку називають киснем), використовують кружечки різного кольору.
Демонстрація моделі атома Водню
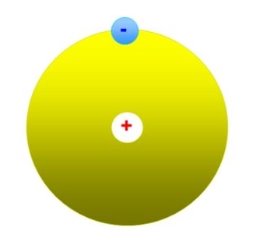 На сьогодні відомо мільйони типів молекул, що складаються з різної кількості атомів. Атоми надзвичайно малі. Тому їх не можна побачити в оптичний мікроскоп. Найменша частинка, яку можна спостерігати в такий мікроскоп, має складатися з мільярда атомів. Фізики змогли «побачити» атом тільки після створення складних приладів – електронного мікроскопа та іонного проектора. Дослідження, виконані такими приладами, підтверджують подільність речовини.
На сьогодні відомо мільйони типів молекул, що складаються з різної кількості атомів. Атоми надзвичайно малі. Тому їх не можна побачити в оптичний мікроскоп. Найменша частинка, яку можна спостерігати в такий мікроскоп, має складатися з мільярда атомів. Фізики змогли «побачити» атом тільки після створення складних приладів – електронного мікроскопа та іонного проектора. Дослідження, виконані такими приладами, підтверджують подільність речовини.
Фізики встановили, що атоми також не є неподільними. Вони складаються з дрібніших частинок. Досліди англійського вченого Е. Резерфорда показали, що в середині атомів розташоване ядро, розміри якого в сто тисяч разів менші, ніж розміри всього атома. Незважаючи на такий малий розмір, в ядрі сконцентрована майже вся маса атома. Навколо ядра, яке має позитивний заряд, обертаються електрони – негативно зарядженні частинки.
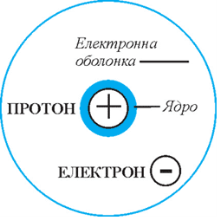 Будова ядра теж виявилася складною. Ядро складається з протонів (позитивно заряджених частинок) та нейтронів (частинок, які не мають електричного заряду) і має позитивний заряд. Найпростіший атом Гідрогену складається з позитивно зарядженого ядра, навколо якого обертається один електрон. Навколо ядра атома Гелію обертаються два електрони. Така модель отримала назву планетарної, за подібністю будови атома до Сонячної системи, в якій навколо нашої масивної Зорі обертаються значно менші за розмірами та масами планети. Атом є електрично нейтральним, оскільки за величиною заряд ядра дорівнює сумарному заряду електронів. Якщо атом втрачає електрон внаслідок взаємодії з іншими атомами, він перетворюється в позитивний йон (має надлишок позитивного заряду). Атом, який отримує електрон, перетворюється в негативний йон (надлишок негативного заряду).
Будова ядра теж виявилася складною. Ядро складається з протонів (позитивно заряджених частинок) та нейтронів (частинок, які не мають електричного заряду) і має позитивний заряд. Найпростіший атом Гідрогену складається з позитивно зарядженого ядра, навколо якого обертається один електрон. Навколо ядра атома Гелію обертаються два електрони. Така модель отримала назву планетарної, за подібністю будови атома до Сонячної системи, в якій навколо нашої масивної Зорі обертаються значно менші за розмірами та масами планети. Атом є електрично нейтральним, оскільки за величиною заряд ядра дорівнює сумарному заряду електронів. Якщо атом втрачає електрон внаслідок взаємодії з іншими атомами, він перетворюється в позитивний йон (має надлишок позитивного заряду). Атом, який отримує електрон, перетворюється в негативний йон (надлишок негативного заряду).
3. Ознайомлення з розвитком атомно-молекулярного вчення про будову речовини.
Наукові погляди на внутрішню будову речовини розвивалися зусиллями багатьох поколінь учених. Давньогрецький філософ Левкіпп та його учень Демокріт вважали, що всі речовини у світі й сама людина складаються з дрібних частинок. За припущенням Демокріта ці частинки, названі ним атомами, є неподільними (від грецького atomos – неподільний). Стародавні вчені вважали, що в природі існує декілька видів атомів, з яких утворюються усі речовини. У XVIII ст. видатний російський учений М. В. Ломоносов (1711 –1765) узагальнив тогочасні уявлення і запропонував науково обґрунтоване вчення про будову речовини, за яким речовини складалися з корпускул (частинок, молекул), що, в свою чергу, складаються з хімічних елементів (атомів).
Р. Броун отримав дослідне підтвердження руху молекул, вивчаючи під мікроскопом спори рослин у рідині. На початку XX ст. Е. Резерфорд запропонував планетарну модель будови атома, яка з доповненнями та уточненнями використовується й до цього часу. За цією моделлю в центрі атома розміщується позитивно заряджене ядро, навколо якого обертаються електрони. За подібністю до будови Сонячної системи таку модель атома Е. Резерфорд назвав планетарною. Якщо атом втрачає електрони, він перетворюється в позитивний йон, а якщо отримує – в негативний. Ядро атома складається з протонів і нейтронів, які теж мають складну структуру. Важливу роль у дослідженнях внутрішньої будови речовини відіграли експериментальні та теоретичні праці українських науковців, виконані в Українському фізико-технічному інституті (м. Харків). На початку 1930-х рр. фізики К. Д. Синельников, О. І. Лейпунський, А. К. Вальтер, Г. Д. Латишев здійснили другу в світі штучну реакцію з розщеплення ядер літію. Д. Д. Іваненко створив протонно-нейтронну модель ядра, а разом з І. Є. Таммом розробив обмінну теорію, яка дала можливість пояснити особливості будови ядра атома. У другій половині минулого століття вчені виявили складну будову протона й нейтрона. Для сучасних досліджень внутрішньої будови речовини створюються спеціальні експериментальні установки, однією з яких є, наприклад, адронний колайдер в Швейцарії.
ІІІ. Закріплення знань
Тепер ми проведемо з вами змагання у формі брейн-рингу.
Поділимо клас на дві команди.
Отже, вибирайте капітана команди, і ми почнемо гру.
Перше завдання. Капітан вибирає двоє учнів. Один буде записувати в колонку, із зачитаного списку, тільки речовини, інший – тільки фізичні тіла.
Склянка, зошит, залізо, цвях, скло, папір, дошка, пластик, деревина, дерево, крейда, ручка, пісок, вода.
Друге завдання. Зачитуються зараз запитання, і відповідати команди будуть по-черзі, якщо команда не відповіла, тоді право голосу надається іншій команді.
- Що називають речовиною?
- Які властивості має речовина?
- Що таке матеріал? (це речовина, з якої складається фізичне тіло)
- Із яких частинок складаються молекули? (з атомів)
- Яку будову має атом? (Атом складається з ядра та електронної оболонки)
- Яку будову має ядро атома? (До складу ядра входять протони, нейтрони).
- Що спільного та чим відрізняються між собою протони та нейтрони? ( Протони та нейтрони подібні за масою та відрізняються між собою зарядом).
- Який заряд мають ядро атома та електрони? (Ядро+, електрони-).
Молодці, всі справилися із завданнями.
ІV. Домашнє завдання
- Опрацювати текст параграфа


про публікацію авторської розробки
Додати розробку
