Урок "Спектри випромінювання атомів і молекул"
Тема уроку: Випромінювання та поглинання світла атомом. Неперервний і лінійчатий спектри. Спектральний аналіз.
Мета уроку: навчальна – Продовжити формування уявлень при випромінювання і поглинання світла атомом. Формувати поняття спектра, ознайомити учнів з його утворенням; продовжити формування в учнів уявлення про співвідношення теорії і експерименту в розвитку фізичних теорій.
розвивальна –формувати в учнів вміння користуватися науково-популярною літературою та виявлення творчих здібностей при розв'язуванні вправ;
виховна – виховати трудолюбивість, точність і чіткість при відповідях і розв'язуванні завдань та навчити дітей «бачити» фізику навколо себе.
Формування ключових компетентностей:
•Математична грамотність.
•Компетентності в природничих науках і технологіях.
•Уміння навчатися впродовж життя.
11 клас
Тема уроку: Випромінювання та поглинання світла атомом. Неперервний і лінійчатий спектри. Спектральний аналіз.
Мета уроку: навчальна – Продовжити формування уявлень при випромінювання і поглинання світла атомом. Формувати поняття спектра, ознайомити учнів з його утворенням; продовжити формування в учнів уявлення про співвідношення теорії і експерименту в розвитку фізичних теорій.
розвивальна –формувати в учнів вміння користуватися науково-популярною літературою та виявлення творчих здібностей при розв’язуванні вправ;
виховна – виховати трудолюбивість, точність і чіткість при відповідях і розв’язуванні завдань та навчити дітей «бачити» фізику навколо себе.
Формування ключових компетентностей:
- Математична грамотність.
- Компетентності в природничих науках і технологіях.
- Уміння навчатися впродовж життя.
Тип уроку: урок вивчення нового матеріалу
Обладнання: комп’ютер, проектор, спектроскоп.
Хід уроку
І. Організаційна частина
ІІ. Актуалізація опорних знань
- Яку будову має атом?
- Хто подолав протиріччя планетарної моделі атома?
- І постулат Бора.
- ІІ постулат Бора.
- Коли атом перебуває у збудженому стані?
- Як атом переходить зі збудженого стану в основний стан?
ІІІ. Вивчення нового матеріалу
- Лінійчасті спектри випромінювання газів
Численні дослідження довели, що внаслідок нагрівання до високої температури пари будь-якої хімічної речовини випромінюють світло, вузький пучок якого призма розкладає на кілька пучків.
Лінійчасті спектри — оптичні спектри випущення й поглинання, що складаються з окремих спектральних ліній.
Лінійчастий спектр випущення будь-якого конкретного хімічного елемента не збігається зі спектром випущення інших хімічних елементів і, відповідно, є «візитною карткою» елемента.
 Відбувається й зворотне явище: у випадку пропускання білого світла через пару речовини спостерігається виникнення темних ліній на тлі суцільного спектра. Темні лінії розташовані точно в тих місцях, де спостерігають лінії спектра випускання цього хімічного елемента. Такий спектр називається лінійчастим спектром поглинання.
Відбувається й зворотне явище: у випадку пропускання білого світла через пару речовини спостерігається виникнення темних ліній на тлі суцільного спектра. Темні лінії розташовані точно в тих місцях, де спостерігають лінії спектра випускання цього хімічного елемента. Такий спектр називається лінійчастим спектром поглинання.
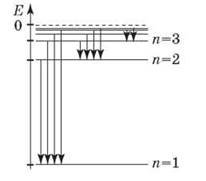
Виходячи з постулатів Бора, можна пояснити процес поглинання і випромінювання енергії атомами. Якщо атом поглинає енергію, то при цьому він переходить у збуджений стан. Його електрон може підніматися на вищу орбіту. Якщо існують вакансії для електрона ближче до ядра, то з часом електрон займає їх, переходячи на більш низький енергетичний рівень. Енергія, яка при цьому вивільняється, випромінюється атомом у вигляді кванта світла.
Якщо світло випромінюють розріджені гази, то атоми газу знаходяться так далеко один від одного, що не чинять ніякого впливу на випромінювання сусідніх атомів, і у спектрі такого джерела будуть спостерігатись лише певні лінії. Так виникають лінійчасті спектри.
- Молекулярні спектри випромінювання (смугасті спектри)
Спектр молекули складається з великої кількості окремих ліній, що зливаються в смуги, чіткі з одного краю й розмиті з іншого. На відміну від лінійчастих спектрів, смугасті спектри створюють не атоми, а молекули, не зв’язані або слабко зв’язані одна з одною. Серії дуже близьких ліній групуються на окремих ділянках спектра й заповнюють цілі смуги.
- Суцільний спектр.
Якщо світло випромінюють тверді тіла, рідини чи дуже сильно стиснені гази, то на випромінювання кожного з атомів суттєво впливають сусідні атоми. Унаслідок цього можна спостерігати розмивання ліній в спектрі випромінювання і плавний перехід від одного кольору до іншого. Так виглядає суцільний спектр.
- Спектральний аналіз.
Лінійчастий спектр кожного хімічного елемента є індивідуальним. Цю властивість використовують для спектрального аналізу сполук, оскільки кожний атом цього елемента в його складі випромінює свої лінії, які не зливаються з лініями інших елементів. Цю речовину обов'язково потрібно перевести в газоподібний стан і дуже нагріти, щоб вона світилась. Прилади, які використовують для спектрального аналізу, називають спектрографами.
Спектральний аналіз має низку переваг і є одним із найбільш чутливих методів дослідження речовин:
· сама речовина не потрібна, потрібне лише випромінювання від неї.
· для проведення досліду потребує дуже мало часу;
· для досліду потрібна дуже мала маса речовини.
ІV. Закріплення вивченого
1). Якісні питання
- Чим відрізняється атом, що перебуває в стаціонарному стані, від атома в збудженому стані?
- Електрон в атомі Гідрогену перейшов із четвертого енергетичного рівня на другий. Як при цьому змінилася енергія атома? Чому?
 2). Навчаємося розв'язувати задачі
2). Навчаємося розв'язувати задачі
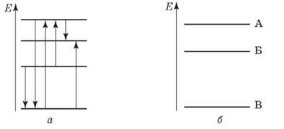
- Визначте, який з переходів (див. рисунок а) відповідає:
а) випромінюванню з найбільшою довжиною хвилі?
б) поглинанню з найбільшою частотою?
- На рисунку б показані три енергетичних рівні атома. Під час переходу з рівня А на рівень Б виникає інфрачервоне випромінювання довжиною хвилі 1,2 мкм; під час переходу з рівня Б на рівень В — світло довжиною хвилі 600 нм. Визначте довжину хвилі випромінювання, що виникає в разі переходу атома з рівня А на рівень В.
V. Підсумок уроку.
1. Побудуйте схему енергетичних рівнів атома водню і поясніть механізм утворення спектральних ліній.
2. У якому випадку атом випромінює квант електромагнітної енергії, а в якому поглинає її?
3. За якою формулою визначають частоту поглинання світла ?
4. Що називають спектром випромінювання ?
5. Які види спектрів випромінювання ви знаєте ? У яких співвідношеннях знаходяться речовини, що випромінюють ці спектри ?
6. Що називають спектром поглинання ? Зобразіть схему досліду з проходження світла через пари натрію і тригранну призму. Який результат цього досліду і про що він свідчить?
7. Що називають спектральним аналізом ? На чому він грунтується ?
VІ. Домашнє завдання: опрацювати § 51;.
Виконати впр. 37 (3).
1


про публікацію авторської розробки
Додати розробку
