Узагальнююча таблиця «Розрахунок кількості теплоти в теплових процесах»
Запропоновано узагальнюючу таблицю «Розрахунок кількості теплоти в теплових процесах» до розділу «Теплові явища».
Матеріал завантажено на сайт у форматі PDF і відкривається у попередньому перегляді не коректно. При завантаженні на свій комп'ютер все виглядає як потрібно.
Охотник Галина Григорівна, вчитель фізики КЗ «СЗШ № 23» Кам'янської міської ради

Фізика, 8 клас
До розділу «Теплові явища»
|
Очікувані результати навчально-пізнавальної діяльності учнів |
|
|
|
Знаннєвий компонент |
Діяльнісний компонент |
Ціннісний компонент |
|
розуміє: властивості теплового руху; особливості руху атомів i молекул речовини в різних агрегатних станах речовини; володіє поняттям, формулює: визначення фізичної величини (температура, внутрішня енергія, кількість теплоти, питома теплоємність, питома теплота плавлення, пароутворення, згорання палива) та їхні одиниці; знає: два способи зміни внутрішньої енергії тіла; види теплообміну; пояснює: графіки теплових процесів (нагрівання/ охолодження, плавлення/ тверднення, пароутворення/ конденсація). |
застосовує: набуті знання в процесі розв’язування задач різних типів та виконання лабораторних робіт; рівняння теплового балансу; аналізує: графіки теплових процесів. |
визначає: переваги і недоліки впливу теплових машин та інших засобів теплотехніки на довкілля; усвідомлює: необхідність використання енергозбережувальних технологій; оцінює: роль видатних учених у розвитку знань про теплоту. |
Розрахунок кількості теплоти в теплових процесах
|
Назва процесу |
Кількість теплоти |
Наведена теплота |
Графіки процесу |
Пояснення з погляду МКТ |
|
Нагрівання |
Q cmt
Q f0 |
c вона чисельно дорівнює кількості теплоти, яку необхідно передати тілу масою 1кг, щоб що б підвищити його температуру на 1К |
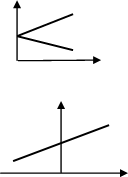
Т нагр. охол. час
0 Q |
Під час нагрівання збільшується кінетична енергія молекул, що призводить до збільшення внутрішньої енергії тіла, мірою зміни якої є кількість теплоти |
|
Охолодження |
Q cmt
Q p0 |
c |
За умови охолодження зменшується кінетична енергія молекул, що призводить до зменшення внутрішньої енергії тіла. Мірою цього зменшення є кількість теплоти, що виділяється, негативне значення якої й указує на це |
|
|
Плавлення |
Qm |
Äæ
чисельно дорівнює кількості теплоти, яку необхідно передати тілу масою 1кг за постійної температури, щоб повністю його розплавити |
Т Тпл
Ткр
Т
Ткр
0 Q |
Під час плавлення до тіла постійно підводиться тепло, але його температура не зростає, тому що воно повністю витрачається на руйнування зв’язків між молекулами |
|
Кристалізація |
Qm |
Äæ
рідина масою 1кг за постійної температури, щоб повністю перейти в кристалічний стан |
Під час кристалізації тепло виділяється тілом у навколишнє середовище, але температура тіла не змінюється, тому що відновлюються зв’язки між молекулами й енергія, що виділяється, дорівнює тій, котра була витрачена на руйнування кристалічної ґратки |
|
|
Пароутворення |
QLm |
L
вона чисельно дорівнює кількості теплоти, яку необхідно передати тілу масою 1кг, щоб перетворити його на пару за постійної температури |
Т
0 час |
Під час пароутворення тепло безупинно підводиться до системи, але температура її при цьому не підвищується, тому що вся енергія, що підводиться, витрачається на розрив між молекулами тіла |
|
Конденсація |
QLm |
L
пара масою 1кг за постійної температури, щоб повністю перейти в рідкий стан |
Т
Ткип
0 Q |
Під час конденсації температура тіла залишається постійною, тому що йде процес відновлення зв’язків між молекулами й виділяється енергія, що дорівнює тій, котра була витрачена на розрив зв’язків під час пароутворення |
|
Горіння ― це самоприскорюван а хімічна реакція, пов’язана з накопиченням теплоти в системі реагуючих речовин |
Qqm |
q
чисельно дорівнює кількості теплоти, яку віддає паливо масою 1кг під час його повного згорання |
|
Під час горіння відбувається процес з’єднання молекул палива з молекулами кисню, при йому зайва енергія виділяється вигляді деякої кількості теплоти |


про публікацію авторської розробки
Додати розробку