Загальна характеристика металів
Про матеріал
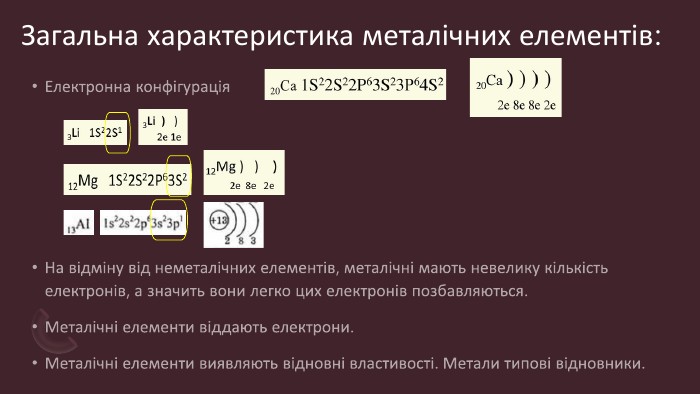
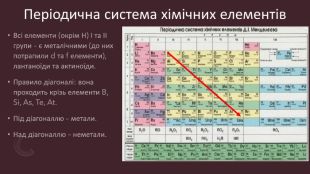
Загальна характеристика металів. Положення в Періодичній системі. Прості речовини метали. Властивості. Корозія. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку