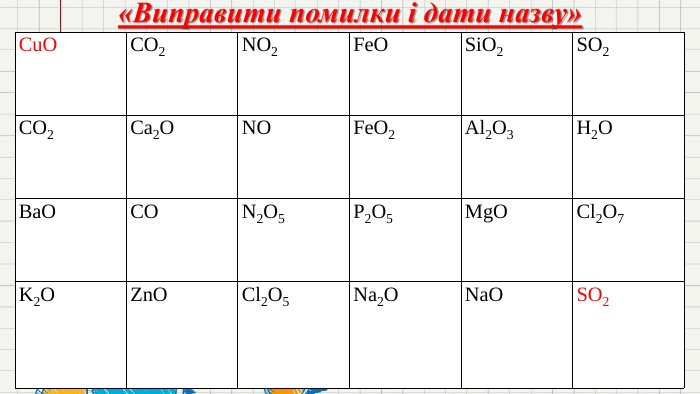
Хімічні властивості кисню
Про матеріал
Хімічні властивості кисню: взаємодія з простими речовинами (вуглець, водень, сірка, магній, залізо, мідь) Реакції сполучення. Поняття про оксиди, окиснення (горіння, повільне окиснення, дихання). Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку