Презентація до уроку на тему " Закон збереження маси"
Матеріал надає можливість учням зрозуміти найголовніший закон природи.

















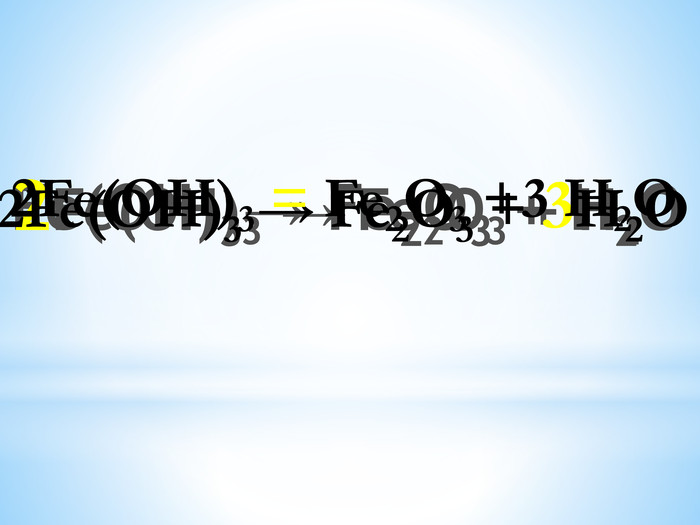











Підрахувати кількість атомів кожного елементу в правій і лівій частині рівняння хімічної реакції. Визначити, у якого елементу кількість атомів змінюється, знайти НСК. Розділити НСК на індекси - отримати коефіцієнти. Поставити їх перед формулами. Перерахувати кількість атомів, при необхідності дію повторити. Останнім перевірити кількість атомів кисню. Алгоритмом розстановки коефіцієнтів у рівняннях хімічних реакцій?
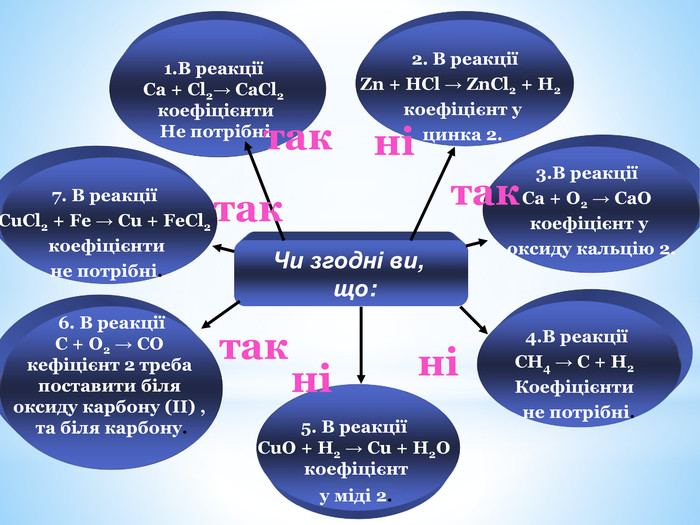
Чи згодні ви, що:1. В реакції Ca + Cl2→ Ca. Cl2 коефіцієнти Не потрібні.2. В реакціїZn + HCl → Zn. Cl2 + H2 коефіцієнт у цинка 2. 3. В реакції Ca + O2 → Ca. O коефіцієнт у оксиду кальцію 2. 4. В реакції CH4 → C + H2 Коефіцієнти не потрібні.5. В реакції Cu. O + H2 → Cu + H2 O коефіцієнт у міді 2. 6. В реакції C + O2 → CO кефіцієнт 2 треба поставити біля оксиду карбону (II) , та біля карбону.7. В реакції Cu. Cl2 + Fe → Cu + Fe. Cl2 коефіцієнти не потрібні. такнінінітактактак
Розставляючи коефіцієнти, слід пам'ятати такі правила:1. коефіцієнт показує число молекул або окремих атомів у рівнян¬ні реакції;2. коефіцієнт ставиться тільки перед хімічною формулою;3. коефіцієнт стосується всіх атомів, із яких складається молеку¬ла, перед якою він стоїть:4. індекс показує число атомів елемента (або груп атомів) у складімолекули;5. коефіцієнт 1, як і індекс 1, не записується. Пам’ятка №1


про публікацію авторської розробки
Додати розробку






























-

Переверзева Інна Євгенівна
17.02.2024 в 23:29
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бакум Альона Миколаївна
18.01.2023 в 19:08
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Безсонова Оксана
16.01.2023 в 18:53
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Стьожка Оксана
16.03.2022 в 09:25
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Kiriyenko Olena
21.01.2022 в 20:47
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Лавська Алла Анатоліївна
05.12.2021 в 19:59
Дякую за презентацію!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Хорольська Наталя Олександрівна
21.01.2021 в 11:49
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Біденко Ніна Дмитрівна
09.12.2020 в 22:34
Дякую. Презентація відмінна!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 5 відгуків