Конспект уроку "Синтез органічних сполук різних класів на основі вуглеводневої сировини "
Урок вивчення нового матеріала з удосконаленням знань, умінь, навичок.
Для з'ясування напрямків синтезу органічних сполук різних класів на основі вуглеводневої сировини; закріплення знань про кам'яне вугілля, його склад, процеси та продукти його переробки; вміння характеризувати напрямки охорони навколишнього середовища від забруднень під час переробки вуглеводневої сировини та використання продуктів її переробки; для розвитку логічного мислення учнів.
Тема: Синтез органічних сполук різних класів
на основі вуглеводневої сировини
Мета уроку: з’ясувати напрямки синтезу органічних сполук різних класів на основі вуглеводневої сировини; закріпити знання про кам’яне вугілля, його склад, процеси та продукти його переробки, про основні види палива та їх значення в енергетиці країни; вміти характеризувати напрямки охорони навколишнього середовища від забруднень під час переробки вуглеводневої сировини та використання продуктів її переробки; розвивати логічне мислення учнів.
Обладнання: підручники, роздатковий матеріал для роботи в групах мультимедійна дошка.
Тип уроку: урок вивчення нового матеріала з удосконаленням знань, умінь, навичок.
- Організаційний етап
- Оголошення теми й мети уроку (презентація – слайд 1 і 2)
- Актуалізація опорних знань
Що таке вугілля? Який його склад? Який основний метод переробки кам’яного вугілля?
Вугілля — горючий матеріал, головна складова частина якого — вуглець. Різновиди вугілля можуть бути природними та штучними. До перших належать: торф, лігніт, кам’яне вугілля, антрацит; до других: кокс, ретортне вугілля, деревне вугілля, брикет. (презентація – слайд 3)
Ретортне вугілля, залишок кам’яного вугілля при отриманні світильного газу; важке, щільне, без домішок, сталевого кольору, йде на пристр. гальванічних батарей. Деревне вугілля отримують або обпаленням в купах при неповному згоранні дерева, або сухою перегонкою дерева, тобто при розжарюванні його без доступу повітря. Деревне вугілля використовується для металургійного виробництв (виплавка заліза), у кузнях (кування заліза), для зварювання заліза. Здатність вугілля поглинати гази й багато рідини дозволяє застосовувати його як засіб для очищення рідин від сивушного масла, офарблюючих речовин.
Антрацит — викопне вугілля. Належить до кам’яновугільних порід, містить 90-94% вуглецю. Колір від оксамитово- до залізно-чорного із сильним блиском скляним або напівметалічним; твердіший за буре та звичайне кам’яне вугілля. Ефективний горючий матеріал, але горить тільки при сильній тязі повітря, без полум’я (або з дуже слабким); без запаху й диму.
Кам’яне вугілля — тверда пальна корисна копалина рослинного походження; різновид вугіллів копалин із високим умістом вуглецю й більшою щільністю, ніж у бурого вугілля. Є щільною породою чорного, іноді сіро-чорного кольору з блискучою, напівматовою або матовою поверхнею. Містить 75-97% і більше вуглецю; 1,5-5,7% водню; 1,5-15% кисню; 0,5-4% сірки; до 1,5% азоту; 2-45% летких речовин; кількість вологи коливається від 4 до 14%; золи — зазвичай від 2-4% до 45%. Вища теплота згорання, у перерахунку на сухий беззольний стан К. в., не менше 30,5-36,8 мДж/кг.
Викладач: Пригадаємо види вуглеводневої сировини ( слайд 4) та основні продукти переробки вуглеводневої сировини (слайд 5)
А тепер серед запропонованих формул знайдіть вуглеводні і дайте їм назву (слайд 6).
Завдання наступного слайду відкриває вам формулу спиртів, альдегідів та карбонових кислот. З’ясуймо належність цих формул до класів (слайд 7).
- Основна частина уроку
Викладач: Органічний синтез — розділ хімії, що вивчає різні способи, методики, засоби визначення, апаратуру тощо для одержання органічних сполук і матеріалів, а також сам процес їхнього одержання в лабораторних умовах чи промисловості. З допомогою органічного синтезу добувають безліч різноманітних органічних речовин. Ця галузь хімії почала стрімко розвиватися лише з розвитком капіталістичного виробництва, аби задовольнити зрослий попит на пальне, мастила, барвники тощо. Вагомий внесок у розвиток синтетичної органічної хімії зробили й українські науковці: П. П. Алексєєв, О. В. Багатський, М. А. Валяшко, А. І. Кипріанов, О. В. Кірсанов, С. М. Реформатський, В. П. Яворський та ін.
Завдання
За допомогою додаткової літератури дайте відповіді на такі питання:
а) Поміркуйте й висловіть припущення: для добування яких речовин доцільно використовувати органічний синтез?
б) Які переваги органічного синтезу?
(Насамперед це спосіб добування сполук з унікальними властивостями, які не трапляються в природі. Найпростіший приклад такої речовини з-поміж вивчених вами - поліетилен, без якого важко уявити сучасне життя.)
в) Наведіть кілька прикладів природних і синтетичних органічних сполук, відомих вам із повсякденного життя.
г) За якою ж ознакою численні органічні сполуки класифікують на природні й синтетичні?
Насамперед за джерелами їхнього видобування. Цю класифікацію спрощено відображає схема. (слайд 8)
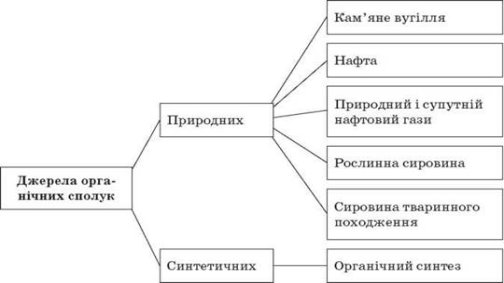
Із природних джерел органічні речовини виділяють переважно в готовому вигляді або завдяки переробці природної сировини. Наприклад, вивчаючи вуглеводні, ви дізналися, що метан і його гомологи видобувають із природного газу, нафти, кам’яного вугілля. Тому ці речовини можна класифікувати як природні органічні сполуки. Натомість етилен і ацетилен через високу реакційну здатність у природі майже не трапляються, тому в лабораторних умовах і промисловості їх синтезують з інших речовин.
Проектуємо на екран схему поділу органічних речовин на природні й синтетичні. (слайд 9)
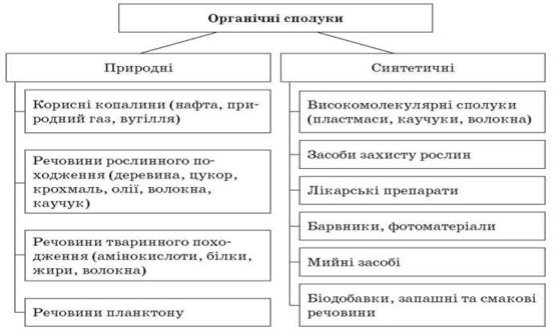
Наводимо приклади природних і синтетичних органічних сполук.
Наводимо приклади добування речовин деяких класів органічних сполук (вивчених у курсі органічної хімії 9 класу).
1) Природний газ — метан.
Неповний розклад метану за t = 1500 °С:
2СН4 ![]() С2Н2 + 3Н2 — утворюється ацетилен
С2Н2 + 3Н2 — утворюється ацетилен
Повний розклад — утворюється сажа:
СН4 ![]() С + 2Н2
С + 2Н2
2) Синтез із вугілля: ![]()
3) Гідрування й дегідрування вуглеводнів, одержаних з метану:
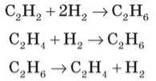
4) Гідратація — приєднання води до алкенів, алкінів:
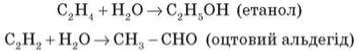
5) Дегідратація — відщеплення води:
![]()
6) Гідрогенгалогенування — приєднання гідрогенгалогенових кислот НСl, НВr, НІ до алкенів, алкінів:
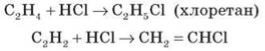
Також може відбуватися зворотна реакція дегідрогенгалогенування:
![]()
7) Окиснення альдегідів до карбонових кислот, наприклад, реакція «срібного дзеркала»:
![]()
8) Реакція Вюрца — подовження карбонового ланцюга:
![]()
9) Одержання жирів:
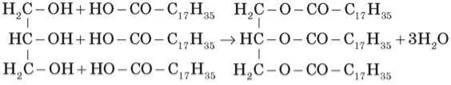
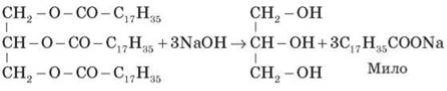
10) Зворотна реакція — гідроліз жирів, наприклад лужний гідроліз:
11) Реакція фотосинтезу — утворення вуглеводів:
![]()
12) Спиртове бродіння глюкози:
![]()
13) Реакція утворення дипептиду з амінокислот:
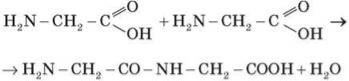
14) Реакція полімеризації:
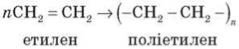
Хочу звернути вашу увагу на деякі базові схеми органічного синтезу (слайд 10, 11, 12)
Пригадаймо, що в основі добування багатьох важливих для хімічної промисловості продуктів є галоген похідні вуглеводнів. Тож запишемо наступну схему. (слайд 13)
- Узагальнення й закріплення знань.
1) Закінчіть рівняння реакцій:

2) Напишіть рівняння реакцій, з допомогою яких можна здійснити перетворення:
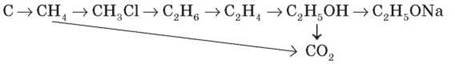
3) Розв’язуємо задачу.
У результаті спалювання 10 г антрациту утворилося 18 л карбон(ІV) оксиду (н. у.). Обчисліть масову частку вуглецю в антрациті.
VII. Підбиття підсумків уроку
VIII. Домашнє завдання


про публікацію авторської розробки
Додати розробку
