Конспект уроку з природознавства для 5 класу на тему "Урок 41 Вода – розчинник."
5 клас
Урок 41
Вода – розчинник.
Мета уроку:
навчальна:
- сформувати поняття про воду як речовину, розчинник, дати поняття
розчину, розчинника та розчиненої речовини, показати значення води в
природі як розчинника;
- розширити знання учнів про класифікацію речовин на розчинні та нерозчинні у воді;
- показати значення води в природі як розчинника.
розвивальна:
- розвивати увагу, мислення, пам’ять учнів, навички групової діяльності на уроці; формувати науковий світогляд;
- розвивати спостережливість та пізнавальний інтерес, дослідницький
підхід до вивчення природних явищ;
- продовжувати формувати вміння виділяти основну думку та робити висновки під час проведеного досліду.
виховна:
- виховувати сумлінність та наполегливість при виконанні завдань;
- сприяти формуванню бережливого ставлення до води;
- виховувати прагнення до роботи в колективі та чіткої організації робочого місця.
Тип уроку: комбінований
Обладнання:підручник, робочий зошит, презентація,відеоматеріали з
Інтернет – ресурсів,вода, хімічні склянки, скляні палички, мірний
посуд, шпателі, кухонна сіль, цукор, крейда, пісок, кристалики
марганцівки, сода харчова, зразки мінеральних
вод України.
Очікувані результати:
- учні пояснюють поняття розчинник, розчинена речовина, розчин;
- наводять приклади розчинів, вміють приготувати розчин та пояснити як відбувається розчинення речовин у воді;
- наводять приклади розчинних і нерозчинних речовин;
- описують результати власних спостережень і дослідів.
Хід уроку.
І . Організаційний момент.
Всі почули дзвінок
Він покликав на урок.
Кожен з вас приготувався,
На перерві постарався.
То ж і ми часу не гаймо
Наш урок розпочинаймо.
ІІ. Актуалізація опорних знань та вмінь
Фронтальне опитування
- В яких станах може перебувати вода у природі?
- Про які властивості води як рідини ви знаєте?
- Де властивості води можна спостерігати в природі?
- За яких умов вода здатна переходити з одного агрегатного стану в інший? Наведіть приклади.
- Що таке гідросфера та з чого вона складається ?
- Які водні об’єкти вам відомі? (океани, моря, річки, озера, ставки, джерела, водосховища)
- Які моря є на території України? (Азовське, Чорне)
- Які річки України ви знаєте? (Дністер, Дніпро, Бистриця, Черемош…)
- Де в Україні найбільше озер? (у Поліському краї)
- Яке найглибше озеро Полісся? (Світязь)
- Яке високогірне озеро в Українських Карпатах вважається одним із семи чудес України? (Синевир)
- Які солоні озера України вам відомі? (Сасик, Сиваш)
ІІІ . Мотивація навчальної та пізнавальної діяльності.
Вправа «Народна скарбничка»
Легенда
Два віслюки йшли однією дорогою, кожний ніс свою поклажу. Одного було нав’ючено сіллю, а іншого — ватою. Перший віслючок йшов дуже-дуже повільно, ледь переплітаючи ноги — такою важкою була його ноша. Інший віслюк був дуже веселий, йшов легко та радіючи.
Невдовзі віслюки підійшли до річки, яку їм слід було подолати. Тварина, що була нав’ючена сіллю, зупинилась у воді й стала купатись — віслюк то лягав у воду, то знову піднімався на ноги, плескався як хотів. Коли віслючок вийшов із річки, його поклажа стала набагато легша. Другий віслюк, поглянувши на першого, також почав купатись. Проте, на відміну від першого, чим довше він купався, тим важче ставала його поклажа — вата, що була нав’ючена на нього.
- Чому ж так сталося?
- Що відбулось із поклажею першого віслюка?
- Чому поклажа другого віслюка стала важчою?
Сіль розчинилась у воді й частка її просто вимилась із поклажі. Тобто сіль є розчинною речовиною. А вата, навпаки, увібрала в себе воду, тому стала важчою. Отже, вата є нерозчинною.
Розчинні та нерозчинні речовини можуть приносити як користь, так і бути шкідливими. Тому, чим більше ми знаємо про розчинні речовини, тим легше нам буде в житті.
Вода може розчиняти різні речовини. Довести це ми зможемо провівши досліди.
ІV. Вивчення нового матеріалу.
За поширеністю вода займає перше місце на Землі. Вона життєво необхідна речовина, без неї не обійтись, її нічим не замінити.
Вода – це й безмежні океанські та морські простори, й річки та озера, мальовничі ставки, а також дощ і сніг, хмари в небі. Від нашого зору в надрах Землі приховане ще одне потужне джерело води – підземні та ґрунтові води. Джерело утворилося внаслідок того, що не вся вода, яка потрапляє на землю з дощем та снігом, випаровується. Частина її проникає у глибші шари ґрунту й утворює там запаси води. Саме цю воду людина отримує з криниць та свердловин.
Вода – це скарб, який потрібно оберігати. Вона незамінна речовина в харчуванні людини та живленні тварин і рослин. Вода також зручний шлях сполучення між населеними пунктами, невтомна трудівниця з вироблення електроенергії, окраса природи. На нашій планеті є великі природні запаси води, однак несолоної (питної) води на нашій планеті в тисячі разів менше, ніж солоної. Нестача питної води відчутна вже тепер, і їй загрожує забруднення. Тому прийнято закони про охорону вод, за цим стежить держава. Зберегти воду чистою означає зберегти здоров’я, життя, красу довкілля.
Та вода має ще унікальну властивість: вона утворює з багатьма твердими, рідкими, газоподібними речовинами однорідні суміші. Ці суміші мають назву розчинів.
Здатність речовин розчинятися у воді називають розчинністю.
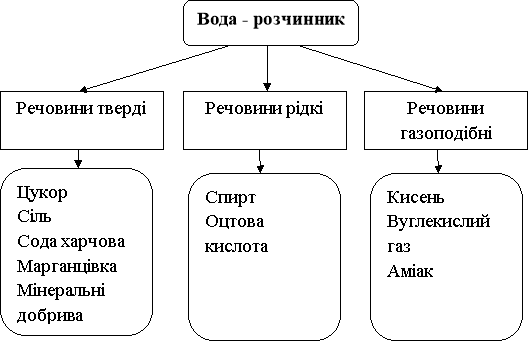
У воді розчиняються тверді, рідкі і газоподібні речовини.
Доведемо, що вода є розчинником.
Дослід 1. Розчинення кухонної солі у воді.
Дослід 2. Розчинення цукру у воді.
Висновки до дослідів:
- Яку властивість води ми дослідили?
- У якому агрегатному стані були сіль і цукор були до розчинення у воді?
- Які агрегатні стани мають утворені розчини?
- Чи можна побачити часточки розчинених речовин у розчинах?
- Скільки речовин входить до складу розчинів?
- Так що ж таке розчини?
Розчини – це однорідні суміші двох і більше речовин.
Висновок: цукор та сіль розчиняються в воді.
Вода є розчинником. Цукор і сіль є речовиною розчиненою у воді. Ми отримали розчин.
Вода + цукор = розчин
Природні розчини: солона вода в морях і озерах, вода в мінеральних джерелах, кров людей і тварин, сік рослин.
Речовини розчиняються у воді не в будь – якій кількості, а лише до певних меж. У 1 л. води може розчинитися 2 кг цукру. І все, далі цукор розчинятися не буде.
Розчини поділяють на:
- розбавлені (мало розчиненої речовини) та концентровані (багато розчиненої речовини);
- насичені (стільки розчиненої речовини, що вона перестала розчинятися) та ненасичені (розчинена речовина ще розчиняється)
Дослід 3. Розчинення глини у воді.
Дослід 4. Розчинення крейди у воді.
Дослід 5. Розчинення піску у воді.
Висновок: глина, крейда,пісок не розчиняються у воді.
Такі речовини називають нерозчинними.
Речовини нерозчинні: пісок, глина, крохмаль, олія, нафта, гас, бензин.
Проте слід пам’ятати, що абсолютно нерозчинних речовин у природі немає. Якщо занурити у воду скляну паличку або кусочок золота чи срібла, то вони у мізерно малих кількостях розчинятимуться у воді. Як відомо, вода, що була у контакті зі сріблом, убиває мікроби.
Існує легенда, що коли армія Олександра Македонського навесні 327 року переможно вступила на землю Індії, серед іі солдатів почалась якась пошесть. Олександр Македонський змушений був відмовитися від подальшого просування війська вглиб країни.
Але хворіли не всі. Сам Олександр і більшість його прибічників залишалися здоровими. Пихаті воєначальники були переконані, що їх уберегли боги. Насправді ж весь секрет полягав у тому, що солдати пили воду зі звичайного посуду, а військові воєначальники з «незвичайного».
- Із чого були виготовлені незвичайні келихи воєначальників ?
- Як срібло їх захистило?
(Срібло має бактерицидні властивості, зовсім нерозчинних речовин не існує.)
Скло, срібло, золото, а також олія, гас і чадний газ – це приклади практично нерозчинних у воді речовин. Прикладами малорозчинних у воді речовин є гіпс, кисень, азот. Багато речовин розчиняються у воді дуже добре, наприклад цукор, спирт, сіль. Отже, розчинність насамперед залежить від природи речовини.
Розчинність більшості твердих речовин залежить і від температури: з підвищенням температури вона, як правило, зростає. У земній корі існує багато розчинних у воді речовин: гіпс, солі, вапняк, крейда.
Гази та рідини також здатні розчинятися у воді. Проте, гази гірше розчиняються у гарячій воді, ніж тверді речовини. Адже під час нагрівання молекули газу віддаляються одна від одної на великі відстані. Частина з них виходить за межі посудини і в розчині їх залишається менше. Тому розчинність газів зростає із зниженням температури і підвищенням тиску.
Газовані мінеральні води, наприклад «Оболонська», «Миргородська», «Трускавецька» та багато інших, готують, розчиняю чи вуглекислий газ у воді з мінеральних джерел. Столовий оцет готують з оцтової кислоти (це рідина) та води.
Отже, розчини можна приготувати з води та твердої речовини, води та рідини, води та газоподібної речовини.
Розчин містить не менше двох компонентів, один з яких розчинник, а інший – розчинена речовина.
Розчинник – це компонент розчину, який перебуває у тому самому агрегатному стані, що й розчин.
Так, якщо змішати кухонну сіль (тверда речовина) і воду (рідина), утвориться рідкий розчин. У цьому випадку вода – розчинник, а сіль – розчинена речовина. Проте часто розчини утворюються речовинами, які перебувають в однакових агрегатних станах, наприклад спирт (рідина) і вода (рідина). У такому разі розчинником вважається той компонент, якого більше.
Розчинники поділяють на органічні та неорганічні.
Існує багато органічних розчинників: нафтові, спирти, прості та складні ефіри тощо. Органічні розчинники дуже широко застосовують, коли виготовляють пластмаси, лаки, фарби, синтетичні волокна, смоли, клеї в гумовій промисловості. Їх також застосовують і з іншою метою, наприклад для хімічного чищення одягу.
До неорганічних розчинників належать рідкий аміак (він є розчинником для лужних металів, фосфору, сірки, солей та речовин), рідкий сірчистий ангідрид (розчинник для багатьох органічних і неорганічних з’єднань) тощо. Проте найпоширенішим і найкращим неорганічним розчинником, вживаним для великого числа неорганічних і органічних сполук, є вода.
Вода утворює однорідні суміші з багатьма твердими, рідкими, газоподібними речовинами. Такі суміші називаються розчинами.
На розчинність також впливає температура. Переважна більшість твердих речовин краще розчиняються в гарячій воді, ніж у холодній. Газоподібні ж речовини, навпаки, гірше розчиняються в гарячій воді.
Також необхідно знати, що на розчинність впливає стан подрібнення речовини: чим дрібніші частинки, тим швидше вони розчиняться у воді.
Отже, розчинник – це те, що розчиняється у воді, а розчин – це сам розчинник + розчинна речовина.
![]()
![]() Склад розчину
Склад розчину
Розчинник Розчинена речовина
Щоб приготувати розчин необхідно визначити масу розчинної речовини і об'єм розчинника. Масу розчину обчислюємо за формулою:
маса розчину = маса розчинника + маса розчинної речовини
- Як ви думаєте, чому воду відмірюють мірним циліндром, а не зважують?
Воду не зважують, бо її маса дорівнює об’єму, на відміну від інших речовин на Землі.
Запам’ятай:
числові значення маси та об’єму води однакові. Це означає, що 100 мл води мають масу 100 г, 1 л води — 1 кг. Воду не зважують, її легше виміряти мірним посудом.
Усі речовини залежно від їхньої здатності розчинятися у воді поділяються на три групи: розчинні, малорозчинні та нерозчинні.
Розчинена речовина – це речовина, яка повністю розчиняється, може змінюватися її агрегатний стан.
Властивості розчинення речовин:
- Тверді речовини краще розчиняються в теплому розчиннику.
- Газоподібні речовини краще розчиняються в холодному розчиннику.
- Дрібні частинки розчиняються швидше.
- При помішуванні збільшується швидкість розчинення.
Складання схеми на дошці.
Використання людиною води як розчинника в побуті:
- розчиняють пральний порошок у воді;
- бензином чистять жирні плями;
- миють посуд засобом для брудного посуду;
- розводять добриво з водою для підливу вазонів;
- користуються рідким милом, шампунем;
- заварює чай, готує соки;
- лікується мікстурами.
Фізкультхвилинка.
Наберемо з криниці (Нахили тулуба вперед.)
Чистої водиці.
Будемо умиватись, (Імітація умивання.)
Будемо промовляти:
— Водичко, водичко,
Умий діткам личка,
Рожеві та білі, мов яблучка спілі.
Хлюп, хлюп, водиченько,
Хлюп, хлюп на личенько,
І на ручки і на ніжки (Імітують миття рук та ніг.)
V. Засвоєння та закріплення знань учнів
Індивідуальна робота учнів з картками
Підкресли назви речовин,що розчиняються у воді:
пісок,цемент,цукор,олія,кисень,бензин,кухонна сіль,оцтова кислота, нафта, вуглекислий газ, глина, крейда, спирт, крохмаль.
Вправа «Доповни речення»
- Речовини, які розчиняються у воді, називають…(розчинними).
- Речовини, які не розчиняються у воді,…(нерозчинні).
- Вода у розчині називається…(розчинником).
- Речовина у розчині називається…(розчиненою речовиною).
- Компоненти суміші у розчині не видно, тому розчин є сумішшю…(однорідною).
- Якщо кількість речовини у розчині мало, то розчин називають…(розбавленим).
- Якщо речовина у воді вже не розчиняється, то розчин називають…(насиченим).
- Воду можна відміряти за допомогою…(мірного посуду).
- Суміші води з твердими, рідкими і газоподібними речовинами називають…(розчинами).
- Речовина, яка розчиняється у воді,…(розчинена речовина).
- Температура на розчинність речовин …(впливає).
- Більшість твердих речовин краще розчиняється не у холодній,а у …(теплій) воді.
- Газоподібні речовини краще розчиняються у…(холодній) воді, ніж у...(гарячій) воді.
V. Підсумок уроку.
Вправа «Мікрофон».
- Що нового дізнались на сьогоднішньому уроці?
- Що сподобалось під час уроку?
- Що не сподобалось під час уроку?
- Чи важливі ці знання особисто для вас?
Сьогодні ви набули досвіду й нових знань, які залишаться з вами на все життя. Тепер ви знаєте, що таке розчини, як вони утворюються та дізналися про роль води як розчинника.
VІ. Домашнє завдання.
1. Опрацювати §31
1


про публікацію авторської розробки
Додати розробку
