Молекулярна фізика. Основні положення молекулярно-кінетичної теорії
Про матеріал
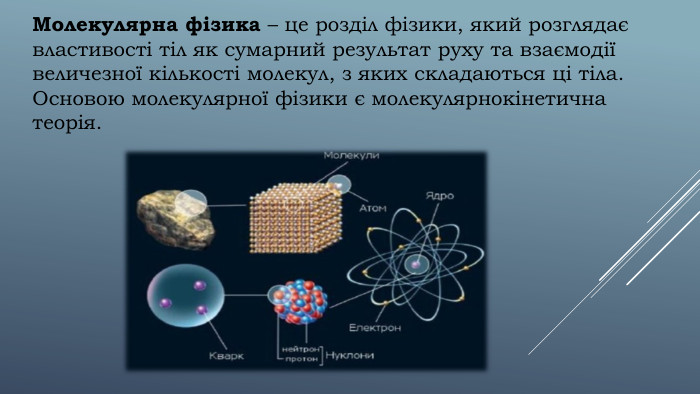
Визначення молекулярної фізики. Основні положення молекулярно-кінетичної теорії. Агрегатні стани речовин. Броунівський рух. Дифузія Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку