Презентація: Можливі ступені окиснення неметалічних елементів 2 і 3 періодів
Про матеріал
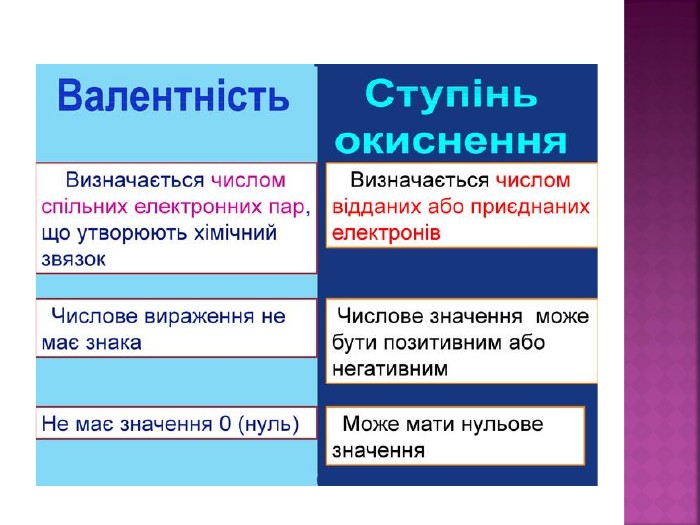
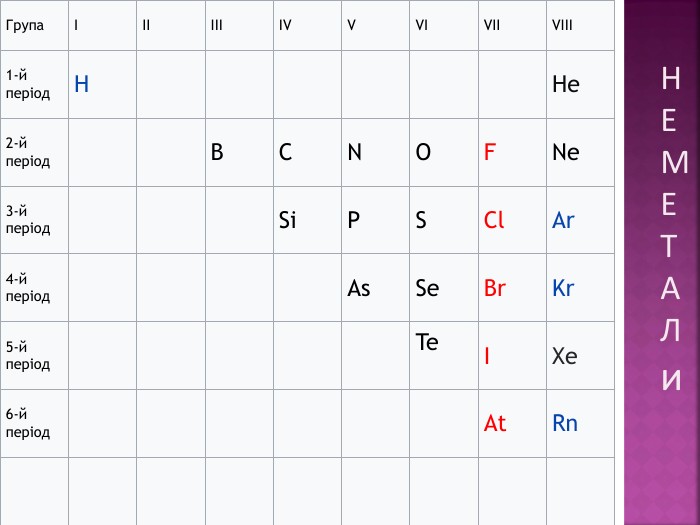
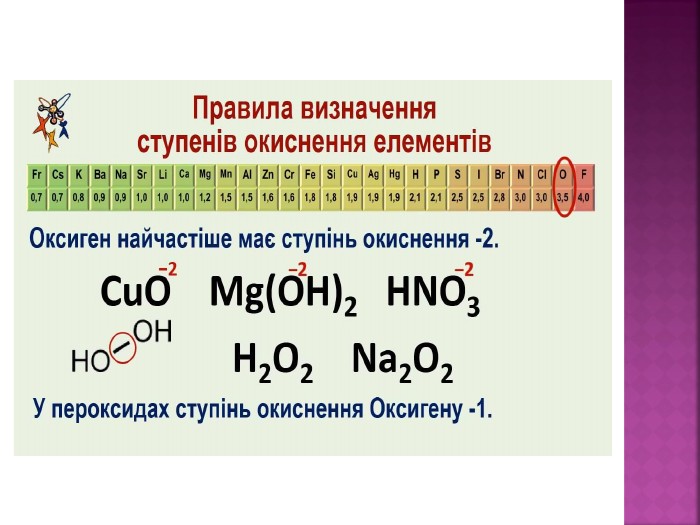
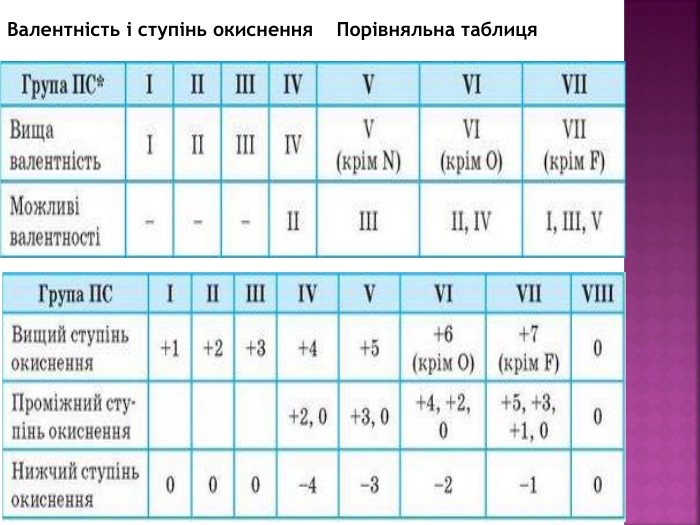
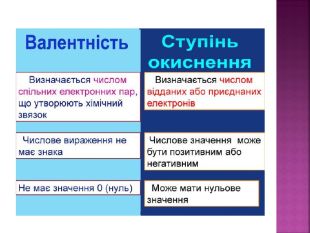
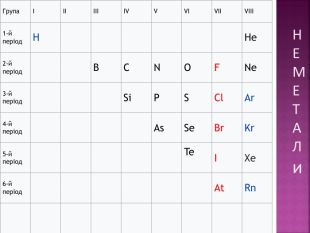
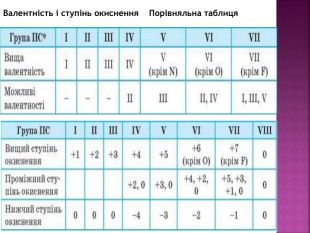
Презентація до уроку "Можливі ступені окиснення неметалічних елементів 2 і 3 періодів" з хімії,11 клас, за новою програмою
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
дякую
-
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку