Презентація для 11 класу "Залізо"
Про матеріал
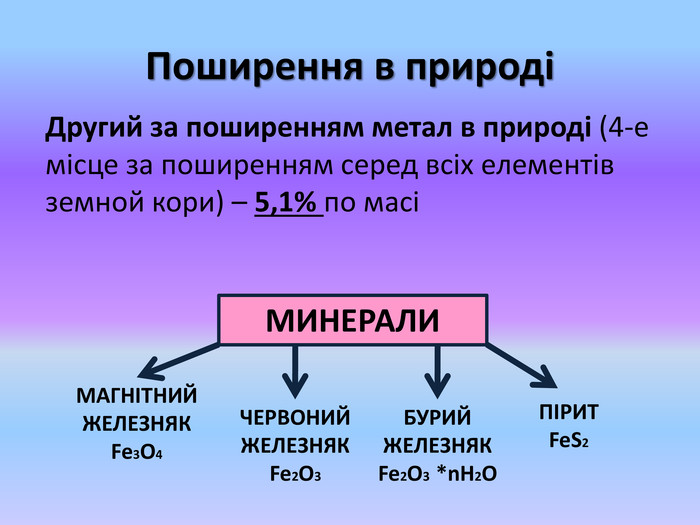
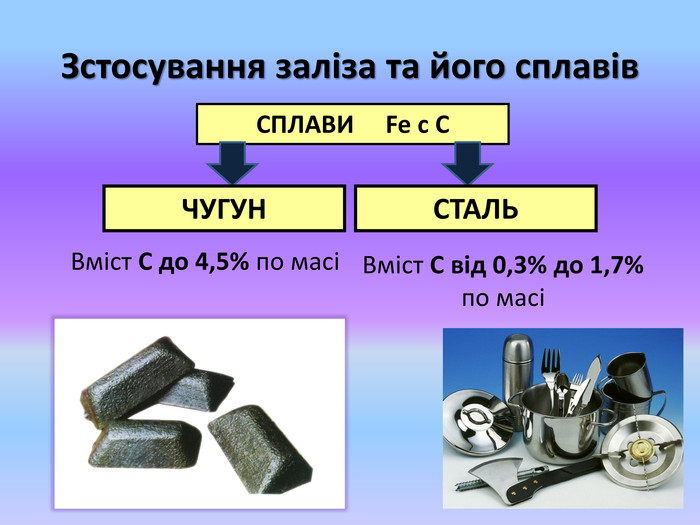
Презентація "Залізо" розроблена для 11 класу за новою програмою, рівень стандарт. Використовувати презентацію можна під час вивчення теми "Феррум.Залізо", як на почтку уроку так як узагальнення набутих знань. Перегляд файлу
Зміст слайдів
ppt
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку