Презентація "Хімічні рівняння"
Про матеріал
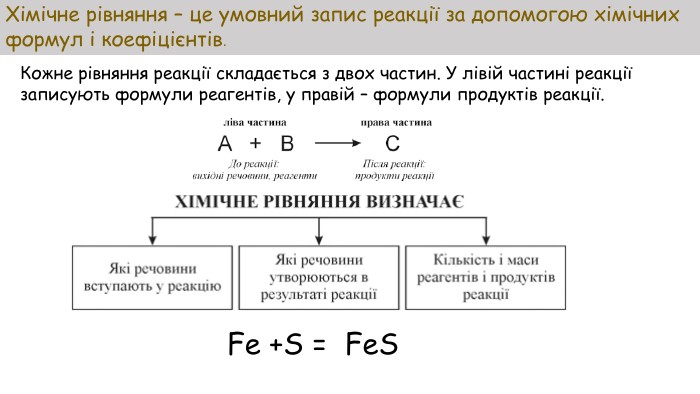
Презентація до уроку "Хімічні рівняння". Формування у учнів поняття про хімічні рівняння та вміння розставляти коефіцієнти в них. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку