Презентація "Маса атома. Атомна одиниця маси. Відносні атомні маси хімічних елементів."
Про матеріал
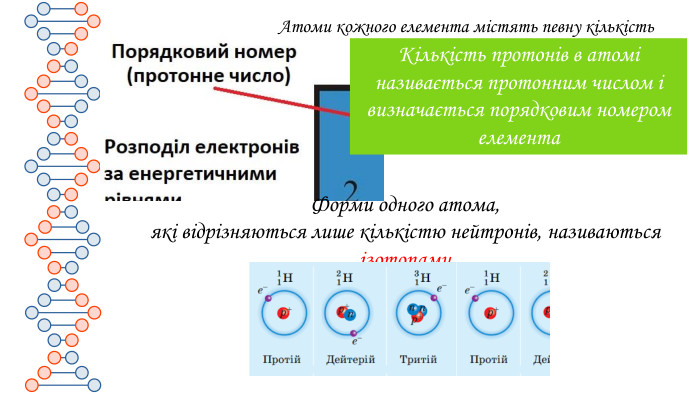
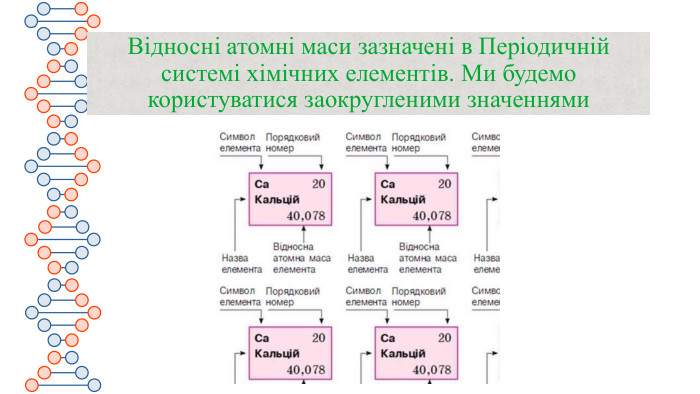
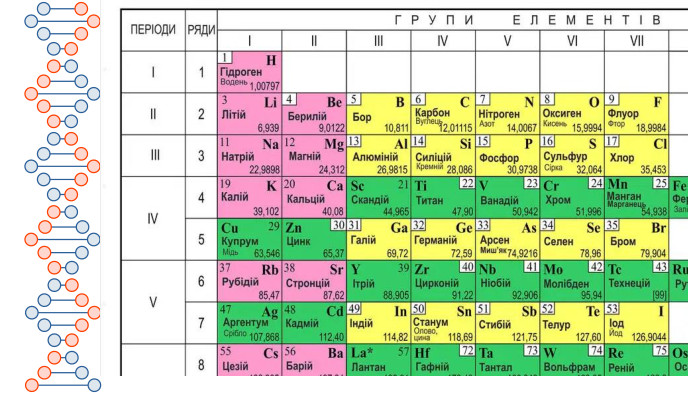
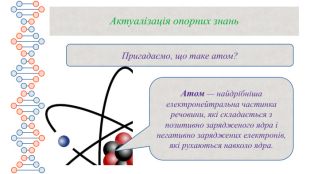
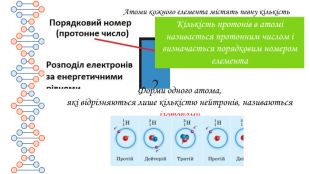
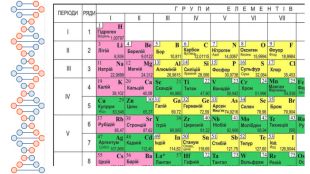
Презентація містить матеріали до уроку хімії на тему "Маса атома. Атомна одиниця маси. Відносні атомні маси хімічних елементів."
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку