Презентація на тему "Алюміній"
Про матеріал
Опис презентації «Алюміній»
Презентація присвячена вивченню алюмінію — одного з найпоширеніших елементів у природі та важливого металу в житті людини.
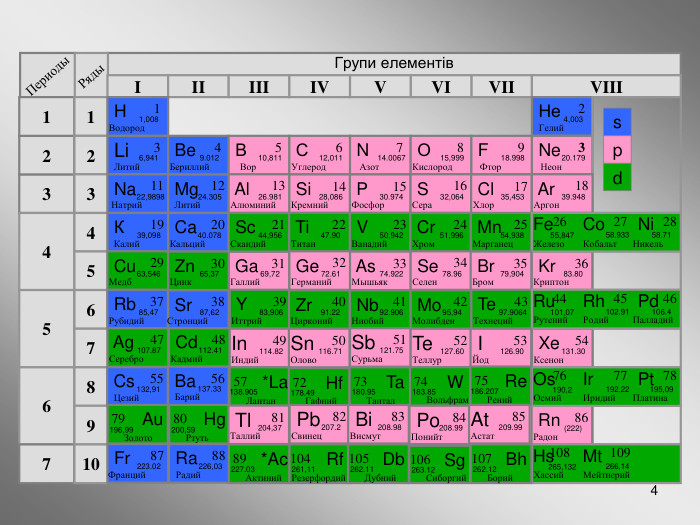
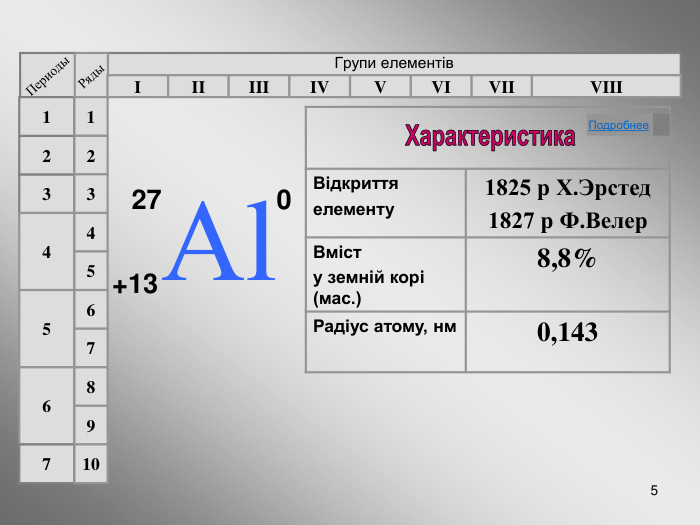
У матеріалі представлено «візитну картку» елемента.
Окремий розділ присвячено тому, де алюміній зустрічається у природі. Учні дізнаються, що в чистому вигляді цей метал не трапляється через свою високу хімічну активність, але широко поширений у складі мінералів і гірських порід, зокрема бокситів, глин та польових шпатів.
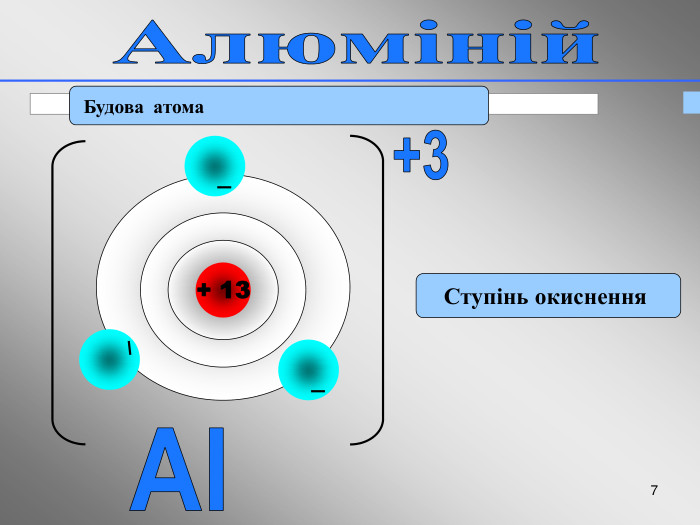
У презентації розглянуто фізичні та хімічні властивості алюмінію.
Також є цікавий факт про алюміній. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку









![* Хімічні властивості 1. з водою (після виделення захисної оксидної плівки) 2Al + 6H2O = 2Al(OH)3 + 3H2 2. з розчинами лугів 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2 3. з соляною та розчиненою сульфатною кислотою: 2Al + 6HCl = 2AlCl3 + 3H2 2Al + 3H2SO4(роз) = Al2(SO4)3 + 3H2 4. с оксидами менш активних металів (алюмотермія) 8Al + 3Fe3O4 = 4Al2O3 + 9Fe 2Al + Cr2O3 = Al2O3 + 2Cr * Хімічні властивості 1. з водою (після виделення захисної оксидної плівки) 2Al + 6H2O = 2Al(OH)3 + 3H2 2. з розчинами лугів 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2 3. з соляною та розчиненою сульфатною кислотою: 2Al + 6HCl = 2AlCl3 + 3H2 2Al + 3H2SO4(роз) = Al2(SO4)3 + 3H2 4. с оксидами менш активних металів (алюмотермія) 8Al + 3Fe3O4 = 4Al2O3 + 9Fe 2Al + Cr2O3 = Al2O3 + 2Cr](/uploads/files/6224799/515783/574461_images/12.jpg)
![* Доповніть речення та закінчіть рівняння реакцій. У Періодичній системі Алюміній розташований у ____ періоді. В електронній оболонці атомів Алюмінію заповнюється ____ електронних шарів. Скільки електронів міститься в іоні Алюмінію Al3+? Ступінь окиснення Алюмінію в сполуках дорівнює ____ У хімічних взаємодіях атоми Алюмінію тільки _______________ Формула Алюміній оксиду __________ Чи зустрічається Алюміній у природі у вільному вигляді _____ Алюміній оксид утворює мінерал _____________ Спосіб відновлення металів з їх оксидів за допомогою Алюмінію називають ______________ Оксид та гідроксид Алюмінію мають ______________ характер. __Al + __H2SO4(розб.) ______________________________ Al(OH)3 + ? [ Al(OH)4]- + ? * Доповніть речення та закінчіть рівняння реакцій. У Періодичній системі Алюміній розташований у ____ періоді. В електронній оболонці атомів Алюмінію заповнюється ____ електронних шарів. Скільки електронів міститься в іоні Алюмінію Al3+? Ступінь окиснення Алюмінію в сполуках дорівнює ____ У хімічних взаємодіях атоми Алюмінію тільки _______________ Формула Алюміній оксиду __________ Чи зустрічається Алюміній у природі у вільному вигляді _____ Алюміній оксид утворює мінерал _____________ Спосіб відновлення металів з їх оксидів за допомогою Алюмінію називають ______________ Оксид та гідроксид Алюмінію мають ______________ характер. __Al + __H2SO4(розб.) ______________________________ Al(OH)3 + ? [ Al(OH)4]- + ?](/uploads/files/6224799/515783/574461_images/13.jpg)














