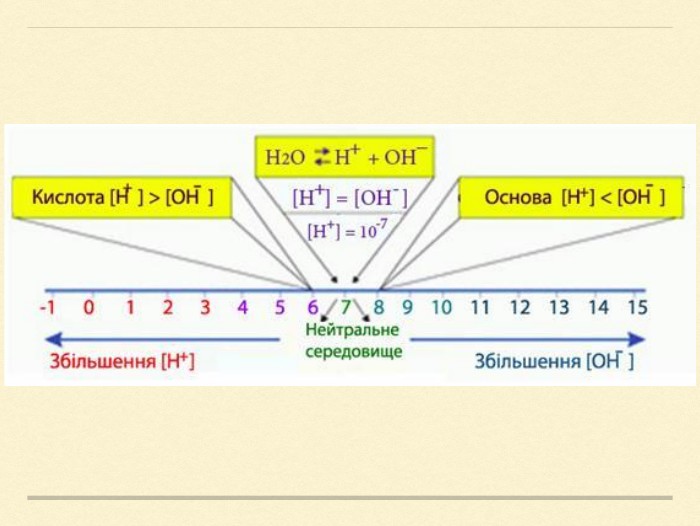
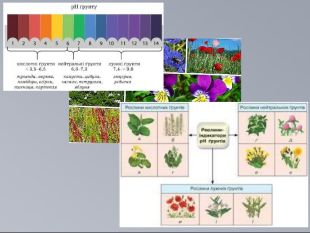
Презентація на тему: "Електролітична дисоціація розчинів електролітів. Водневий показник"
Про матеріал
Вивчення електролітів, вміння складати рівняння реакцій йонного обміну, за умов випадання осаду, виділення газу і утворення малодисоціюючої речовини у хімії. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку