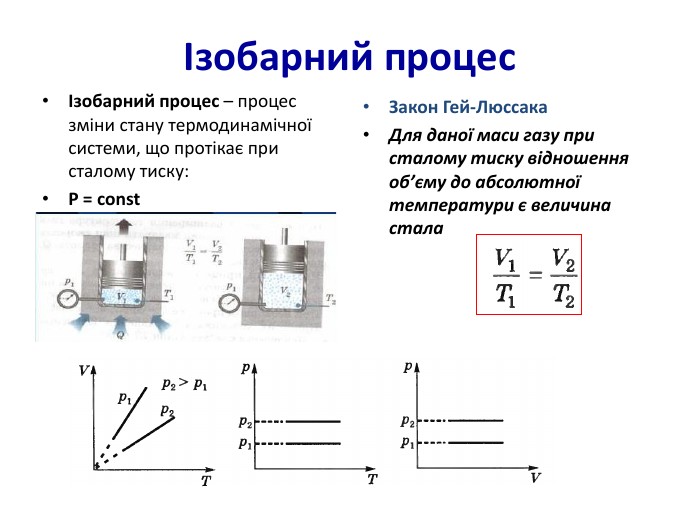
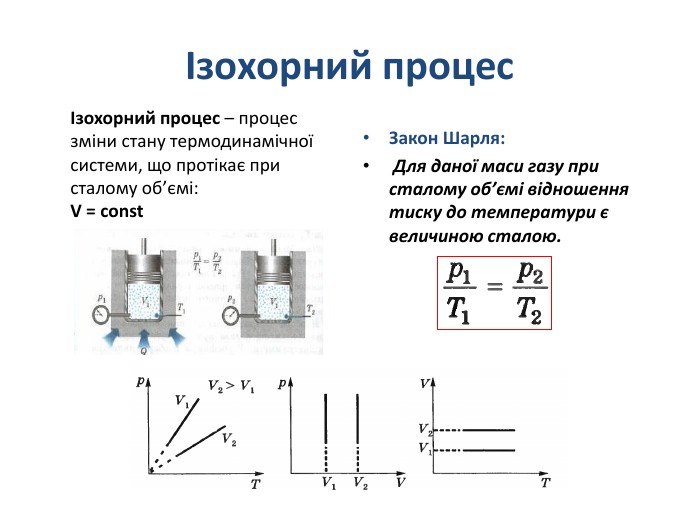
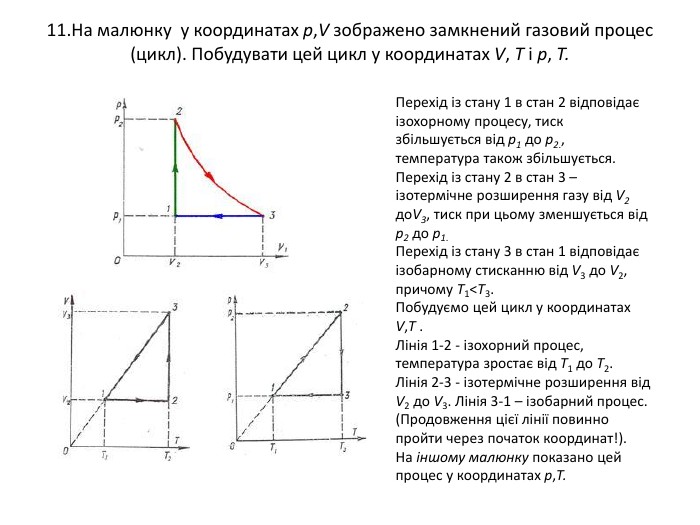
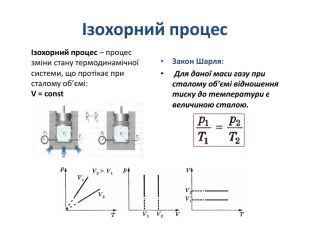
Презентація "Рівняння стану ідеального газу. Ізопроцеси в газах. Задачі на розрахунок параметрів газу"
Про матеріал
Матеріал презентації дає можливість навчити розв'язувати задачі в дистанційній формі навчання. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку