Презентація Способи збирання кисню. Доведення наявності кисню.
Про матеріал
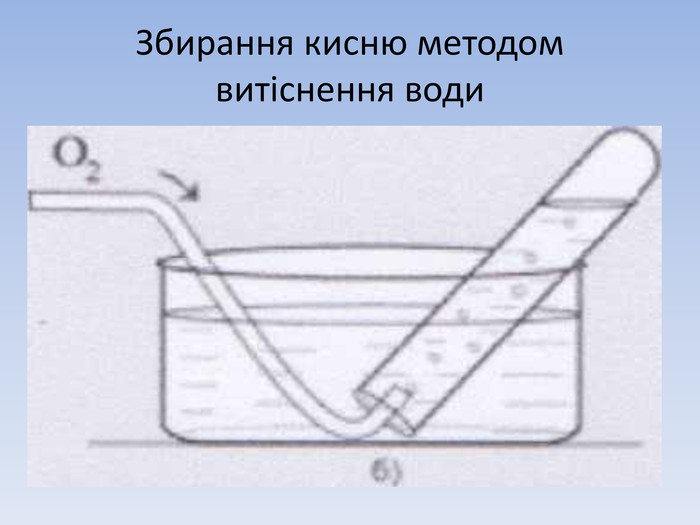
Презентація містить інформацію про методи збирання кисню.Одержання кисню в лабораторії.Практичні завдання для учнів.
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку