Презентация "Урок с элементами STEM технологий "Оксиген. Кислород. Физические свойства кислорода. Круговорот Оксигена""
Урок с элементами STEM-технологии по химии «Оксиген. Кислород. Физические свойства кислорода. Круговорот Оксигена»
Формирование ключевых компетентностей:
- Основные компетентности в естественных науках и технологиях;
- Социальная и общественная компетентность;
- Экологическая грамотность и здоровый образ жизни;
- Информационно-цифровая компетентность.
Цели урока:
- Сформировать понятия об Оксигене как химическом элементе, о кислороде - как простом веществе;
- Ознакомить учащихся с характеристикой элемента Оксигена, с физическими свойствами кислорода, круговоротом Оксигена в природе;
- Развивать познавательный интерес на примере ознакомления с озоном.
Задачи урока:
- Научиться работать с разными источниками информации;
- Описать историю открытия кислорода, строение молекулы;
- Овладеть знаниями о круговороте Оксигена в природе;
- Оценить роль кислорода в жизнедеятельности организмов.
Оборудование: мультимедийный проектор, компьютер, учебники, тетради, пластилин, цветные карточки
Ход урока
I.Мотивация учебной деятельности
Вступительное слово учителя: добрый день дети и наши гости!
Для того, чтобы эффективнее организовать нашу работу на сегодняшнем уроке, давайте определим эмоциональное состояние каждого из нас и класса, в целом.
Для этого, поднимите карточку красного цвета – если настроение у вас радостное, желтую – трудно сказать, синюю – грустное.
А о том, что мы будем изучать на уроке, вы узнаете, отгадав мою загадку.
В чем горят дрова и газ,
Фосфор, водород, алмаз?
Дышит чем любой из нас
Каждый миг и каждый час?
Без чего мертва природа?
Правильно, без …
Девизом нашего урока будут слова нобелевского лауреата Роберта Вудворта
« Своими знаниями я обязан только самому себе. Я сам себя учу химии»
IІ. Подготовительный этап:
Для подготовки к сегодняшнему уроку, вы заранее были распределены на 5 групп:
Разделение учеников на группы
1 группа – «Химики»;
2 группа – «Физики»;
3 группа - «Историки»;
4 группа – «Биологи»;
5 группа - «Технологи».
III.Изучение нового материала
Слово учителя.
Сегодня на уроке мы поговорим о химическом элементе Оксигене и о простых веществах, которые он образует, о веществе, которое так необходимо для нашей жизни.
Слово предоставляется группам учащихся.
1 группа – «Химики»
1. Элемент Оксиген находится в VI группе, главной подгруппе, II периоде, порядковый номер №8, Ar = 16. Валентность II
Неметаллический элемент
2. Заряд ядра атома Оксигена +8. Вокруг ядра вращается 8 электронов
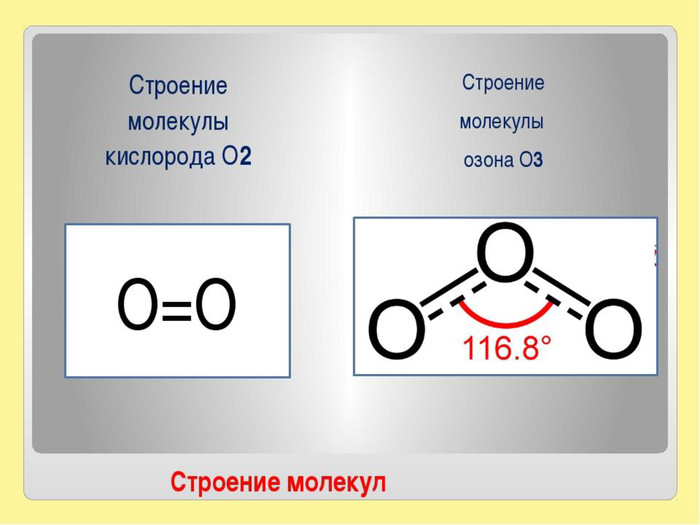
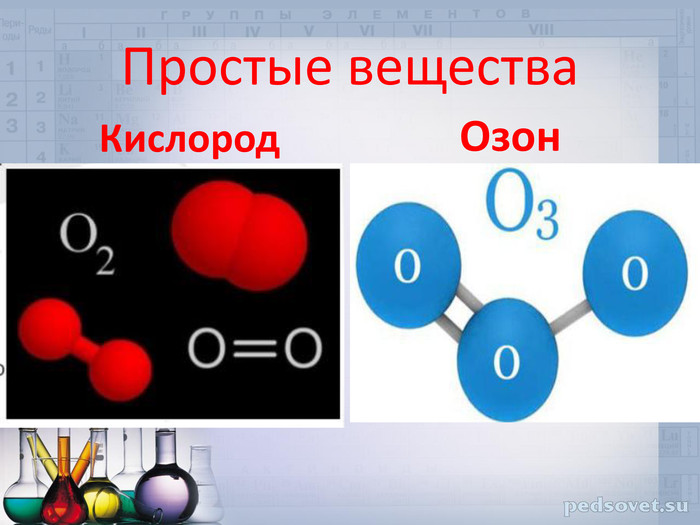
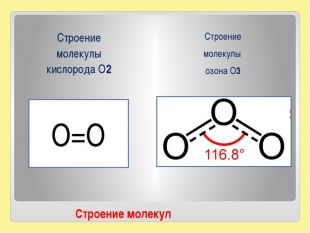
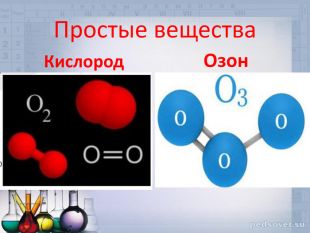
3. Химический элемент Оксиген образует 2 простых вещества: кислород, молекула которого состоит из 2 атомов Оксигена, формула вещества – О2
И озон, молекула состоит из 3 атомов Оксигена, формула вещества - О3
4. Относительные молекулярные массы кислорода=32, озона=48
2 группа – «Физики»
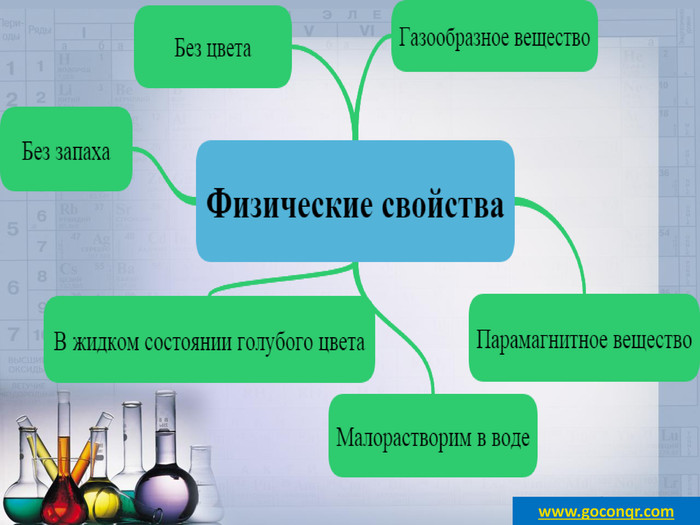
1. При обычных условиях кислород – газ без цвета, вкуса и запаха. Толстый слой кислорода имеет светло-голубую окраску. Кислород малорастворим в воде – в 1 л воды, при температуре 20°С растворяется 31 мл кислорода.
2. Жидкий кислород – это подвижная, слегка голубоватая жидкость, которая кипит при (- 183°С). Твердый кислород – это синие кристаллы, которые плавятся при температуре(-218,7 °С)
Кислород – парамагнитное вещество, в жидком и твердом состоянии притягивается магнитом
3 группа – «Историки»
- 1.
2. Несколькими годами ранее (в 1771 году) кислород получил шведский химик Карл Шееле. Он прокаливал селитру с серной кислотой и затем разлагал получившийся оксид азота. Шееле назвал этот газ «огненным воздухом» и описал своё открытие в изданной в 1777 году книге.
Именно потому, что книга Шееле была опубликована позже, чем результаты опытов Пристли, последний и считается первооткрывателем кислорода
3. Наконец, окончательно разобрался в природе полученного газа французский химик Антуан Лавуазье, воспользовавшийся информацией от Пристли и Шееле. В 1775 году он установил, что кислород является составной частью воздуха, кислот и содержится во многих веществах.
ВЫВОД: заслугу открытия кислорода фактически делят между собой Д.Пристли, К. Шееле и А. Лавуазье.
4 группа – «Биологи»
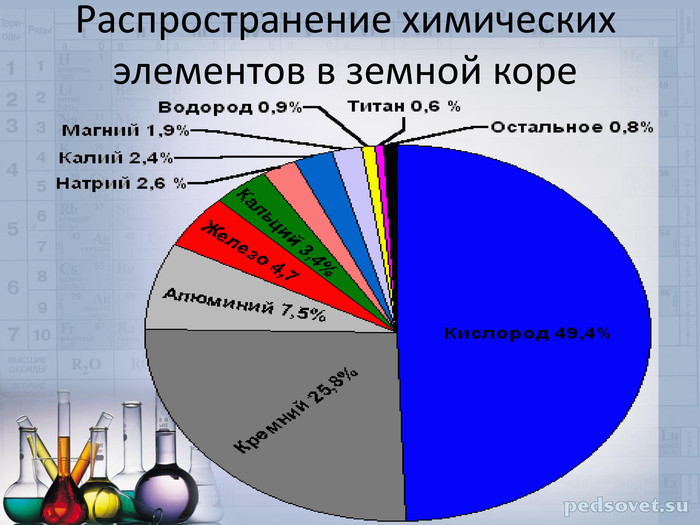
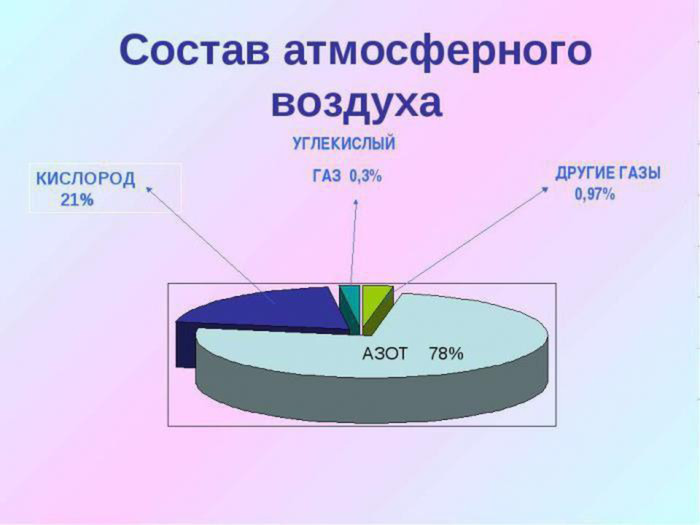
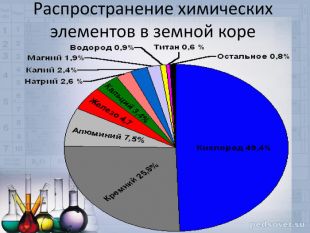
1. Оксиген – самый распространенный химический элемент в земной коре, на его долю приходится 49,4% всех атомов. Распространенность Оксигена в природе по массе: в атмосфере – 21%, в литосфере – 49%, в гидросфере – 89%, в живых организмах – 62%.
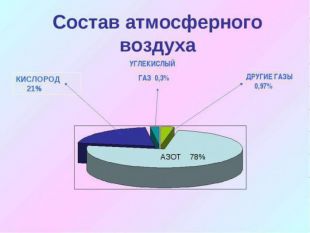
2. Кислород важный компонент воздуха, его массовая доля в нём составляет 21%
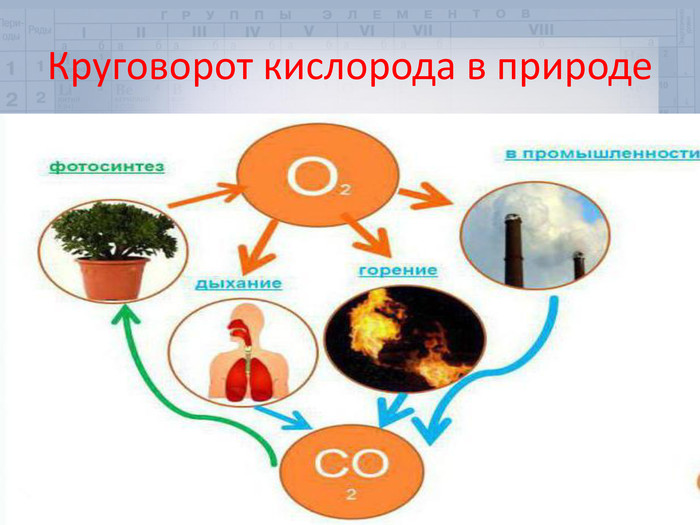
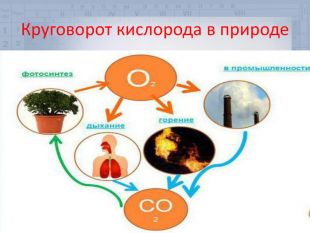
3. Впервые учение о круговороте элементов в природе разработал первый президент Украинской академии наук В.И. Вернадский.
Кислород – одно из самых важных веществ на Земле, обеспечивающее возможность существования жизни.
4. Почти все живые организмы используют кислород для дыхания, и только некоторые микроорганизмы могут без него обходиться. При окислении органических веществ выделяется большое количество энергии, которую организмы используют для своей жизнедеятельности.
5. При дыхании животных и растений выделяется углекислый газ и вода, то есть, атомы Оксигена, из молекул кислорода, переходят в состав этих веществ.
Большое количество кислорода тратится на гниение и горение различных веществ.
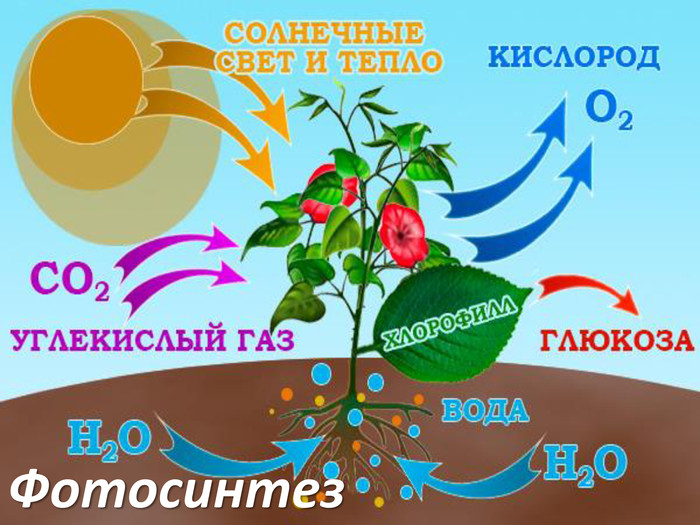
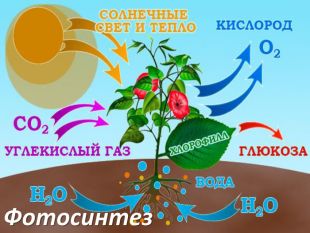
Главный поставщик кислорода на Земле - это растения. Они образуют и выделяют кислород в атмосферу в процессе фотосинтеза.
5 группа – «Технологи»
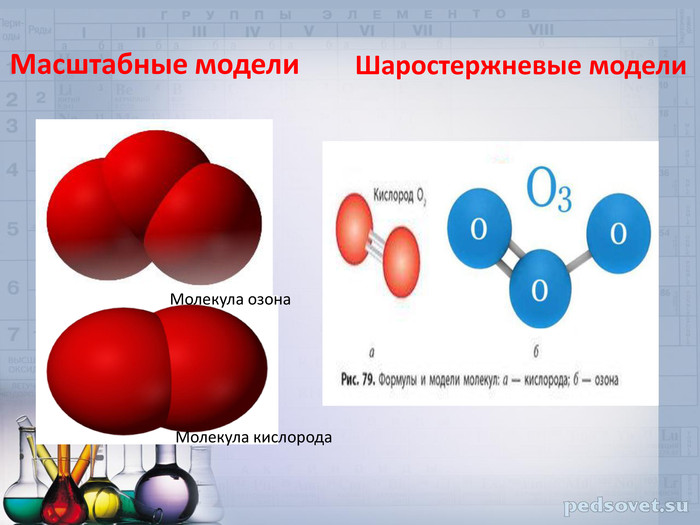
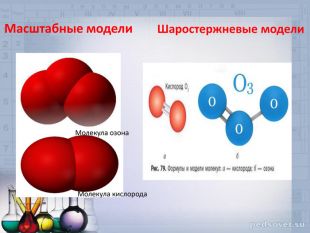
Задача этой группы: изготовление шаростержневых и масштабных моделей кислорода и озона. При изготовлении моделей, необходимо учитывать валентность Оксигена.
Инструктажная карта:
1. Выбери для работы необходимый цвет пластилина
2. Отрежь стеком необходимое количество пластилина
3. Согрей кусочек пластилина теплом своих рук, чтобы он стал мягким
4. Шар первый соедини с другим, при помощи 2 спичек – это шаростержневая модель кислорода, затем, 2 шарика соедини между собой без спичек – это масштабная модель.
5. 3 шара соедини между собой при помощи спичек – это шаростержневая модель озона, затем 3 шарика соедини между собой без спичек – это масштабная модель.
Оксиген имеет валентность 2, поэтому два шарика соединены двумя спичками в молекуле кислорода, а в молекуле озона связи полуторные, поэтому одну связь мы изобразили при помощи 2 спичек, а вторую – при помощи одной.
IV.Обобщение и систематизация знаний
Блиц-опрос.
1. Дополнить предложение, вставив слова Оксиген или кислород:
А)…самый распространенный на Земле элемент
Б)Рыбы дышат растворенным в воде…
В)…входит в состав белков, жиров, углеводов
Г)В результате фотосинтеза выделяется…
2. Какие утверждения, относительно кислорода, являются правильными:
А)жизненно важен для живых организмов
Б)входит в состав воздуха
В)молекула состоит из 3 атомов Оксигена
Г)имеет валентность ІІ
Д)кислород открыл Д.И. Менделеев
3. Укажите значение относительной молекулярной массы кислорода:
А)8 В)16
Б)32 Г)64
4. Укажите порядковый номер Оксигена в периодической системе:
А)6 В)8
Б)16 Г)32
5. Укажите правильные утверждения о физических свойствах кислорода:
А)хорошо растворяется в воде
Б)жидкий кислород имеет светло-голубой цвет
В)не смешивается с другими газами
Г)имеет парамагнитные свойства
6. Как называется процесс образования кислорода в природе:
А) брожение В) гниение
Б) фотосинтез Г) горение
7. Какой ученый считается первооткрывателем кислорода:
А) Лавуазье В) Менделеев
Б) Ломоносов Г) Пристли
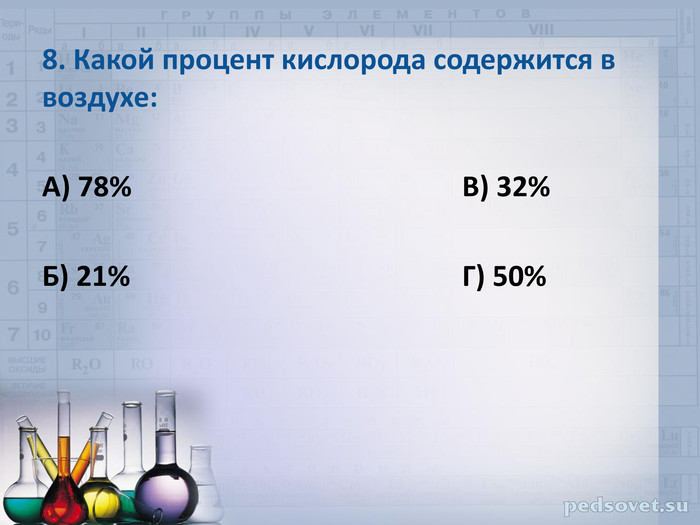
8. Какой процент кислорода содержится в воздухе:
А) 78% В) 32%
Б) 21% Г) 50%
V.Подведение итогов урока
VI.Домашнее задание
Выучить §15,21 С.114 №1,2-письменно,№3-6-устно
Приложение – презентация к уроку


про публікацію авторської розробки
Додати розробку