Презентація УРОКУ-8 "Струм в електролітах. Закони Фарадея"
Про матеріал
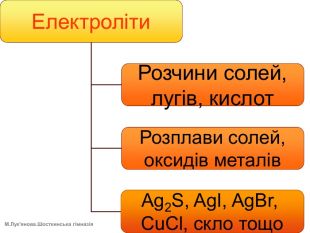
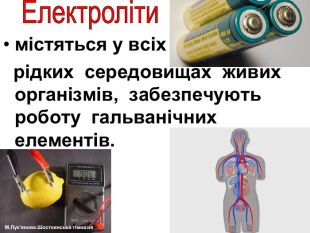
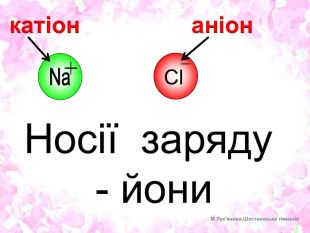
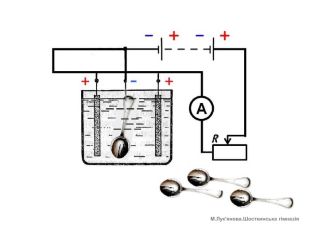
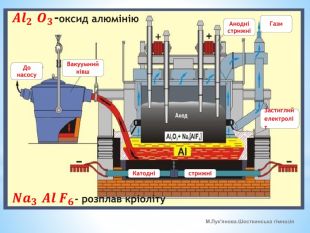
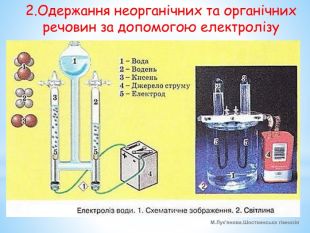
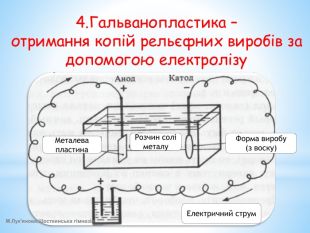
Презентація УРОКУ-8 в розділі "Електродинаміка. Постійний електричний струм" (Підручник - Фізика (рівень стандарту), 11 клас, Бар'яхтар В.Г. та ін.). Тема уроку - "Струм в електролітах. Закони Фарадея". Пояснено, що собою являє електричний струм в електролітах, що таке електроліз та де його застосовують, сформульовано два закони Фарадея. Перегляд файлу





























Зміст слайдів
Номер слайду 18
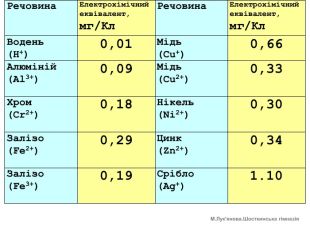
Речовина. Електрохімічний еквівалент, мг/Кл. Речовина. Електрохімічний еквівалент, мг/Кл. Водень (Н+)0,01 Мідь (Cu+)0,66 Алюміній (Аl3+)0,09 Мідь (Cu2+)0,33 Хром (Cr2+) 0,18 Нікель (Ni2+)0,30 Залізо (Fe2+) 0,29 Цинк (Zn2+)0,34 Залізо (Fe3+) 0,19 Срібло (Ag+)1.10 М. Лук'янова. Шосткинська гімназія
Номер слайду 20
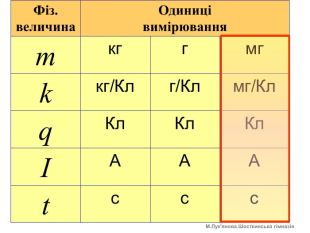
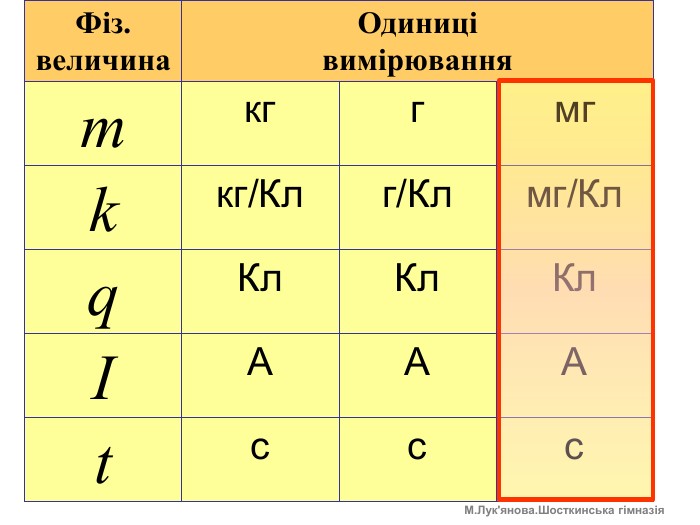
m- маса речовини, яка виділяється на електроді, кг ; k- електрохімічний еквівалент, кг/Кл; q- заряд (Кл), що пройшов за час t (с) при силі струму І (А); М- молярна маса речовини, що виділяється на електроді, кг/моль; n – валентність елемента в сполуці; F=𝑵𝑨∙𝒆=96500 Кл/моль - стала Фарадея. m=kqm=k. It. Перший закон Фарадея. Другий закон Фарадея. М. Лук'янова. Шосткинська гімназія
pptx
Додано
20 червня 2023
Переглядів
2888
Оцінка розробки
Відгуки відсутні


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку
Рекомендовані матеріали
Схожі матеріали