Презентація "Взаємодія води з оксидами"
Про матеріал
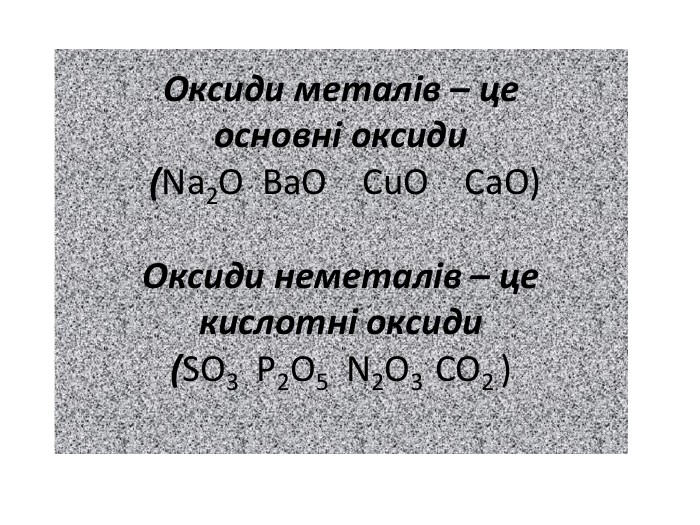
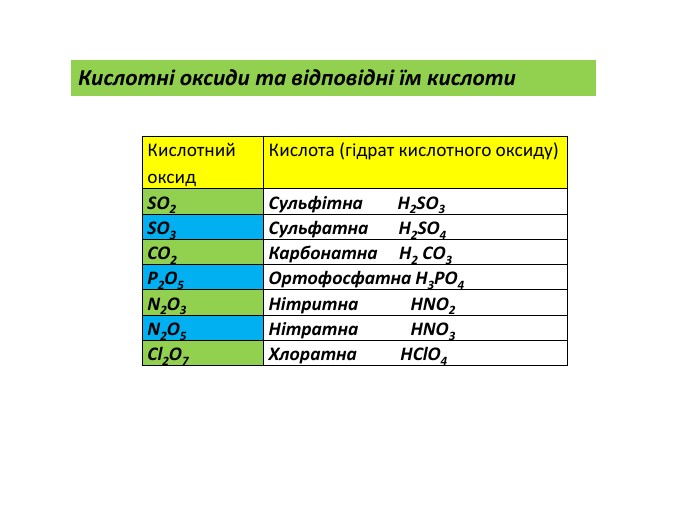
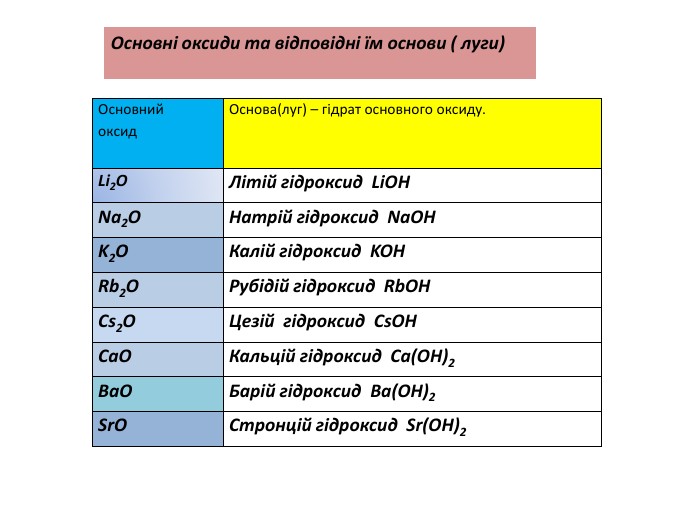
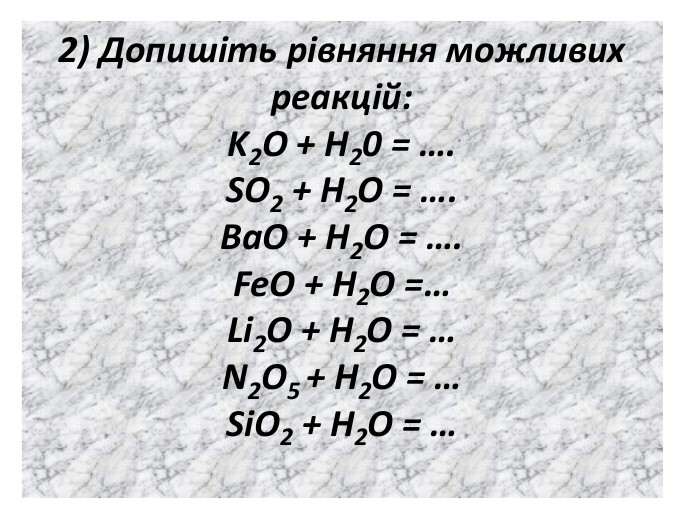
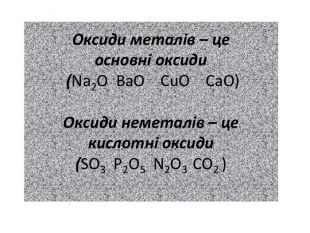
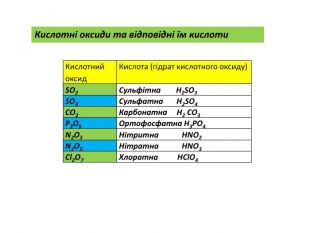
Презентація містить матеріал до уроку хімії в 7 класі "взаємодія води з оксидами". Призначена для вивчення теми вказаного уроку, містить пояснення нового матеріалу, повторення уже вивченого, відео дослідів. Також є завдання на виконання тренувальних вправ із даної теми. Особливо зручно використовувати презентацію під час дистанційного навчання. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую!
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку