Розв'язування експериментальних задач з хімії 2024
000
Розв'язування
експериментальних задач з xiMi'i
пас
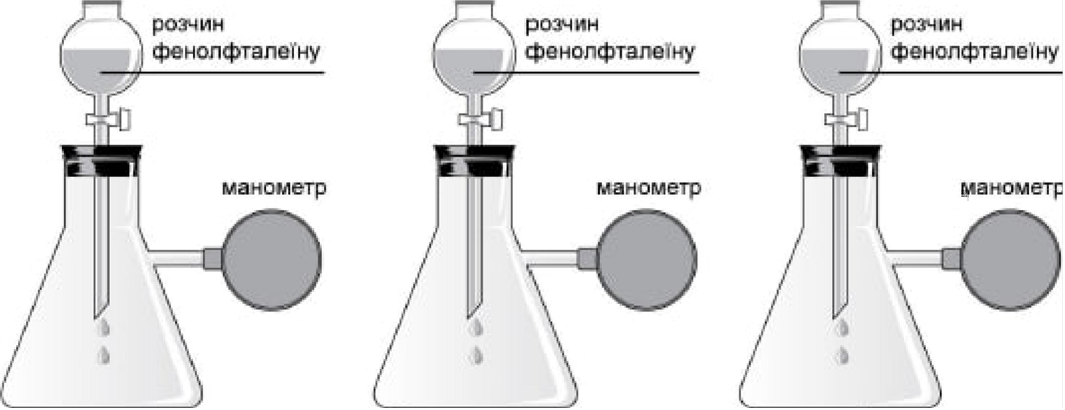
Е три ![]() прилади, колби яких
прилади, колби яких ![]() газами (див. рисунок).
газами (див. рисунок).
У ![]() схематично зображений на рисунку, можна
схематично зображений на рисунку, можна ![]() води й
води й
метац еЙ)роеен хлорщ) имонгсј,зг
Без порушення ![]() в кожну з колб додали крапель водно-спиртового розчину фенолфталетну.
в кожну з колб додали крапель водно-спиртового розчину фенолфталетну.
![]() твердження.
твердження.
1. У двох колбах ![]() зменшення тиску.
зменшення тиску.
ll. У двох колбах ![]() появу малинового забарвлення додано:
появу малинового забарвлення додано:![]()
Чи Е них![]()
Завдання скеровано на ![]() застосовувати знання про
застосовувати знання про ![]() хлориду, aM0Hial<Y, метану.
хлориду, aM0Hial<Y, метану.
Метан - малорозчинна у сполука, тому додавання крапель водно-спиртового розчину фенолфталеТну в колбу з метаном не вплине на тиск цього газу ![]() нет.
нет.
HaT0MicTb хлорид й амонЈак добре розчиняються у водЈ, тому додавання HaBiTb незначноТП ![]() зумовить зменшення
зумовить зменшення ![]() цих у колбах i приведе до зниження тиску в них.
цих у колбах i приведе до зниження тиску в них.
Середовище водного розчину aM0Hial<Y лужне, тому фенолфталеТн набуде в ньому малинового забарвлення.
Середовище водного розчину хлориду кисле, тому фенолфталеТн у ньому залишиться безбарвним.
Тому правильним наведених Е лише перше твердження.
![]() А. правильне лише I
А. правильне лише I
 У схематично зображений на рисунку, добули та деякого газу. У
У схематично зображений на рисунку, добули та деякого газу. У ![]() 1
1 ![]() розчин
розчин ![]() а в
а в

 Що
Що ![]() в посудинах 1 i 2?
в посудинах 1 i 2?
ТЕМА: ![]() речовини. 0cH0BHi класи
речовини. 0cH0BHi класи ![]() сполук. Кислоти.
сполук. Кислоти.![]()
Завдання скеровано на  прогнозувати
прогнозувати
![]() peal<LliT хлоридом i концентрованою сульфатною хлорид.
peal<LliT хлоридом i концентрованою сульфатною хлорид.
Водний розчин ![]() хлориду - сильна хлоридна кислота.
хлориду - сильна хлоридна кислота. ![]() хлоридноТ кислоти на
хлоридноТ кислоти на ![]() утворюеться осад
утворюеться осад ![]() кислоти (посудина 1 ).
кислоти (посудина 1 ).
![]() аргентум(1) HiTpaTY з хлоридною кислотою утворюеться осад аргентум(1) хлориду. (посудина 2).
аргентум(1) HiTpaTY з хлоридною кислотою утворюеться осад аргентум(1) хлориду. (посудина 2).
Умову завдання задовольняе BapiaHT ![]() В: в обох посудинах утворилися осади. YM0BHi позначення:
В: в обох посудинах утворилися осади. YM0BHi позначення:
![]() » — уТ ВореННЯ осаду;
» — уТ ВореННЯ осаду; ![]() » -
» - ![]() газу.
газу.
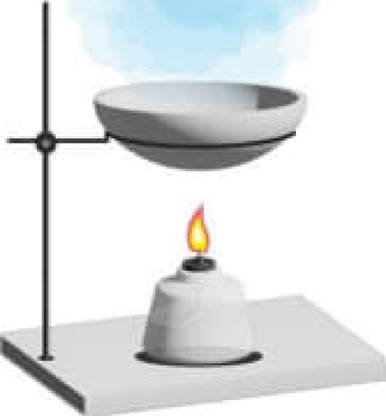
Безбарвну прозору ![]() Х деякий час випарювали (див. рисунок). Твердий залишок
Х деякий час випарювали (див. рисунок). Твердий залишок ![]() випарювання - калЈй хлорид. РЈдина Х -
випарювання - калЈй хлорид. РЈдина Х -
ТЕМА: Речовина. речовин. Види ![]()
![]()

 розчини -
розчини -![]()
За результатами рисунка й наведених BapiaHTiB ![]() можна
можна ![]() висновку, що зображено випарювання водного розчину хлориду.
висновку, що зображено випарювання водного розчину хлориду. ![]() такого розчину у
такого розчину у ![]() за допомогою спиртового пальника вода випаровуеться, а хлорид
за допомогою спиртового пальника вода випаровуеться, а хлорид![]()
Водний розчин хлориду Е ![]() це система частинок двох речовин - води i хлориду.
це система частинок двох речовин - води i хлориду.
води, l<aTi0HiB i ![]() не перевищують 10-1 см.
не перевищують 10-1 см.
![]() розчин
розчин
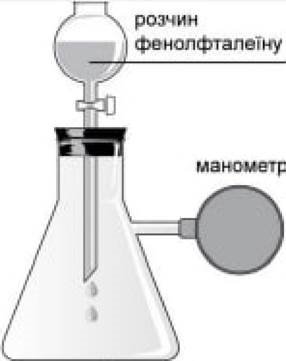
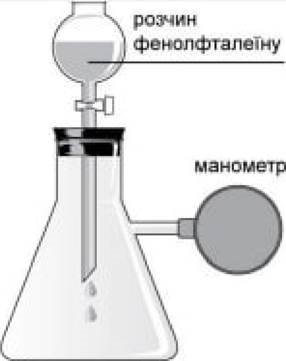
Е два ![]() прилади, колби яких
прилади, колби яких ![]() газами (див. рисунок).
газами (див. рисунок).
 Без порушення
Без порушення ![]() в кожну з колб додали
в кожну з колб додали ![]() крапель водно-спиртового розчину фенолфталетну.
крапель водно-спиртового розчину фенолфталетну. ![]() твердження.
твердження.
1. В обох колбах зменшення тиску. II. В обох колбах появу малинового забарвлення доданоТ
 гЈДроген хлорид п.нонгон• Чи Е них
гЈДроген хлорид п.нонгон• Чи Е них
ТЕМА: Метали й неметали. ![]() про
про ![]() елементи й неметали.
елементи й неметали.
Завдання скеровано на ![]() знання
знання ![]() i властивостей aM0Hial<Y й хлориду.
i властивостей aM0Hial<Y й хлориду.
![]() хлорид й aM0Hial< добре розчиняються у тому додавання HaBiTb незначноТ П
хлорид й aM0Hial< добре розчиняються у тому додавання HaBiTb незначноТ П ![]() зумовить зменшення
зумовить зменшення ![]() цих у колбах i приведе до зниження тиску в них.
цих у колбах i приведе до зниження тиску в них.
Середовище водного розчину aM0Hial<Y лужне, тому фенолфталеТн набуде в ньому малинового забарвлення.
Середовище водного розчину хлориду кисле, тому фенолфталетн у ньому залишиться безбарвним.
Тож правильним наведених Е лише перше твердження.
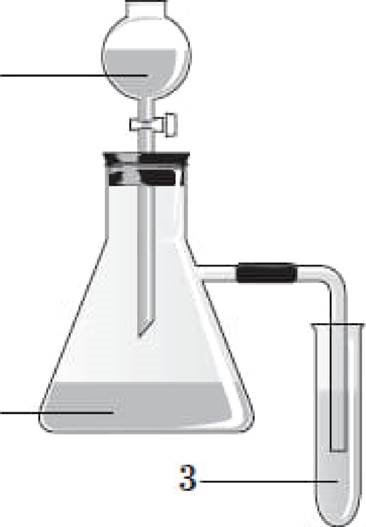
У схематично зображений на рисунку, одночасно ![]() фенолу, карбонатноћ' та хлоридноТ кислот. Довели, що
фенолу, карбонатноћ' та хлоридноТ кислот. Довели, що ![]() кислотою
кислотою ![]() них Е хлоридна, а
них Е хлоридна, а ![]() ВИЯВЛЯЕ фенол.
ВИЯВЛЯЕ фенол.
![]() речовин А - Г, формули яких наведено, у використали розчини лише трьох i3 них.
речовин А - Г, формули яких наведено, у використали розчини лише трьох i3 них. ![]() формулу Ti€i речовини, водний розчин якот позначено на рисунку цифрою З.
формулу Ti€i речовини, водний розчин якот позначено на рисунку цифрою З.
ТЕМА: ![]() Фенол.
Фенол.

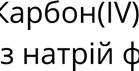 1 Завдання скеровано на
1 Завдання скеровано на ![]() фенолу, карбонатноТ та хлоридноТ кислот.
фенолу, карбонатноТ та хлоридноТ кислот.
взяти до уваги, що хлоридна кислота (1 ) ![]() за карбонатну, тому П з карбонату, водний розчин якого на рисунку позначено цифрою 2. оксид продукт
за карбонатну, тому П з карбонату, водний розчин якого на рисунку позначено цифрою 2. оксид продукт ![]() карбонату з хлоридною кислотою - фенол з феноляту (З), що доводить: фенол Е слабшою кислотою
карбонату з хлоридною кислотою - фенол з феноляту (З), що доводить: фенол Е слабшою кислотою ![]() з карбонатною.
з карбонатною.
2Ключовим в YMOBi завдання Е слово одночасно, тобто за допомогою одного в тому самому ![]() силу трьох кислот.
силу трьох кислот.
![]() C6H50Na
C6H50Na
![]() тверд»кення щодо схематично зображеного на рисунку способу
тверд»кення щодо схематично зображеного на рисунку способу![]()
![]()
I. Утакий можна ![]() води й бензену.
води й бензену.
II. цей ![]() фунтуеться на
фунтуеться на ![]() cyMil.ui.
cyMil.ui.
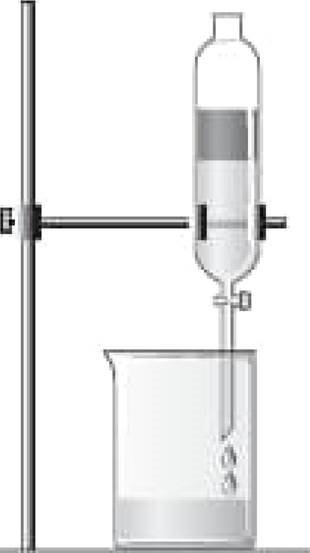 Чи Е них
Чи Е них![]()
На рисунку схематично зображено ![]() двох i3
двох i3 ![]() густиною за допомогою
густиною за допомогою ![]() Густина бензену менша за густину води, тому в
Густина бензену менша за густину води, тому в ![]() пЈсля розшаровування цих шар бензену буде зверху, а води знизу. його можна видалити, вџдкривши кран
пЈсля розшаровування цих шар бензену буде зверху, а води знизу. його можна видалити, вџдкривши кран ![]()
![]() обидва
обидва![]()
Яку газувату речовину добувають i збирають так, як схематично показано на рисунку?
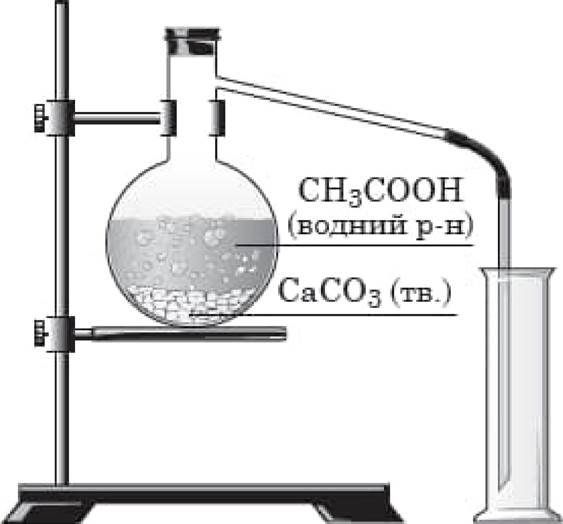 ТЕМА: Неорган1чн\ речовини i 'l*Hi
ТЕМА: Неорган1чн\ речовини i 'l*Hi ![]() kap60H(lV) оксид.
kap60H(lV) оксид.
Зовдання скеровоно на перевћрку врл(ння застосовувати зноння про xiMiHHi ![]()
![]() основних oociB неорганћнних сполук способи Тхнього добувоння.
основних oociB неорганћнних сполук способи Тхнього добувоння.
Дђею етановоТ (оцтово•ђ кислоги но КОЛЬЦЈЙ карбонат добувоють ![]() оксид
оксид
(вуглекислий газ):
СаСО3 + 2СНзсоон (СН3СОО)2Са + C02 +1120.
Густино kop60H{lV) оксиду 6iA6LLQ за густину пов1тря, тому його збироють у посудину, розташовану отвором догори.
![]() А.
А. ![]() оксид
оксид
![]() Проаналћзуйте наведену схему гальванјчного елемента.
Проаналћзуйте наведену схему гальванјчного елемента.
Гальванометр
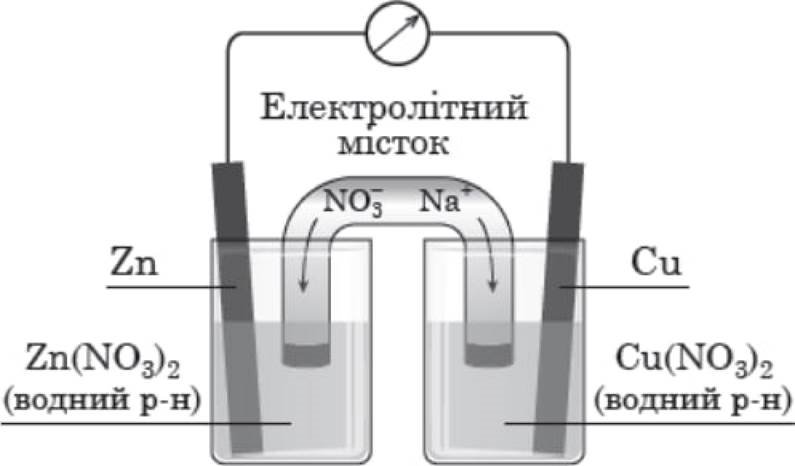
Укажћть ПОМИЛКОВЕ твердження щодо його роботи.![]()
![]() Но цинковому електродћ Zn2+
Но цинковому електродћ Zn2+![]()
![]() Но м1дному електродћ катЈони cu 2+ вћдновлюються.
Но м1дному електродћ катЈони cu 2+ вћдновлюються. ![]() в Мосо цинкового електрода поступодо зменшуеться.
в Мосо цинкового електрода поступодо зменшуеться.
г Мосо м1дного електродо поступово збЈльшуеться.
Коментар
ТЕМА: ![]() елемент.
елемент.
Зовдання скеровано но перевћрку ![]() принципу роботи гальванћнного елемента.
принципу роботи гальванћнного елемента.
![]() елемент — хћмћнне джерело електричного струму (енергћя xiMiHH0T реакцй• перетворюеться в електричну енергЈю).
елемент — хћмћнне джерело електричного струму (енергћя xiMiHH0T реакцй• перетворюеться в електричну енергЈю).
![]() як процюе гальзонђчний елемент. схему якого наведено в завданн(. Електроди
як процюе гальзонђчний елемент. схему якого наведено в завданн(. Електроди
(зоря»кенћ стержн1) зиготовленђ з метал:в цинку й MLi, занурен( в рознини тхнћх солей i ![]() електролћтним -мћстком. Електроди 3' гольванометром. цинк
електролћтним -мћстком. Електроди 3' гольванометром. цинк ![]() зо
зо ![]() тому е онодом, о м(дь — котодом. Анод окиснюеться: Zn — 2е —У Zn2+, його масо зменшуеться. У прикатодному
тому е онодом, о м(дь — котодом. Анод окиснюеться: Zn — 2е —У Zn2+, його масо зменшуеться. У прикатодному ![]() Си2+ 13 рознину
Си2+ 13 рознину ![]() нђтроту втдновлюються: Си2+ -l- 26 —h Си , ЛАОСО катода зольшуеться. ОТ>Ке. помилкове твердження лише А.
нђтроту втдновлюються: Си2+ -l- 26 —h Си , ЛАОСО катода зольшуеться. ОТ>Ке. помилкове твердження лише А.
![]() А.
А.
У схематично зображений на рисунку, можна ![]() води й - соняшниковот
води й - соняшниковот![]()
|
|
|
||||||||||||||||
|
|
|
||||||||||||||||
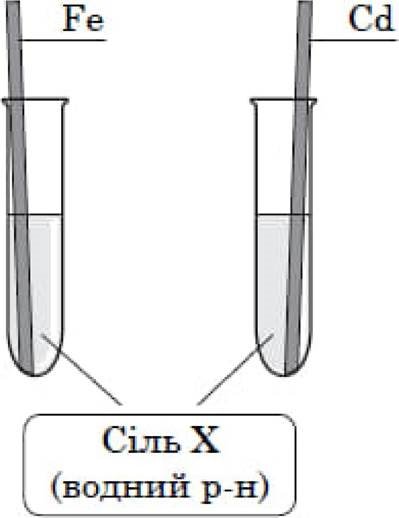
У водний розчин Х занурили пластинки, ![]() з i (див. рисунок). Згодом пластинки вийняли, висушили й зважили. Маса
з i (див. рисунок). Згодом пластинки вийняли, висушили й зважили. Маса ![]() пластинки
пластинки ![]() а
а ![]() зменшилася.
зменшилася.
![]() формулу Х.
формулу Х.
![]()
У схематично зображений на рисунку, одночасно ![]() фенолу, карбонатнот та хлоридноТ кислот. довели, що
фенолу, карбонатнот та хлоридноТ кислот. довели, що ![]() кислотою
кислотою ![]() них Е хлоридна, а
них Е хлоридна, а ![]() ВИЯВЛЯЕ фенол.
ВИЯВЛЯЕ фенол.
З-помЈж речовин А - Г, формули яких наведено, у використали воднЈ розчини лише трьох i3 них. Yka>kiTb формулу Ti€i речовини, водний розчин якот позначено на рисунку цифрою
З.
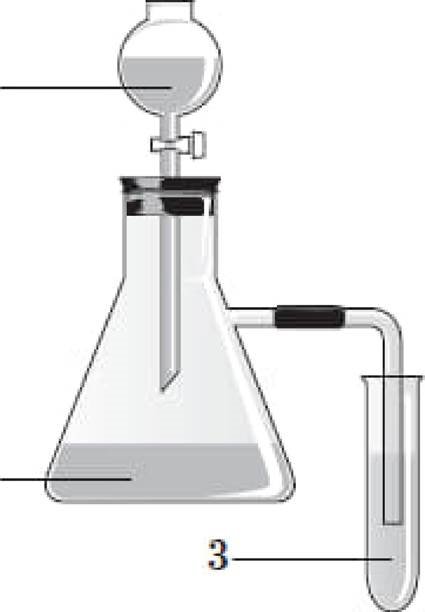 1
1
2
C6H50Na
 твердження щодо схематично зображеного на рисунку способу роздЈлення
твердження щодо схематично зображеного на рисунку способу роздЈлення
l. У такий можна ![]() води й бензену.
води й бензену.
ll. Цей ![]() фунтуеться на
фунтуеться на![]()
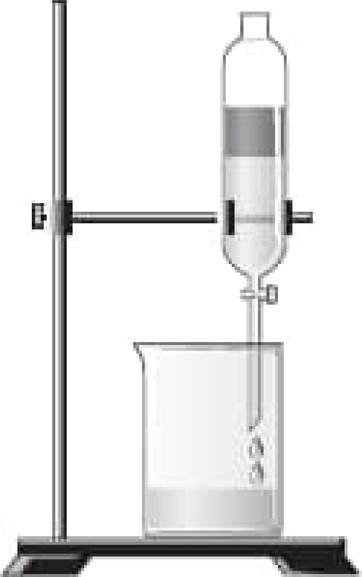 Чи Е них
Чи Е них![]()
обидва
У посудинах 1-4 окремо метилися р1дкий крохмольний клейстер 1 водн1 розчини бђлка курячого яйця, глюкози, ![]() до тхн1х ПОРЦ1Й,
до тхн1х ПОРЦ1Й, ![]() добавили водно-спиртовий розчин йоду. Появу синього кольору спостер1гали лише в досл1дЈ з пробою, в1дЈброною з посудини 1 . до нових порц1Й 13 посудин 2-4 добавили етанол. Ылий осад утворився лише в досл1дђ з пробою, узятою з посудини 2. Пот1м 13
добавили водно-спиртовий розчин йоду. Появу синього кольору спостер1гали лише в досл1дЈ з пробою, в1дЈброною з посудини 1 . до нових порц1Й 13 посудин 2-4 добавили етанол. Ылий осад утворився лише в досл1дђ з пробою, узятою з посудини 2. Пот1м 13 ![]() посудин З й 4 д пробђрки вђдћбрали наступн1 ПОРЦЙ'. На них подтяли свЪкоосодженим за надлишку лугу
посудин З й 4 д пробђрки вђдћбрали наступн1 ПОРЦЙ'. На них подтяли свЪкоосодженим за надлишку лугу ![]() унаслћдок чого утворилися прозор1 розчини темно-синього кольору. ПД чос нагр1воння цих розчин1в спостерћголи утворення червоного осаду лише в пробђрц1, у яку було вјдћбрано пробу з посудини 4.
унаслћдок чого утворилися прозор1 розчини темно-синього кольору. ПД чос нагр1воння цих розчин1в спостерћголи утворення червоного осаду лише в пробђрц1, у яку було вјдћбрано пробу з посудини 4.
У якому рядку таблицђ записано правильний висновок, зроблений за результатами
![]()
|
|
|
Посудини |
|
|
|
1 |
2 |
з |
4 |
|
|
|
крохмальний клейстер |
6iA0k |
глюкозо |
глћцерол |
|
|
бћлок |
гл1церол |
крохмальний клейстер |
глюкоза |
|
в |
бћлок |
крохмольний клейстер |
глюкозо |
глћцерол |
|
|
крохмольний клейстер |
|
гл1церол |
глюкоза |
|
|
||||
|
|
||||
1. ![]()
 Ксантопротегнова на 6i«Flk'u.
Ксантопротегнова на 6i«Flk'u.
![]() з конц.
з конц.![]()
кислотою, яка супроводжу€ться появою жовтого забарвлення.
2. Бђретова ![]() на розчину NaOH з
на розчину NaOH з
CuS04 - забарвлення розчину
![]() на
на![]()
![]() двома газуватими речовинами синтезують один газуватий продукт. Ця
двома газуватими речовинами синтезують один газуватий продукт. Ця![]()
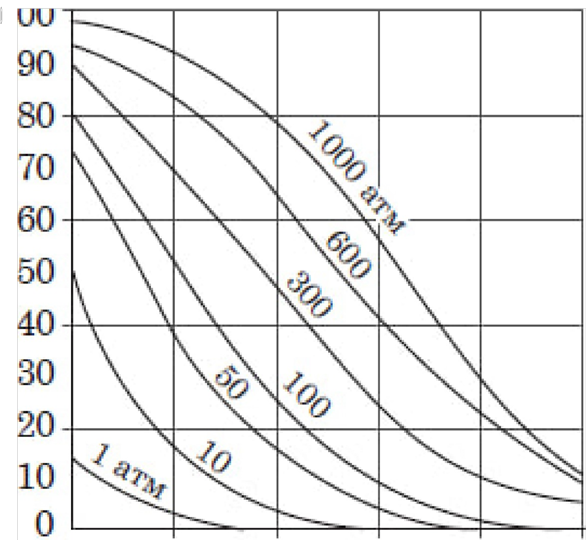
 Е оборотною. Тт проводили в закритому peakTopi, узявши реагенти в обкмному
Е оборотною. Тт проводили в закритому peakTopi, узявши реагенти в обкмному ![]() що
що ![]() у
у ![]() об'ЕмноТ частки (%) продукту реакцй' в температури за значень тиску (див. рисунок) i Bka>kiTb правильне твердження.
об'ЕмноТ частки (%) продукту реакцй' в температури за значень тиску (див. рисунок) i Bka>kiTb правильне твердження.
|
Реагенти
Продукти |
||
|
|
|
Продукти
Реагенти |
![]()
![]()
![]() Н Н
Н Н
![]() реакцй'
реакцй'
а) ![]() б)
б) ![]()
200 зоо 400 500 600 700
Температура. ос
![]() синтезу газуватого продукту
синтезу газуватого продукту![]()
3i зменшенням об'ему, Е![]()
Формули солей, для k0>kH6f з яких правильно зозночено середовище П розбавленого
водного розчичу, наведено в рядку
|
|
Середовище водного розчину |
||
|
кисле |
нейтральне |
лужне |
|
|
А |
H4Cl |
N02C03 |
Noa |
|
Б |
N02C03 |
NH4Cl |
Ноа |
|
в |
NH4Cl |
Ноа |
|
|
г |
N02C03 |
Ноа |
NH4Cl |
Правильно в1дповћдь:

![]() Результати
Результати
кислот i розчинами властивостями П kaTi0Ha i aHi0Ha, е в П водному
Укажјть назву газу, який збирають у спосЈб, схематично зображений на рисунку.
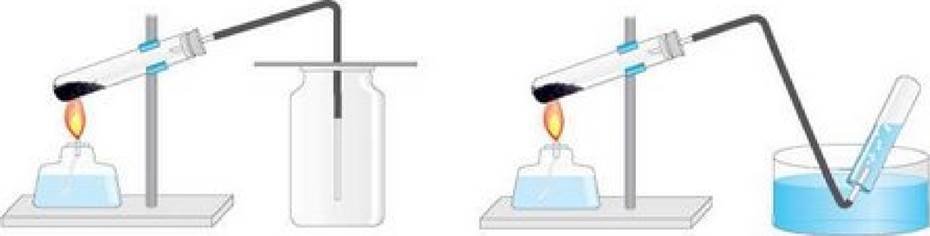
ноо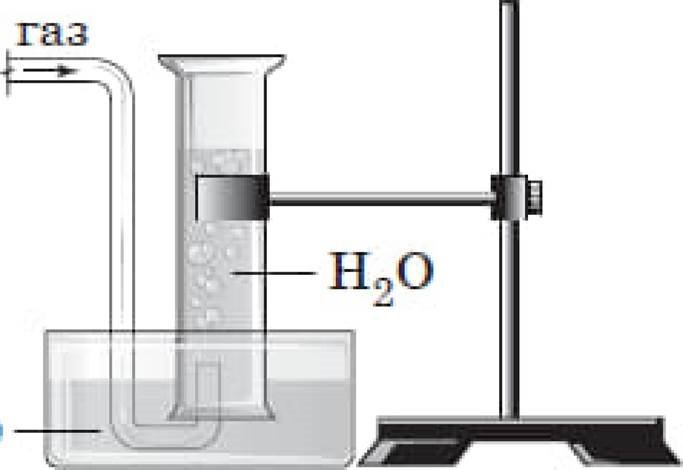 Мал. 94. Пристраг для эбирдннн кисню: а методом зит@нення лов[тря; б методом витћснення води
Мал. 94. Пристраг для эбирдннн кисню: а методом зит@нення лов[тря; б методом витћснення води
кисень
![]() HiTpaTiB i у залежить температури (див. рисунок).
HiTpaTiB i у залежить температури (див. рисунок).
![]()
![]() твердження, використавши
твердження, використавши![]()
NaN03 ![]() за
за
RbN03
правильне лише I о 20 40 60 80 100  Температура, ос
Температура, ос
Потр1бно визначити, у 13 трьох пронумерованих пробђрок м1ститься водний розчин ма нЈй хлориду, у якћй — цинк хлориду, о в .якћй хлориду. У кожну проб1рку добавляли кроплями водний розчин калћй гђдроксиду. У пробђрках 1 З утворився осад, а в пробћрцћ 2 змђн не було. до occuiB у ![]() 1 З добавили надлишок розчину
1 З добавили надлишок розчину ![]() лугу.
лугу. ![]() швидке розчинення осаду в проб1рц1 З. У
швидке розчинення осаду в проб1рц1 З. У ![]() 1 осад не розчинився.
1 осад не розчинився.
У якому рядку таблиц1 записано провильний висновок, зроблений за результатами дослђд1в?
|
|
|
||
|
|
2 |
з |
|
|
|
|
NaCl |
,zrc12 |
|
Б |
7ЛСК |
мдск |
NaCl |
|
В |
MgC12 |
znCl2 |
Naa |
|
|
|
!NaCl |
мдск |
Правильна вћдповћдь:
АБВГ

Речовина Х реагуе 3i ![]() за надлишку лугу купрум(")
за надлишку лугу купрум(") ![]() чого утворюеться прозорий розчин темно-синього кольору. Також речовина Х вступае в
чого утворюеться прозорий розчин темно-синього кольору. Також речовина Х вступае в ![]() дзеркала» з
дзеркала» з ![]() розчином аргентум(1) оксиду за
розчином аргентум(1) оксиду за ![]()
![]() формулу речовини Х.
формулу речовини Х.
![]()
![]() Глюкоза як багатоатомний спирт реагуе 3i за надлишку лугу купрум(11) утворюеться прозорий розчин темно-синього кольору. Також глюкоза за
Глюкоза як багатоатомний спирт реагуе 3i за надлишку лугу купрум(11) утворюеться прозорий розчин темно-синього кольору. Також глюкоза за ![]() групою вступае в
групою вступае в ![]() «cpi6Horo дзеркала» з
«cpi6Horo дзеркала» з ![]() розчином аргентум(!) оксиду за
розчином аргентум(!) оксиду за
сњон
У ![]() наведено cTpykTypHi формули двох
наведено cTpykTypHi формули двох ![]() й утвореного ними трипептиду.
й утвореного ними трипептиду. ![]() у цьому трипептид1
у цьому трипептид1
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
||||||||||||||||||||
![]()
У водний розчин co.Ti Х занурили пластинку, виготовлену з металу У. Згодом на П.лаСТННЦ1 ociB шар металу, ыдновленого металом У. Визначте формули Х та металу У.
|
|
|
|
|
|
|
Васк |
|
|
|
|
мдсц |
|
|
|
в |
.znS04 |
|
|
|
|
|
cuS04 |
|
Проаналзуйте наведен1 в тао.лищ дам щодо те,мператур плав.лення та кипжня a.TkaHiB I—IV за тиску 10 Па. Який з a.uaHiB за такого тиску й температури 25 перебуватиме у твердому cTaHi?
|
|
Алкан |
Температпа .ня, О С |
Температура плавлення |
|
|
|
|
-13S |
|
Б |
п |
69 |
|
|
в |
ш |
287 |
|
|
|
|
343 |
37 |
![]() B116epiTb пару структурних i30MepiB.
B116epiTb пару структурних i30MepiB.
|
1 |
сн=сн снз |
2 |
снз снз |
сн—сн |
4 |
СН¯ СН |
BapiaHTH Bgr10Bij:
|
Б |
1.4 |
1зомери — це сполуки з однаковою |
|
в |
|
молекулярною формулою, але |
формулами. Число можливих i30MepiB ![]() велике, що доводиться вЈдзначати структурнЈ або
велике, що доводиться вЈдзначати структурнЈ або ![]() формули
формули ![]() сполук,
сполук,
![]()
Укаяать ПОХШ„ЖОВЕ твердж•ення щодо речовпни, структурна формула якот
снз
|
А |
Молекула речовинп пдроксильну трупу. |
|
|
Б |
Речовина належить до ароматичних сполук. |
он |
в Молекулярна формула речовини C7HsO.
Г Речовина е гомологом бензену.
Бен зён — перший представник ![]() ряду ароматичних
ряду ароматичних ![]() молекулярна формула СбН6.
молекулярна формула СбН6.
![]() Бен зён — перший представник
Бен зён — перший представник ![]() ряду ароматичних
ряду ароматичних ![]() молекулярна формула СбН6. Безбарвна летка з характерним запахом.
молекулярна формула СбН6. Безбарвна летка з характерним запахом.
Бензол
Нафтален — летка з характернпм запахом кристалчна речомжа.
ћ температура плавленњя близько SO •С. Укажтъ тип ![]() фаток нафталену.
фаток нафталену.
йонними називають фаткки, у вузлах яких знаходяться йони.
А молекулярн ![]() називають фатки, складаються з позитивних aT0MiB металу i вЈльних електронЈв.
називають фатки, складаються з позитивних aT0MiB металу i вЈльних електронЈв.
Б метал:чн:
Атомними називають фатки, у вузлах яких знаходяться 01<peMi
![]() В атомы атоми, ковалентними зв%зками.
В атомы атоми, ковалентними зв%зками.
Г йоню
![]() Молекулярними називають фатки, у вузлах яких знаходяться молекули,
Молекулярними називають фатки, у вузлах яких знаходяться молекули, ![]() слабкою
слабкою 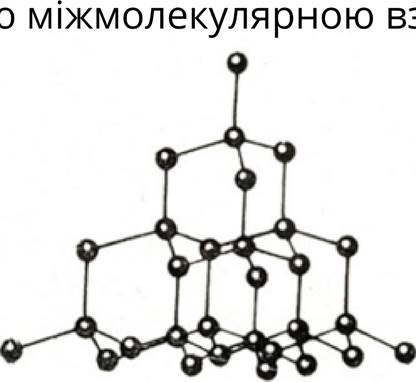 взаЕМОДКЮ.
взаЕМОДКЮ.
У кристалзатор з Водою помстили шматочок кальщю. Унаслцок цього ![]() бурхлнва
бурхлнва ![]() одним з продукт{Б була газувата займиста речовинаг закжчення peak14ii Б MicTLTacz каламутна рцина.
одним з продукт{Б була газувата займиста речовинаг закжчення peak14ii Б MicTLTacz каламутна рцина.
![]() тверд:кенна щодо peaki!ii, 'fi реагенпв i
тверд:кенна щодо peaki!ii, 'fi реагенпв i ![]() зовн1шн1х
зовн1шн1х ![]() ефектљ.
ефектљ.
![]() РеактЙя е екзотерзйчною.
РеактЙя е екзотерзйчною.
П. Газ, що БИДIЛИВСЛ внас.тщок реакцй, — кисень. ![]() Ш. Атоми
Ш. Атоми ![]() прнйня.ти електрони й
прнйня.ти електрони й![]()
IV. Попа каламуп зумовлена упореннл.м малорозчинноз• основи„
![]() Правильн1 з-пом:ж них лише
Правильн1 з-пом:ж них лише
в![]()
![]() г III, IV
г III, IV
![]()
насичений розчин — це розчин, у якому за певноТ температури дана речовина не розчиняеться; ненасичений розчин — це розчин, у якому за певноТ температури дана речовина ще може розчинятися; пересичений розчин — це розчин, у якому концентрацЈя розчиненоТ речовини бЈльша, ![]() у насичених.
у насичених.
Для проведення взяли тверду речовину Х та рџину У. У pe3YTbTaTi реакцй добули газ, B,TacTIIBocTi лкого достдили так, лк показано на рисунку. час ![]() змжу кольору внасмдок упорення свинцю з плюмбум (П) оксиду.
змжу кольору внасмдок упорення свинцю з плюмбум (П) оксиду.
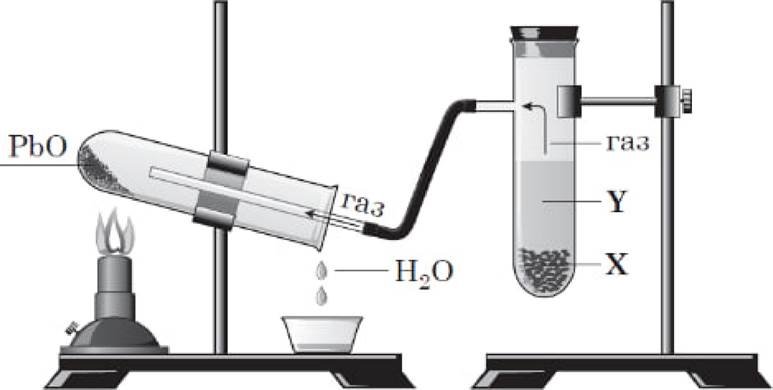
Тверда речовина Х та рџина У — це![]()
А манган(IV) оксид i розчин ![]() пероксиду
пероксиду
Б кальщй карбонат i хлоридна кислота
В цинк 1 хлоридна кислота
![]() Г кальцдй оксид 1 вода
Г кальцдй оксид 1 вода
У водний розчин Х занурили каддйеву пластинку. Згодом пластинку вийняли. висуши„ли й зважили. Маса пластинки 301льшиласл. Укажлть формулу co.Ti Х.![]()
А Ваф4Оз)2
![]()
![]()
![]()
![]() Потр{оно внзначити, у тай з трьох пронумероважх
Потр{оно внзначити, у тай з трьох пронумероважх ![]() :кпститься водний розчшт глюкозн, у ямй — етаналю, а Б лмй — гмцеролу. У ко•жну
:кпститься водний розчшт глюкозн, у ямй — етаналю, а Б лмй — гмцеролу. У ко•жну ![]() добавили СБIЖООСаДЖЕНИЙ за надлшж-у лугу купрум(П) пдроксид i ретелъно
добавили СБIЖООСаДЖЕНИЙ за надлшж-у лугу купрум(П) пдроксид i ретелъно ![]() реагенти. У проб1рках 1 i З утворпвсл прозорий розчин темно•сннъого колюру, а в 2 купрум(П) не розчинився. Унаслдок
реагенти. У проб1рках 1 i З утворпвсл прозорий розчин темно•сннъого колюру, а в 2 купрум(П) не розчинився. Унаслдок ![]() BMiCTY 2 i З утворення осаду жовтого кольору й поступову з.м:ну його забарвлення на червонег
BMiCTY 2 i З утворення осаду жовтого кольору й поступову з.м:ну його забарвлення на червонег
|
|
|
|
|
|
|
2 |
|
|
|
|
глщерол |
етаналь |
глюкоза |
|
Б |
глщерол |
глюкоза |
етаналь |
|
в |
глюкоза |
етана.ть |
глщерол |
|
|
етаналь |
глщерол |
глюкоза |
![]()
![]()
![]()
![]() У якому рядку записано правильний висновок, зроблений за результатами досм;џв?
У якому рядку записано правильний висновок, зроблений за результатами досм;џв?
cuso„ сирв},
На рисунку зображено залежност{ ![]() HirpaTiB i
HirpaTiB i ![]() у Ei;; температури.
у Ei;; температури.
![]() Проаналзуйте твердж•ення, використавши
Проаналзуйте твердж•ення, використавши
![]() У фарфоровий тигель похпстили к[лька -шматочкчв
У фарфоровий тигель похпстили к[лька -шматочкчв ![]() кароонату та про;карили. Унас,тдок цього утвориласл перда речовина Х i -видплився газ. Речовину Х перенесли в порцелянову чашку й добавили невелики.ми
кароонату та про;карили. Унас,тдок цього утвориласл перда речовина Х i -видплився газ. Речовину Х перенесли в порцелянову чашку й добавили невелики.ми ![]() воду У результат{ цього
воду У результат{ цього ![]() бурхлива
бурхлива ![]() з утвореннк,м речовини У. YkakiTb формули речовин Х та У.
з утвореннк,м речовини У. YkakiTb формули речовин Х та У.![]()
|
|
|
250
200
150
-100
'20 40 60 80 100
Температура, ос
I. За температури 40 'С ![]() натрлй ютрату за розчинжсть калй ютрату. II. За температури 80 'С розчинмсть натр1й ютрату менша за
натрлй ютрату за розчинжсть калй ютрату. II. За температури 80 'С розчинмсть натр1й ютрату менша за ![]() калй н:трату.
калй н:трату.
Чи е ПОМЕК них![]()
А правильне лише I
Б правильне лише II
обидва![]()
Г немае правилъних
![]() Для потЯвнлннл akNBHocTi трьох умовно позначених
Для потЯвнлннл akNBHocTi трьох умовно позначених ![]() Х, У i Щ провели дослдкення див. рисунок). Результати показали, що активюстъ цих 2€:era.T1iB зростае Б ряду Х, У, Z.
Х, У i Щ провели дослдкення див. рисунок). Результати показали, що активюстъ цих 2€:era.T1iB зростае Б ряду Х, У, Z.
![]() Проаналзуйте тверджтення
Проаналзуйте тверджтення 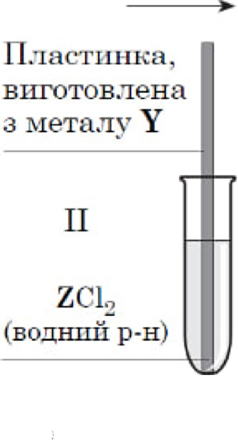
Z найсильн1шим окисжжом е kaTi0H Х2+ ![]() .II. час досмд:кення .ЛИШе в III в)цбулася реакци.
.II. час досмд:кення .ЛИШе в III в)цбулася реакци.
Чи е пом:ж них правильж.
А правильне лише I
Б правильне лише П
![]() В ооидва прави.льж
В ооидва прави.льж
![]() Г немае прави.льних
Г немае прави.льних
![]() TEMA: ,3araAbHi BiAOMOCTi npo MeTaAiHHi e,sxemeHTM 'Ta MeTaAh. XiMiHHi BAaCT%BOCTi MeTCIAiB. PHA aKTMBHOCTi MeTaAiB.
TEMA: ,3araAbHi BiAOMOCTi npo MeTaAiHHi e,sxemeHTM 'Ta MeTaAh. XiMiHHi BAaCT%BOCTi MeTCIAiB. PHA aKTMBHOCTi MeTaAiB.
.3aBACIHHfi nepeaiph€ 3CICTOCYBC%-lHh 3HaHb npo .XiMiHHi BACICW180CTi meTClAi8 i ClKTVIBHOCTi Merani8 y KOHKPeTHih AOCAiAHHUbKih 3CIAa Lli.
A/S pc-na!naHHfi ,3aaaHi Kpaue B3hTkl eAemeHTkl, fiKi aiAn0BiAa0Tb ,AiTepaM y 3CJBACIHHi 4-—2--2-— 3
Mg, .znt Fe
ypaxyeaHHfiM aKTMBHOCTi MeTaAia i BiAnOBiAHO AO aKTklBHOCTi meTaAi8, Hanpm«aa
![]() Y HaaegxeHOMY 3POCTaHHfi aKThBHOCTi meTaAY nc)Ka3aH0 CTPiAOHKOlO i 8iAnoaiaae P03TClUjyaaHHfO eæmeHTia y aKTk18HOCTi -MeTCIAiB. ILIO Aiaiue p03Miu-ueHL,11h .MeTCIA y PfiAi
Y HaaegxeHOMY 3POCTaHHfi aKThBHOCTi meTaAY nc)Ka3aH0 CTPiAOHKOlO i 8iAnoaiaae P03TClUjyaaHHfO eæmeHTia y aKTk18HOCTi -MeTCIAiB. ILIO Aiaiue p03Miu-ueHL,11h .MeTCIA y PfiAi ![]() aKTMBHOCTi, TO ail-i XiMiHHO a«maHiU-lVlh, CMAbHiUJVtV1 BiAHOBH%lK, .Aeruje OFUCH*O€TbCfi, aaxye
aKTMBHOCTi, TO ail-i XiMiHHO a«maHiU-lVlh, CMAbHiUJVtV1 BiAHOBH%lK, .Aeruje OFUCH*O€TbCfi, aaxye
BiAHOBA}O€TbCfi 3 horo VIOHiB. Y XiMiHH%lX peaKl-Lisx OKklCHMK np%€AHY€ e,meKTPOHM, TOMY B![]()
![]() enxeKTPOHH KaTi0HY Fe 2+, ail-i e Hav7C%AbHiLlJVlM OKklCHMKOM.
enxeKTPOHH KaTi0HY Fe 2+, ail-i e Hav7C%AbHiLlJVlM OKklCHMKOM.
Y nepuih np06ipui X(Fe) He BklTHCKye Y (Zn), TOMY 1±10 e Mel-Il-I] aKTk18HVlM meTCIAOM. Y .apyrirl np06ipui Y(Zn) He BYITHCKye Z(Mg), TOMY 1±10 € Mey-lU-l aKTk13HHM MeraAOM. Y TpeTiV1 np06ipLli Z(Mg) BMTklCKY€ X(Fe), TOM}/ e 6iAbLIJ Cll<TklBHk1M MeraAOM. Chxe, peauih BiA6YBaeTbCR ![]() AMI.ue B TpeTii np06ipui.
AMI.ue B TpeTii np06ipui.
BiAn0BiAs: B.
ЗНО онлайн 2018 року з xiMfl'— основна сес1я
|
ч |
|
23 |
24 |
25 |
|
26 |
|
27 |
28 |
29 |
зо |
31 |
|
32 |
|
34 |
|
35 |
|
36 |
|
37 |
|
|
|
|
Завдоння 29 з 52 |
|||||||||||||||||||||||
|
|
||||||||||||||||||||||||
|
|
|
|
||||
|
|
|
ЗНО-2018 (ОСНОВНАСЕСЈО29 i3 52 |
||||
|
У до розчину пдроксиду добавили купрум(11) сульфату. До осаду що утворився. добавили А етанол cuS04 + 2NaOH Б пропаналь сњ—он ХаОН В пропан-2-ол Г етан- 1 1 етиленглАколь |
||||||
|
крапель розчину розчин речовини прозорий розчин темно- - реактив 6araToaT0.MHi спиртн + Na2S04 сщ—о--._ си сщ—о розчин
пропан-2-ол |
на
|
Х.
|
||||
|
А Б В Г |
НзС—СНт---0Н етанол пропаналь |
|||||
|
|
||||||
![]()
![]() У
У ![]() до розчину пдроксиду добави-ти
до розчину пдроксиду добави-ти ![]() крапель розчнну купрум(П) су:љфату До осаду, що утворився, добавили розчин речовини Х.
крапель розчнну купрум(П) су:љфату До осаду, що утворився, добавили розчин речовини Х. ![]() сумтш ретельно пере.мц.цали: утворився прозорий розчин темносинього кольору. Речовина Х — це
сумтш ретельно пере.мц.цали: утворився прозорий розчин темносинього кольору. Речовина Х — це
А етанол
Б пропаналь
В пропан-2-ол
Г етан-1![]()
У пробђон„у з розчином алюмж1й хлориду учень добавив по крап.лях розчнн натр:й пдроксиду до утворення осаду, лкий поим роздппв на дм прооцжи.
![]()
![]() У вж добавив надлпшок розчину
У вж добавив надлпшок розчину ![]() г1дрокспду, у П
г1дрокспду, у П ![]() кислоти. Унаслдок цього осад
кислоти. Унаслдок цього осад![]()
![]() А розчинивсл лише в
А розчинивсл лише в![]()
Б розчннився лише в П![]()
в розчинився i в i в П![]()
Г не розчижљся Hi в I, Hi в П![]()
ТЕМА: ![]() речовини i iXHi
речовини i iXHi![]()
Зовдання скеровоно но перевћрку ![]() сутђ амфотерностј, умЈння пояснювати
сутђ амфотерностј, умЈння пояснювати
результати![]()
![]() — нерозчинна у сполука, тому його можно добути реокцјею 06MiHY мЪк рознинною стлю
— нерозчинна у сполука, тому його можно добути реокцјею 06MiHY мЪк рознинною стлю ![]() i лугом у водному рознинђ:
i лугом у водному рознинђ:
AlC13 + 3NaOH — АЦОН)3 +3NaCl;
АЦОН)зј .
бјлий драглистий
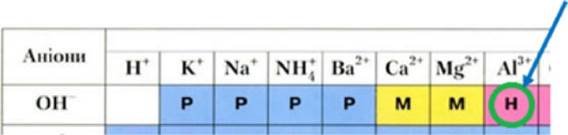
![]() називають деяких хћмћнних сполук залежно вћд умов виявляти обо оснбвнћ, обо кислотнђ властивостј. З кислотами алюмђнћй гћдроксид реагуе як основа, i3 лугами — як кислота, тобто виявляе амфотернђ
називають деяких хћмћнних сполук залежно вћд умов виявляти обо оснбвнћ, обо кислотнђ властивостј. З кислотами алюмђнћй гћдроксид реагуе як основа, i3 лугами — як кислота, тобто виявляе амфотернђ![]()
Тому осад олюмЈн•џ7 гћдроксиду розчиняеться в в лугу:
АЦОН)з + ,3HCl = AlC13 + 31120;
АЦОН)3 + 3NaOH [АЦОН)6].
У ![]() I
I ![]() розчин пдроксиду. а в
розчин пдроксиду. а в ![]() II розчин
II розчин ![]() хлориду. В 06E13i
хлориду. В 06E13i ![]() ,дооампи розчин речовини Х. Унаслдок цього
,дооампи розчин речовини Х. Унаслдок цього ![]() утворення осаду i в npooipui 1, i в
утворення осаду i в npooipui 1, i в ![]() П. РечовинаХ це
П. РечовинаХ це
![]() А натртй ютрат
А натртй ютрат
Б магюй жтрат
ТЕМА: ![]() речовини i •tXHi
речовини i •tXHi![]()
|
В |
натртй сульфат |
Завдання скеровоно но перевђрку вм(ння застосовувоти знання про xiMiHHi |
|
Г |
|
визнонати можливпсть перебћгу реокщТ обмћну мћж електролћтоми в рознин1. |
Проаножзувавши умову завдання, можно висновку. що Т задовольнить реновино, яка у водному ![]() з утворенням:
з утворенням:
• анћонћв, якћ осад.жують кат1они k0Aio i Борћю,•
• kQTi0HiB, 9i<i утворюють осад 13 ![]() i хлорид-0}-Пономи.
i хлорид-0}-Пономи.
цо умову з-помЪк новедених ворћонтћв Јдпов1д1 задовольняе лише могнћй сульфат:
MgS04 + ЖОН 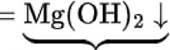 -+k2S04;
-+k2S04;
бЈлий драглистий
MgS04 + Вась BaS04$ + МдС12.
„бћий
![]()
![]() Г.
Г.


про публікацію авторської розробки
Додати розробку




