Сульфатна кислота. Хімічні властивості.
 Сульфатна кислота. Хмчн властивост .
Сульфатна кислота. Хмчн властивост .
Особливості взаємодії металів з концентрованою сульфатною кислотою
Мета: навчальна: поглибити знання про
будову властивост сульфатної кислоти;
розвинути ум ння по складанню
окислювально-в дновного балансу р внянь реакц й, п дготувати
здобувач в осв ти до усп шної здач ЗНО.
 розвиваюча : розвивати нтерес до предмета, ум ння висловлювати свої думки, лог чно м ркувати.
розвиваюча : розвивати нтерес до предмета, ум ння висловлювати свої думки, лог чно м ркувати.
виховна: формувати поняття, про необхднсть
дотримування правил технки безпеки, при зустрч з кислотою в побут .
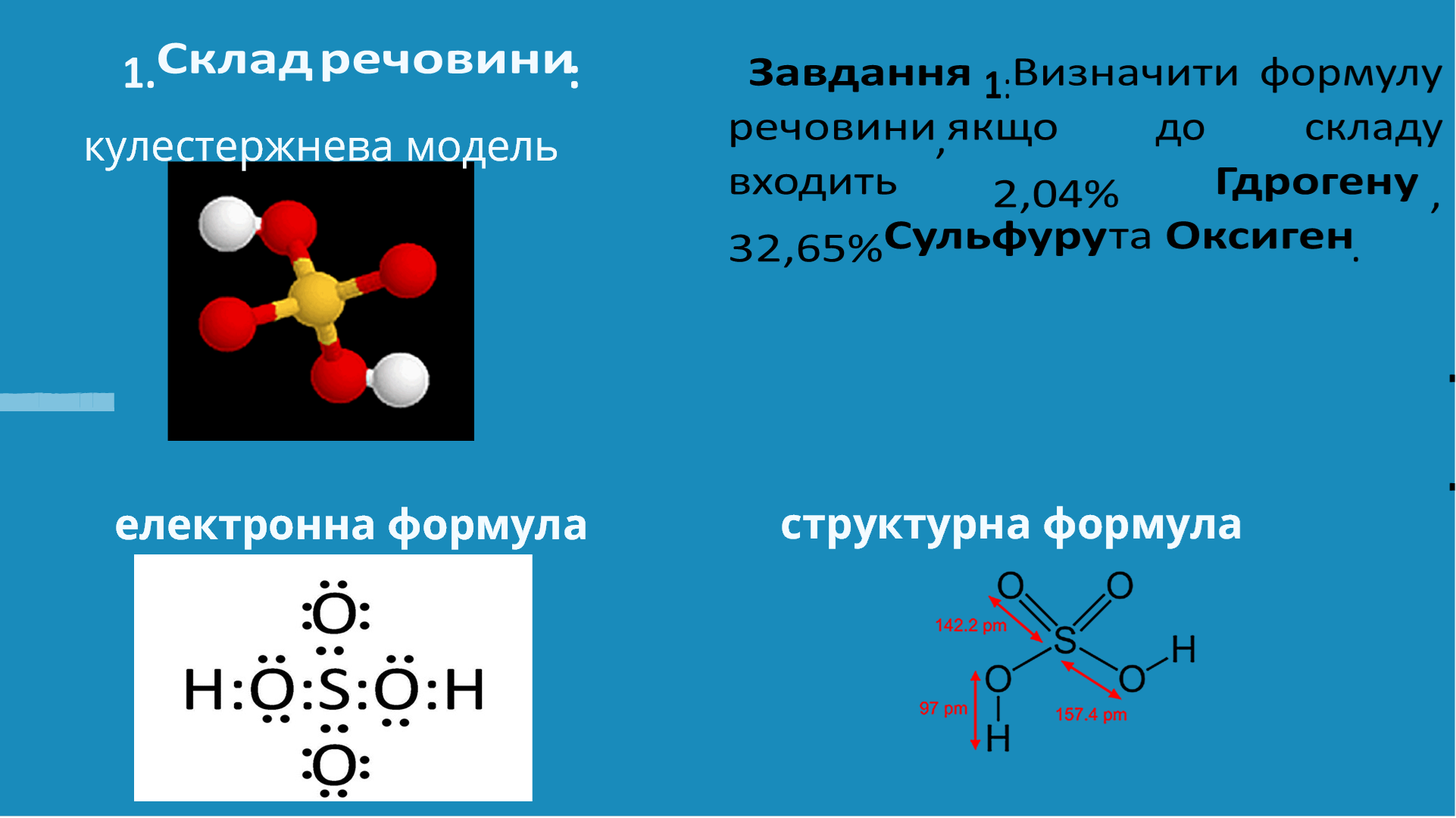
ПЛАН: 1. Склад речовини

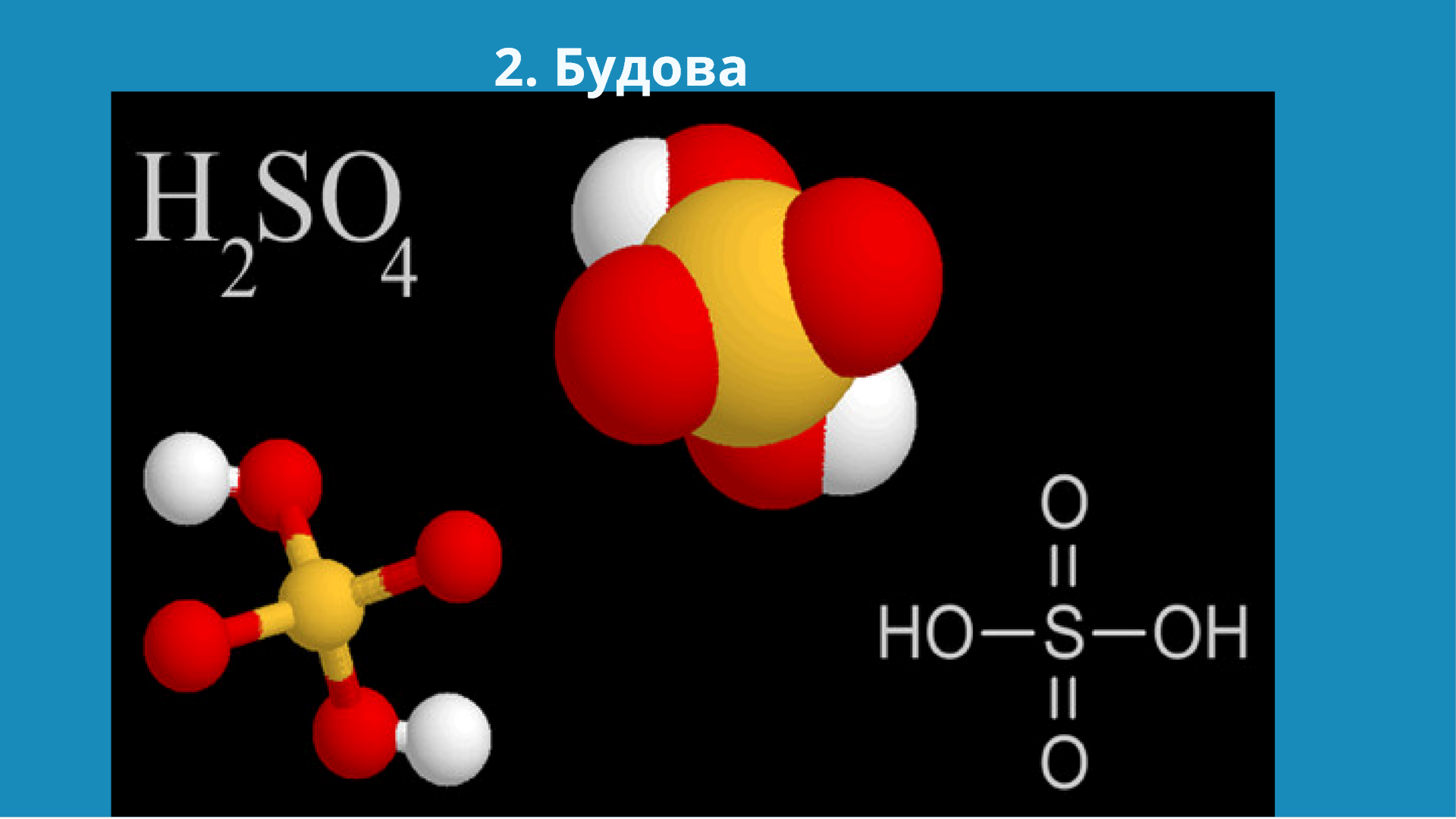
2. Будова.
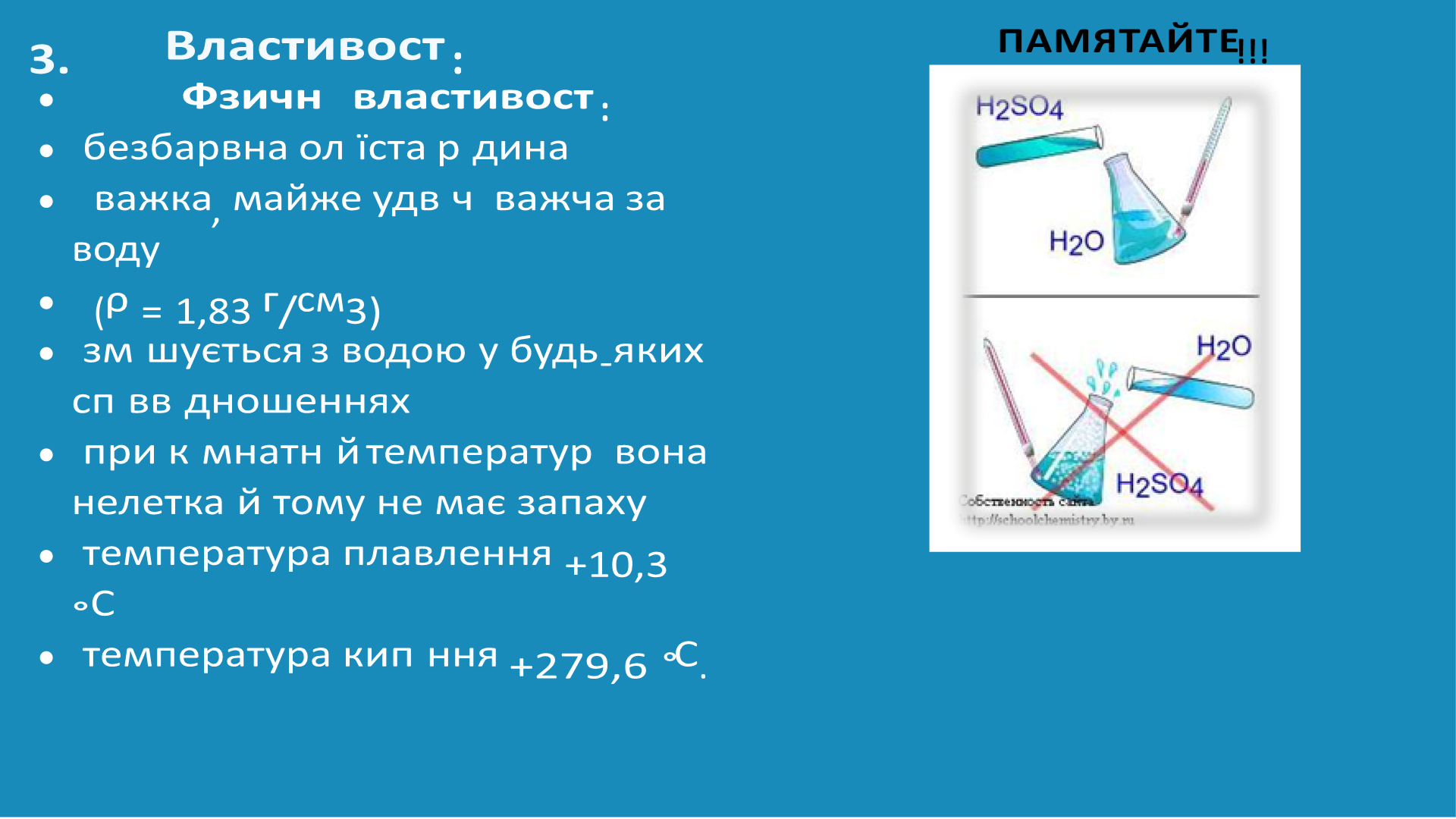
3.Властивост
4.Застосування
5.Добування
![]()

ЗАВДАННЯ 3:
НА ЗОВНІШНЬОМУЕНЕРГЕТИЧНОМУ РІВНІ АТОМА
ХІМІЧНОГО ЕЛЕМЕНТА, ЩО ПЕРЕБУВАЄ В ОСНОВНОМУ
 СТАНІ, ЧИСЛО НЕСПАРЕНИХЕЛЕКТРОНІВ УДВІЧІ МЕНШЕ ЗА ЧИСЛО СПАРЕНИХ. НАЗВАЦЬОГО ЕЛЕМЕНТА – А. Силцй Б. Фосфор
СТАНІ, ЧИСЛО НЕСПАРЕНИХЕЛЕКТРОНІВ УДВІЧІ МЕНШЕ ЗА ЧИСЛО СПАРЕНИХ. НАЗВАЦЬОГО ЕЛЕМЕНТА – А. Силцй Б. Фосфор
В. Сульфур
Г. Хлор
Х м чн властивост розбавленої сульфатної кислоти:
Х м чн властивост розбавленої сульфатної кислоти:
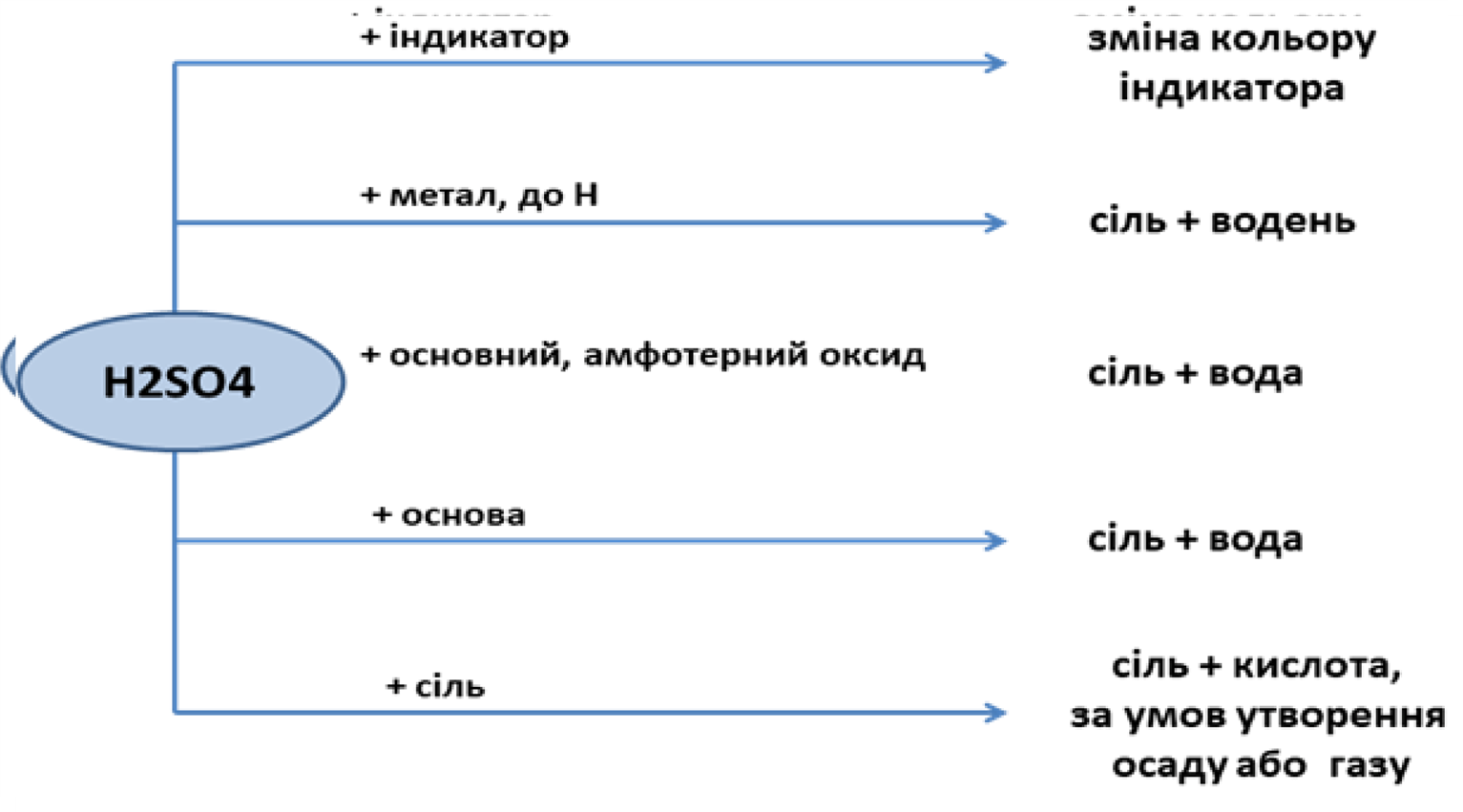
Х м чн властивост розбавленої сульфатної кислоти:

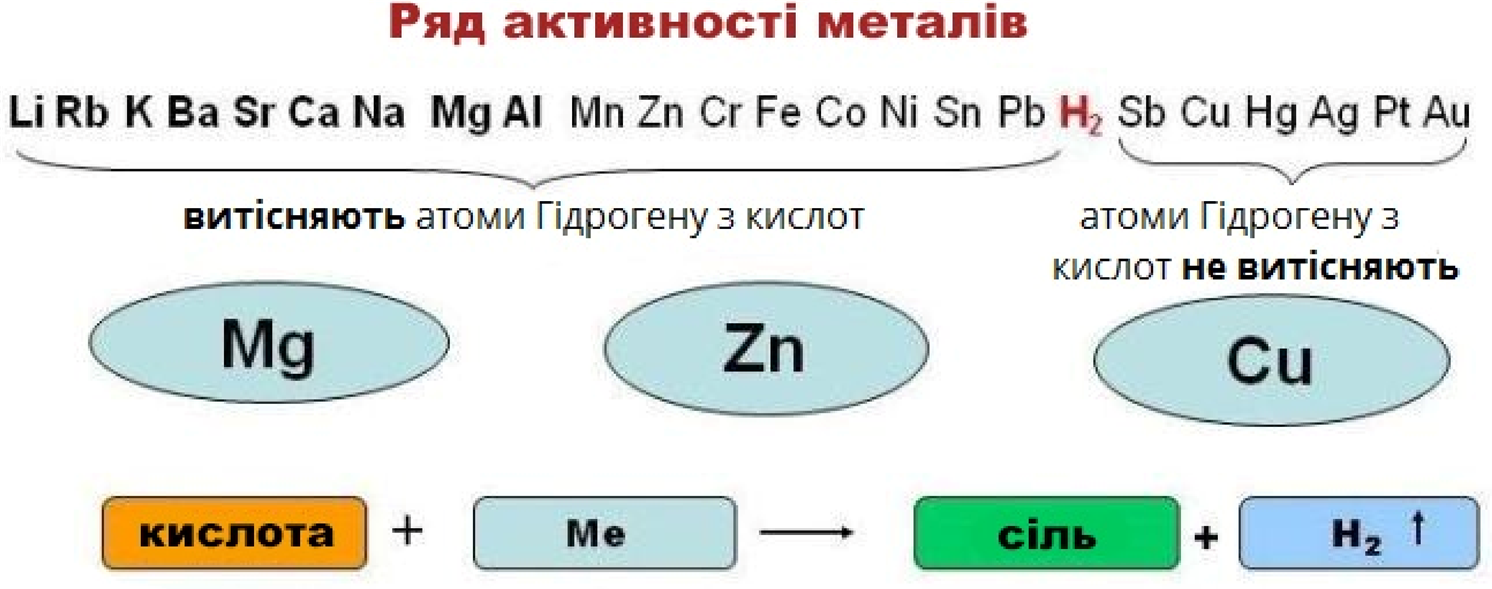
Реакційна здатність розведеної сульфатної кислоти з металами різної електронегативності: алюміній (Al) окиснюється найлегше, цинк (Zn) та залізо
(Fe) активно виділяють водень, в той час як свинець (Pb) пасивується через утворення плівки нерозчинного сульфату, а електронегативна мідь (Cu) майже не реагує.



Завдання 7: Необоротна реакц я в дбувається у водному розчин м ж:
А. кал й хлоридом купрум(ІІ) н тратом.
Б. натр й сульфатом кал й г дроксидом.
 В. бар й хлоридом сульфатною кислотою. Г. натр й н тратом ферум (ІІІ) хлоридом.
В. бар й хлоридом сульфатною кислотою. Г. натр й н тратом ферум (ІІІ) хлоридом.
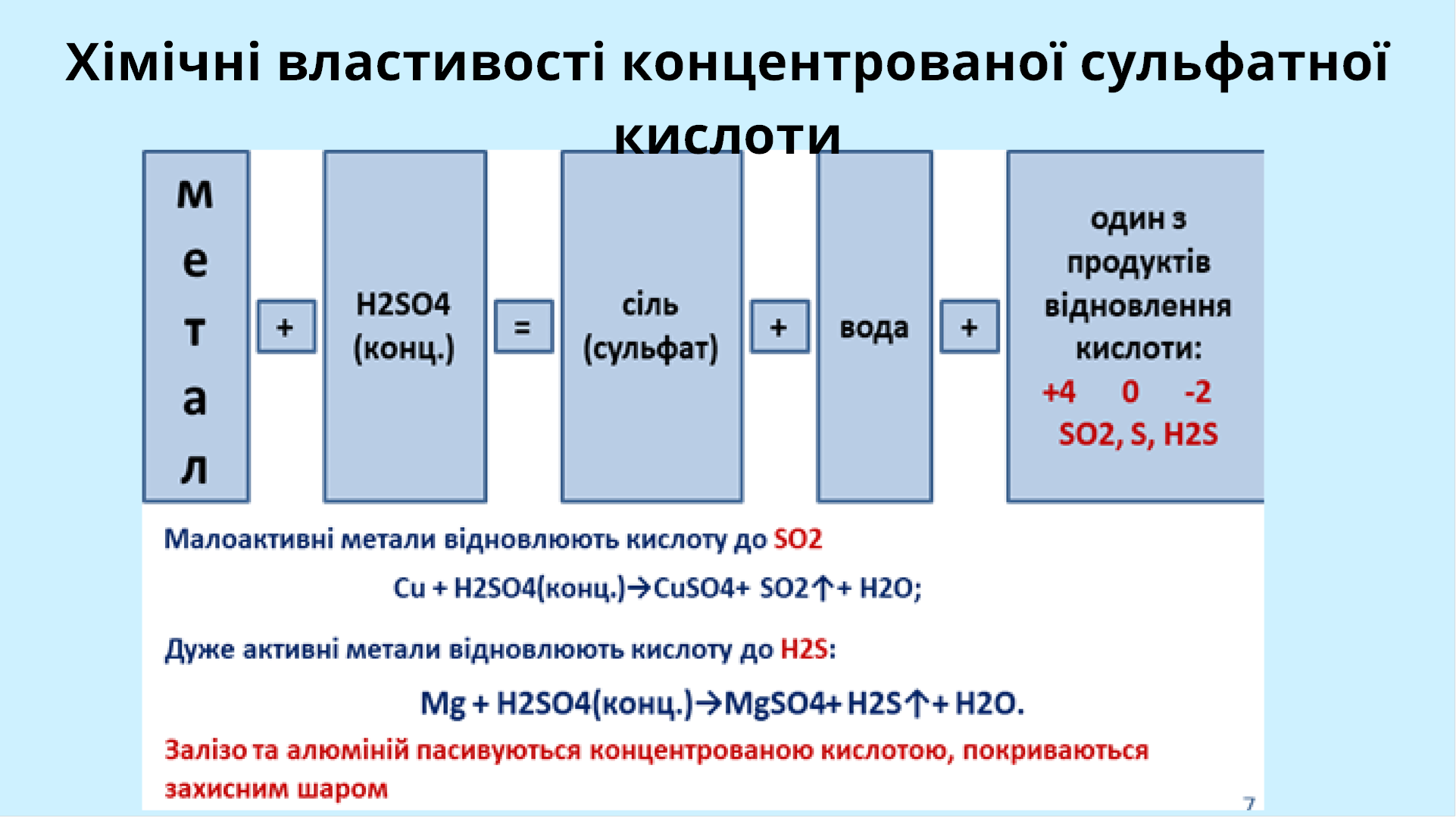
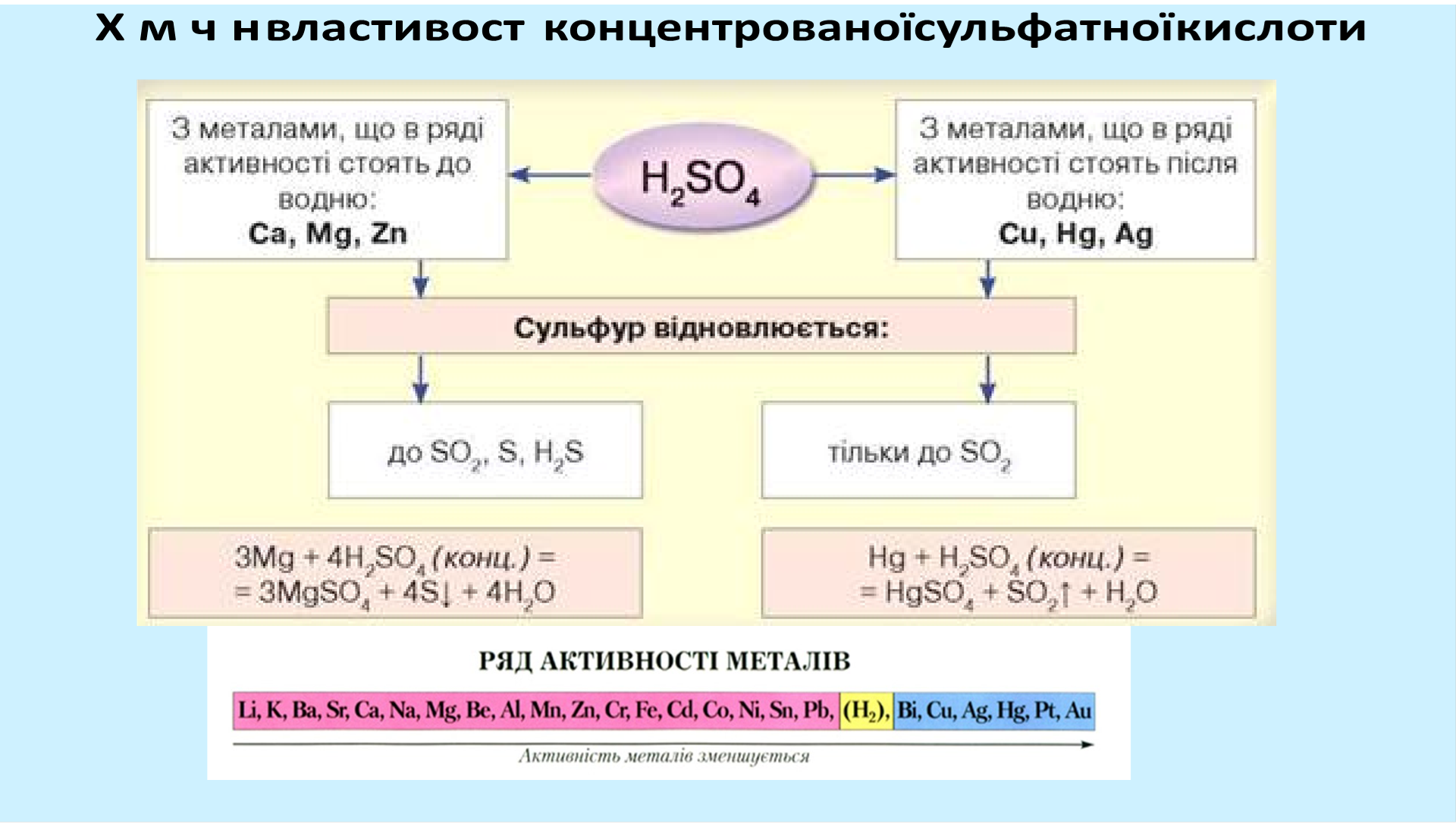

 Концентрована с рчана кислота має сильний окислювальний ефект здатна реагувати, при нагр ванн , нав ть з благородними металами,
Концентрована с рчана кислота має сильний окислювальний ефект здатна реагувати, при нагр ванн , нав ть з благородними металами,
такими якм дь, ртуть ср бло, хоча при цьому
вона невзаємод є з зал зом та деякими ншими металами через їх пасивац ю. Тому для
перевезення концентрованої сульфатної кислоти використовують зал зн цистерни.
 Сульфатна кислота руйнує також багато органічних речовин, зокрема вуглеводи — дерево, папір, бавовняні тканини, цукор тощо.
Сульфатна кислота руйнує також багато органічних речовин, зокрема вуглеводи — дерево, папір, бавовняні тканини, цукор тощо.
Руйнування цих речовин обумовлюється тим, що концентрована сульфатна
кислота віднімає від них водень і кисень у вигляді води, а вуглець залишається у вигляді пористого вугілля.


![]()
![]()
![]()
![]()
![]()
Контактний метод (промисловий)
У промисловостс рчану кислоту отримують окисленням с рки дос рчистого газу. С рку беруть елементарну, абос рчаний колчедан, або с рководневовм сн гази.
S(s)+O2⟶SO2
С рчистий газокиснюють до триоксиду (с рчаного анг дриду) на твердому ванад євому катал (дана реакц я екзотерм чна, тому застосовується пром жне охолодження п сля першого шару за допомогою трубних пучк в, через як подається пов тря,
2SO2+O2↽−−⇀2SO3
П сля наступнихдвох ступен в — за допомогою к льцевої труби, що має великий д аметр, через яку подаєтьсяпов тря, над якою розташований дефлектор.
![]() Триоксид с рки поглинається97–98 % H2SO4 з утворенням олеуму (H2S2O7), також в домого як димляча с рчана або п рос рчанакислота. Пот м олеум розбавляють водою з утворенням концентрованої с рчаної кислоти.
Триоксид с рки поглинається97–98 % H2SO4 з утворенням олеуму (H2S2O7), також в домого як димляча с рчана або п рос рчанакислота. Пот м олеум розбавляють водою з утворенням концентрованої с рчаної кислоти.
H2SO4+SO3⟶H2S2O7 H2S2O7+H2O⟶H2SO4
С рчану кислоту, яку одержують таким способом, також називають«контактною»
(концентрац я 92–94 %).
![]()
Мокрий метод
На першомуетап с рка спалюється для отримання д оксиду с рки:
S+O2⟶SO2
або, ж, с рководень спалюється до газу д оксиду с рки:
2H2S+3O2⟶H2O+2SO2
Пот м д оксид с рки окислюється до триоксиду с ркиза допомогою кисню з оксидом ванад ю (V) яккатал затором.
2SO2+O2↽−−⇀SO3
Триоксидс рки г дратується в с рчану кислоту:
SO3+H2O⟶H2SO4
Останн метапом є конденсац я с рчаної кислоти дор дкої 97–98 % H2SO4 :
H2SO4(g)⟶H2SO4(l)
![]() Пряме розчинення SO3 увод (мокрий метод), р дко практикується, оск льки реакц я є надзвичайно екзотерм чною, що призводитьдо утворення гарячого аерозолю с рчаної кислоти, який потребує конденсац ї та в дд лення.
Пряме розчинення SO3 увод (мокрий метод), р дко практикується, оск льки реакц я є надзвичайно екзотерм чною, що призводитьдо утворення гарячого аерозолю с рчаної кислоти, який потребує конденсац ї та в дд лення.
Нтрозний спосб
Окисленнядоксиду срки доксидом азоту у присутностводи.
![]() Саме у такий спосбвдбулася реакця у повтр Лондона пд час Великого смогу.
Саме у такий спосбвдбулася реакця у повтр Лондона пд час Великого смогу.
SO2+NO2+H2O=H2SO4+NO
Удосконаленням технолог ї виробництвасульфатної кислоти займався український х м к ІванЄвграфович
Ададуров (1879-1938)
Домашнє завдання
П дручник П. Попель, Л.Криля
Київ Видавничий центр
|
5-157 |
|
,1 |
![]() «Академ я» 2019
«Академ я» 2019
§21№ 155-157,158 стор 127
Домашнє завдання
Завдання 14:
Яку масу(г) води необх дно зм шати з олеумом масою400г, масова частка
сульфур (VI) оксиду в якому 20%, щоб
утворився розчинз масовою часткою сульфатної кислоти 40%?
|
5-157 |
|
,1 |
![]() Завдання15:
Завдання15:
На сум ш масою 10г, що складається з зал за там д , под яли надлишком
розбавленої сульфатної кислоти, унасл док
чого вид лився газ об’ємом 2.8л (н.у.).
Обчисл ть масовучастку (%) зал за у сум ш .


про публікацію авторської розробки
Додати розробку
