тест НМТ хімія (24 питання)
Обчисліть об'єм водню (н.у.), що виділиться внаслідок взаємодії цинку масою 6,5 г з надлишком хлоридної кислоти.
До складу якої з речовин входить найменше хімічних елементів?
Укажіть речовину з йонним типом хімічного зв’язку.
Укажіть кількість речовини (моль) катіонів, що утворилися внаслідок електролітичної дисоціації в розбавленому водному розчині натрій сульфату кількістю речовини 3 моль.
У якій із хімічних реакцій підвищення тиску спричинить зміщення хімічної рівноваги в бік утворення реагентів?
Який метал реагує з водним розчином ферум(ІІ) сульфату?
Гідратація алкенів є реакцією
Проаналізуйте твердження й укажіть правильні.
І. Бензен знебарвлює бромну воду.
ІІ. Бензен можна добути тримеризацією етану.
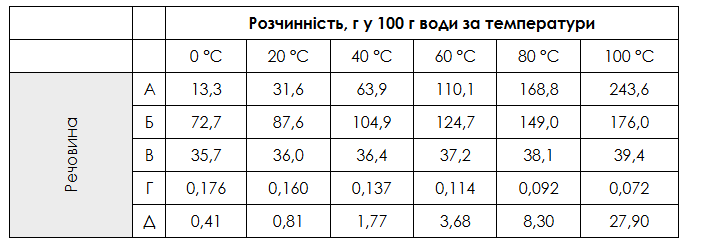
У таблиці наведено значення розчинності речовин А – Д у воді за різних температур. Використавши дані таблиці, доповніть кожне речення 1–3 буквою А – Д так, щоб утворилося правильне твердження.
1. З підвищенням температури розчинність речовини … зменшується.
2. За температури 40 °C в насиченому розчині речовини … її маса більша, ніж маса розчинника.
3. Максимальна маса речовини …, яку можна розчинити у воді масою 150 г за температури 20 °C, становить 47,4 г.
Біогаз ─ це суміш, основними компонентами якої є метан, карбон (ІV) оксид. Обчисліть об’єм (м3) кисню (н. у.), що витрачається на спалювання біогазу об’ємом 10 м3, з об’ємною часткою метану − 70 % і карбон (ІV) оксиду − 30 %.
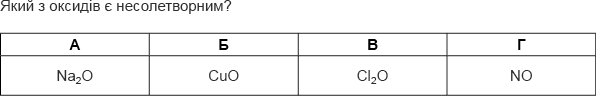
оксид?
Правильне твердження наведено в рядку
Яку речовину одержують гідролізом крохмалю?
Увідповідніть інформацію щодо хімічних реакцій, наведену в лівому й правому стовпчиках.
Хімічна реакція
1 гідратація кальцій оксиду
2 розкладання кальцій карбонату
3 розкладання гідроген пероксиду
Що утворюється внаслідок її перебігу
А проста й складна речовини
Б дві складні речовини
В лише складна речовина
Г дві прості речовини
Д лише проста речовина
Обчисліть масу (г) етанової кислоти, що утвориться внаслідок окиснення етаналю масою 110 г, якщо відносний вихід кислоти становить 80 %.
Обчисліть відносну густину карбон(ІІ) оксиду за гелієм.
Є чотири пробірки з розчинами, що утворилися внаслідок змішування з водою речовин, формули яких: 1 – NH3, 2 – NaCl, 3 – H2S, 4 – SO2. У кожну із чотирьох пробірок добавили кілька крапель водно-спиртового розчину фенолфталеїну. Укажіть номер пробірки, у якій індикатор набув малинового кольору.
Укажіть хімічну формулу негашеного вапна.
Визначте тип реакції, внаслідок якої рідкі жири перетворюються у тверді.
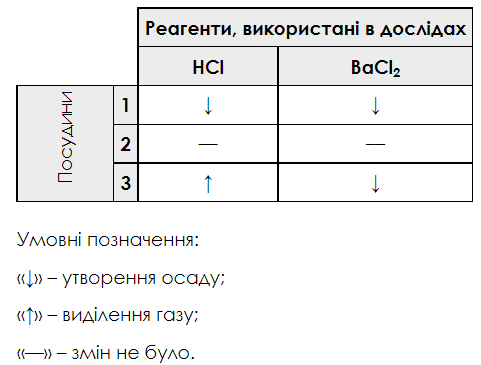
У кожній з посудин 1-3 міститься водний розчин певної солі (А – Д). З ними провели такі досліди. Спочатку вміст кожної посудини розділили на дві пробірки: в одну добавили хлоридну кислоту, а в другу – водний розчин барій хлориду. За наведеними в таблиці результатами дослідів укажіть уміст посудин 1-3.
АMg(NO3)2
Б Na2CO3
В K2SiO3
Г MgSO4
Д K2SO4
Негашене вапно (кальцій оксид) добувають прожарюванням вапняку, головним складником якого є кальцій карбонат. Класифікуйте цю реакцію.
Яким з описаних дослідів доведено амфотерні властивості однієї з речовин?
Обчисліть відносну молекулярну масу естеру, який утворився внаслідок реакції метанолу з етановою кислотою.
Визначте молекулярну формулу газуватого вуглеводню, що містить 80% Карбону. Відносна густина цієї речовини за воднем становить 15. Обчисліть суму індексів у формулі вуглеводню.

Створюйте онлайн-тести
для контролю знань і залучення учнів
до активної роботи у класі та вдома


















