Завдання І етапу Всеукраїнської олімпіади з хімії
В алхімії і астрології існують стійкі асоціації між металами і небесними тілами, як, наприклад, Сонце – золото, Меркурій – ртуть, Марс – мідь, тощо. Однак ці асоціації не мають наукового підґрунтя. А який хімічний елемент і за назвою і за поширеністю має безпосереднє відношення до Сонця? :
З переліку оберіть природні речовини:
Розставте коефіцієнти в рівнянні реакції
Al + H2SO4 = Al2(SO4)3 +H2
Сума коефіціентів в даному рівнянні становить:
1. Розташуйте рівняння реакцій у порядку зростання суми коефіцієнтів
А. Р + О2 = РV…
Б. S + O2 = SIV…
В. H2O2 =
Г. CH4 + O2 =
реакції що відбуваються в одному напрямку є необоротними якщо
вкажіть типи хімічних реакцій за напрямком перебігу реакцій
якщо реагент однієї реакції є продуктом другої і навпаки то це
Розташуйте речовини за зростанням сили електролітів:
А сульфатна кислота
Б вода
В ортофосфатна кислота
Г сульфідна кислота
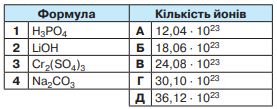
Установіть відповідність між формулою речовини та кількістю йонів, на які повністю дисоціює 1 моль цієї речовини.
Обчисліть ступінь електролітичної дисоціації бромідної кислоти, якщо в її розчині міститься 0,9 г йонів Гідрогену та 0,1 моль молекул, що не розпалися на йони.
Колір йонів під час гідратації може змінитися. Наприклад, негідратовані йони Купруму безбарвні, а гідратовані - блакитні. Відомо, що розчин сульфатної кислоти у воді безбарвний. Передбачте колір розчину купрум (ІІ) сульфату у воді.
Позначте речовини, розчини яких у воді є електролітами.
Сумарне рівняння дисоціації ортофосфатної кислоти має вигляд:
Яка з представлених кислот є слабким електролітом:
Які з нижченаведених електролітів відносяться тільки до слабких
Суспензія — це суміш води з
1 бензином, 2 олією, 3 глиною, 4 піском, 5 нафтою, 6 крейдою
Складіть рівняння реакції йонного обміну між калій гідроксидом і
алюміній хлоридом. Скорочене йонне рівняння:
Складіть рівняння якісної реакції між натрій бромідом і аргентум нітратом.
Скорочене йонне рівняння:
Вкажіть значення концентрації йонов Н+ (моль/л) у розчині одноосновної кислоти з рН = 5,0, якщо ступінь ї їдисоціації становить 100%.
У початковому розчині містилося 18 молекул кислоти. Після дисоціації залишилось 6 молекул. Обчисли ступінь дисоціації (%) кислоти:

Створюйте онлайн-тести
для контролю знань і залучення учнів
до активної роботи у класі та вдома


















