Урок "Діагностична контрольна робота"
У розробці використано різноманітні цікаві прийоми критичного мислення. Дігностична контрольна робота проводиться з метою перевірки знань учнів. Матеріали можна використовувати при підготовці уроків хімії у інших класах.
Урок № 3
Тема : Діагностична контрольна робота
Мета: Формування ключових компетентностей:
-саморозвитку й самоосвіти-уміння розв’язувати задачі;
-соціальної-вчити дітей, спираючись на отримані знання, самостійно працювати. Компетентності у галузі природничих наук, техніки і технологій;
інноваційність; екологічна компетентність; інформаційно-
комунікаційна компетентність, соціальні компетентності, культурна
компетентність; підприємливість та фінансова грамотність.
розвивати вміння користуватись хімічними формулами для
позначення складу речовини ; виховувати культуру хімічної мови.
Формування предметних компетентностей:
-повторити основні поняття хімії, вивчені в 7 класі: речовина, матеріал, суміші, атом, молекула, хімічний елемент, прості та складні речовини, хімічна формула, індекс, коефіцієнт, валентність, фізичні та хімічні явища, хіміча реакція, реакція сполучення і розкладу;виховувати інтерес до вивчення хімії.
розвивати вміння користуватись хімічними формулами для
позначення складу речовини ; виховувати культуру хімічної мови.
Хід уроку
І.Організація класу.
«Я вітаю»
«Я вітаю тих, хто…» (… має хороший настрій; добре виспався; хоче працювати; виконав домашнє завдання; в доброму гуморі; хотів би дізнатися щось нове; хоче спілкуватися… тощо). Після кожної фрази учні, які вважають, що фраза стосується їх, підводяться. Учитель та учні аплодують.
ІІ. Фаза актуалізації .

1.«Інструктаж щодо виконання контрольної роботи»
ІІІ.Фаза консолiдацiї

1.Контроль знань
![]() - перевірк знань учнів
- перевірк знань учнів
![]() -зошити для контрольних робіт, ручки, калькулятори, періодична система
-зошити для контрольних робіт, ручки, калькулятори, періодична система
![]() -Самостійна робота для учнів всього класу, два варіанти завдань.
-Самостійна робота для учнів всього класу, два варіанти завдань.
![]() - 40 хвилини
- 40 хвилини
![]() - позитивне налаштування,уважність
- позитивне налаштування,уважність
Варіант I
У запитаннях 1-9 укажіть правильну відповідь.
1. Якому елементу відповідає значення відносної атомної маси 23?
а) Магнію; г) Сульфуру;
б) Силіцію; д) Хлору.
в) Натрію;
2. Виберіть правильний запис складу формули FeCl2:
а) молекула FeCl2 складається з одного атома Феруму і двох атомів Хлору;
б) молекула FeCl2 складається з одного атома Феруму і двох атомів Карбону;
в) до складу FeCl2 входять два елементи: Ферум і Хлор;
г) до складу FeCl2 входять два елементи: Ферум і Карбон.
3. Кисень першим відкрив:
а) Дж Пристлі; в) Мао-Хоа;
б) К. Шеєле; г) А. Лавуазьє.
4. Який запис означає «чотири молекули водню»?
а) 4HCl; в) 4H2;
б) 4H; г) 4H2O.
5. Яка валентність Феруму в сполуці Fe2O3 ?
а) II; в) IV;
б) I; г) III.
6. Вкажіть хімічне явище:
а) іржавіння заліза; в) танення льоду;
б) розчинення цукру у воді; г) фільтрування розчину.
7. Яке з понять є зайвим у наведеному рядку?
а) Залізо; в) каструля;
б) мідь; г) срібло.
8. Формула ферум(ІІ) оксиду:
а) FeO; в) Fe (OH)3;
б) Fe2O3; г) Fe3O4.
9. Вкажіть чисті речовини:
а) кисень; в) залізо;
б) молоко; г) річкова вода.
10. Установіть відповідність між вихідними речовинами і продуктами реакцій.
|
1) K i Cl2 |
a) CO2 |
|
2) C i O2 |
б) BaS |
|
3) Ba i S |
в) KCl |
|
4) К і O2 |
г) K2O |
|
|
Д) CuO |
11. Заповніть таблицю формулами складних речовин, які можна отримати з наведених елементів.
|
|
Cl |
O |
|
Na |
|
|
|
Ca |
|
|
|
Li |
|
|
|
Al |
|
|
12. Установіть відповідність між назвами та формулами речовин.
|
1) Сульфур(IV) оксид |
а) BaO |
|
2) Фосфор(V) оксид |
б) CaI2 |
|
3) Кальцій йодид |
в) P2O5 |
|
4) Барій оксид |
г) SO2 |
|
5) Нітроген(II) оксид |
д) FeCl2 |
|
6) Ферум(II) хлорид |
е) NO |
13. Складіть рівняння реакцій за наведеними схемами:
а) CH4 + O2→ CO2+ H2O
б) P + O2→ P2O3
14. Маса води, під час розкладання якої електричним струмом утворилося 12 г водню та 96 г кисню, дорівнює:
а) 110 г; в) 220 г;
б) 96 г; г) 108 г.
15. Обчисліть масові частки елементів у ферум(ІІ) хлориді.
16. Запишіть формули гідроксидів, що відповідають таким оксидам:
SO2, CaO, MgO.
17. Допишіть рівняння хімічних реакцій:
а) Al + O2 →
б) ZS + O2 →
18. В якій речовині масова частка Феруму більша: Fe (NO3 )2 чи FeSO4 ?
19. Складіть рівняння реакцій за схемами й дайте назви сполукам:
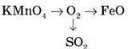
20. Виведіть молекулярну формулу речовини, масова частка Феруму в якій 70 %, Оксигену — 30 %, відносна молекулярна маса сполуки — 160.
Варіант II
У запитаннях 1-9 укажіть правильну відповідь.
1. Якому елементу відповідає значення атомної маси 12?
а) S; в) Cl;
б) O; г) C.
2. Найбільше Оксигену міститься:
а) у літосфері; в) у гідросфері;
б) в атмосфері; г) у космосі.
3. Першим дослідив властивості кисню:
а) К. Шеєле; в) Мао-Хоа;
б) А. Лавуазьє; г) Дж. Пристлі.
4. Виберіть формулу гідроген пероксиду:
а) Na2O2; г) K2O;
б) H2O2; д) CO2.
в) C2H2;
5. Яка валентність Купруму в оксиді CuO?
а) II; в) IV;
б) I; г) III.
6. Вкажіть фізичне явище:
а) випаровування води;
б) скисання молока;
в) пожовтіння листя;
г) одержання гуми з нафти.
7. Яке з понять є зайвим?
а) Вода;
б) лід;
в) сніжинка;
г) пара.
8. Відносна молекулярна маса Fe3O4 дорівнює:
а) 232; в) 112;
б) 160; г) 132.
9. Виберіть із переліку фізичні властивості газоподібного кисню:
а) без запаху;
б) крихкий;
в) нерозчинний у воді;
г) розчинний у воді.
10. Установіть відповідність між вихідними речовинами і продуктами реакцій.
|
1) Cu i O2 |
а) CaCl2 |
|
2) Li i Br2 |
б) CuO |
|
3) Ca i Cl2 |
в) LiBr |
|
4) Са і O2 |
г) СО |
|
|
д) СаО |
11. Заповніть таблицю формулами складних речовин наведених елементів.
|
|
O |
S |
|
К |
|
|
|
Ba |
|
|
|
Cr(III) |
|
|
|
Mg |
|
|
12. Установіть відповідність між назвою та формулою речовин.
|
1) Карбон(IV) оксид |
а) MgO |
|
2) Калій оксид |
б) CaCl2 |
|
3) Кальцій хлорид |
в) CuCl |
|
4) Магній оксид |
г) K2O |
|
5) Фосфор(ІІІ) оксид |
д) CO2 |
|
6) Купрум(I) хлорид |
е) P2O3 |
13. Складіть рівняння реакцій за наведеними схемами:
а) Al + Cl2→ AlCl3
б) C3H8 + O2→ CO2 + H2O
14. Під час взаємодії міді масою 6,4 г з киснем масою 1,6 г утвориться купрум(ІІ) оксид масою:
а) 4,8 г;
б) 4 г;
в) 8 г;
г) 10,24 г.
15. Запишіть формули гідроксидів, що відповідають таким оксидам:
SO3, ВaO, P2O5.
16. Обчисліть масові частки елементів у ферум(ІІ) оксиді.
17. Допишіть рівняння реакцій:
а) Ca + S →
б) CH4 + O2 →
18. В якій речовині масова частка Феруму більша: Fe (NO3 )3 чи Fe (OH)2?
19. Складіть рівняння реакцій за схемами й дайте назви сполукам:
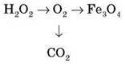
1. 
20. Виведіть молекулярну формулу речовини, масова частка Натрію в якій 83,13 %, Нітрогену — 16,87 %, відносна молекулярна маса сполуки — 83.
VІ. Домашнє завдання.
Підготувати навчальний проект «З історії відкриття періодичної системи хімічних елементів».
-
-
Алла Анатоліївна, чи можна попросити у Вас відповіді на питання? Дякую.


про публікацію авторської розробки
Додати розробку
