Урок Фізика 7 клас "Агрегатні стани речовини "
Терентьєва Оксана Петрівна
План-конспект уроку
Фізика 7 клас Агрегатні стани речовини
Тема: Агрегатні стани речовини
Мета:
• сформувати уявлення про агрегатні стани речовини
• порівняти фізичні властивості тіл у різних агрегатних станах
• ознайомити з кристалічними й аморфними тілами
• розвивати логічне мислення, спостережливість
Тип уроку: формування нових знань та вмінь.
I. Організаційний момент
II. Актуалізація опорних знань, перевірка домашнього завдання
Робота в групах:
- Що таке явище дифузії? (Взаємне проникнення частинок однієї речовини в іншу)
-
В яких речовинах явище дифузії відбувається повільніше? (де густина більша. Таким чином, густина
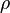 для цього випадку запишеться як:
для цього випадку запишеться як:
![]()
- Чому ми не відчуваємо ударів молекул повітря? (маси молекул надзвичайно малі, а їхні удари - дуже часті, «барабанний дріб» швидких ударів крихітних молекул виявляє себе як остійний тиск повітря)
- Яку природу має взаємодія молекул? (на дуже малих відстанях молекули відштовхуються, а на трохи більших – притягуються)
III. Вивчення нового матеріалу
Агрегатні стани речовин
— В яких агрегатних станах може перебувати речовина?
Кожному учневі на долоню покласти шматок льоду, а під долоню поставити склянку, щоб вода, розтанувши, була зібрана в склянку.
— У вас на долоні вода, що перебуває у твердому стані. Що з нею відбувається?
Учитель демонструє процес випаровування води за допомогою власного кубика льоду та її конденсацію на склі, пояснює відмінності між фазами — агрегатними станами.
— Таким чином, запишемо:

Ви вже знаєте, що вода і лід (сніг, іній) — це два різні агрегатні стани води: рідкий і твердий. Поява інею на деревах пояснюється просто: вода з поверхні річки випаровується, перетворюючись на водяну пару. Водяна пара, у. свою чергу, конденсується й осідає у вигляді інею. Водяна пара — це третій стан води — газоподібний.
Наведемо ще один приклад. Ви, безперечно, знаєте про небезпеку розбити медичний термометр: у ньому міститься ртуть — густа рідина сріблястого кольору, яка, випаровуючись, утворює дуже отруйну пару. А от за температури, нижчої від -39 °С, ртуть перетворюється на твердий метал. Таким чином, ртуть, як і вода, може перебувати у твердому, рідкому й газоподібному станах.
Практично будь-яка речовина залежно від фізичних умов може перебувати в трьох агрегатних станах: твердому, рідкому й газоподібному.
Водяна пара, вода, лід — це три агрегатні стани тієї самої речовини, утвореної однаковими молекулами — молекулами води. Чому ж фізичні властивості речовин, які утворені однаковими молекулами, але перебувають у різних агрегатних станах, відрізняються одна від одної? Імовірно, причина такої відмінності полягає в тому, що молекули по-різному рухаються та взаємодіють?
Пропоную розглянути малюнок, на основі якого пояснюю, що молекули по-різному взаємодіють і рухаються в різних агрегатних станах тому, що змінюється відстань між ними, та хімічний склад залишається при цьому незмінним.
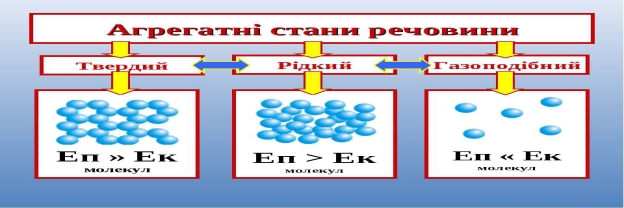
Далі учні повинні усвідомити властивості речовин різних агрегатних станів. Це питання я розкриваю , систематизуючи дані в таблицю.
|
Властивості речовини |
Стани речовини |
||
|
Твердий |
Рідкий |
Газоподібний |
|
|
Форма |
Зберігає |
Не зберігає |
Не зберігає |
|
Об’єм |
Зберігає |
Зберігає |
Займає весь об’єм |
|
Розташування |
Відстані між молекулами приблизно дорівнюють розміру молекул, порядок у розташуванні |
Відстані між молекулами приблизно дорівнюють розміру молекул, порядок відсутній |
Відстані між молекулами набагато більші від розміру молекул |
|
Стиснення |
Майже неможливе |
Майже неможливе |
Досить легко стиснути |
|
Рух |
Коливання |
Коливання, інколи “стрибки” |
Літають по всьому об’єму, інколи зазнають зіткнень |
|
Взаємодія |
Сильна |
Сильна |
Під час зіткнень слабо притягаються і слабо відштовхуються |
Зміни агрегатного стану, їх суть - це процеси, називані фазовими переходами. Виділяють наступні їхні різновиди: із твердого в рідке - плавлення; з рідкого в газоподібне - випар і кипіння; із твердого в газоподібне – сублімація відбувається практично при любій мінусовій температурі та сухому повітрі (кристалики йоду, нафталіну, «сухого» льоду); з газоподібного в рідке або тверде – конденсація.
Цікаво знати
- Метали можна розплавити (перетворити на рідину). Це відбувається при температурі в сотні і навіть тисячі градусів. Для плавлення вольфраму (електричні лампи) потрібно 3000 С. Але під час роботи електричної лампи вольфрам потроху випаровується, тобто існує всередині лампи в газоподібному стані.
- Якщо сильно охолодити кисень або азот, з яких в основному складається повітря, можна перетворити їх на рідину і навіть на тверде тіло.
- Будь яка речовина, нагріта до досить високої температури переходить у стан плазми.
Плазма – четвертий стан речовини:
- У плазмі електрони відірвалися від атомів і набули цілковитої волі руху. Втративши частину своїх електронів, атоми й молекули набувають позитивного електронного заряду; після цього вони називаються іонами.
- Плазма – це газ, що складається з позитивно й негативно заряджених частинок у таких пропорціях, що загальний заряд дорівнює нулю.
- Електрони, що вільно рухаються, можуть переносити електричний струм. Тому інакше говорять, що плазма – це провідний газ.
- В наших земних умовах стан плазми рідкісний і незвичайний. У Сонячній системі із плазми складається Сонце. Верхні шари земної атмосфери іонізовані випромінюванням Сонця, тобто теж складаються із плазми. Цю верхню атмосферу називають іоносферою (від неї залежить можливість далекого радіозв’язку).
У твердому стані залежно від взаємного розташування атомів і молекул фізичні тіла класифікуються на:
1. Кристалічні речовини:
• У твердому стані молекули й атоми більшої частини речовин розташовані в чітко визначеному порядку (утворюють кристалічні гратки). Такі речовини називаються кристалічними.
• Порядок розташування молекул (атомів) у гратках речовини визначає її фізичні властивості.
• Кристалічні тіла плавляться за певної температури.
• Приклади: алмаз, лід, кухонна сіль, цукор.
2. Аморфні тіла:
• Тверді речовини, молекули (атоми) яких не утворюють кристалічних граток і в цілому розташовані безладно, називаються аморфними.
• Аморфні тіла не мають певної температури плавлення, тобто при збільшенні температури вони переходять у рідкий стан поступово.
• Притаманні пружна та пластична деформації
• Приклади: смола, скло, пластмаси, віск, бурштин.
IV. Закріплення нових знань
1. Практикум
• У дві склянки води обережно налити дві-три краплі чорнил. Перша склянка повинна бути з холодною водою, друга — з гарячою. Результати спостережень за швидкістю процесів записати та замалювати в зошитах. Пояснити результати досліду, зробити висновок про вплив температури на дифузію.
2. Бесіда
Поміркуємо разом:
Назвіть речовину, яку часто можна спостерігати в трьох різних агрегатних станах (за звичних для нас умов).
Чи можна стверджувати, що ртуть – завжди рідина, а повітря – завжди газ ?
Чи відрізняються одна від одної молекули водяної пари і льоду?
Чому тверді тіла зберігають об*єм і форму?
У чому подібність і в чому відмінність кристалічних і аморфних речовин?
Як рухаються молекули в рідинах?
Чому гази займають весь наданий об*єм?
Цікаві завдання «Перевір себе»
• З підвищенням температури швидкість руху молекул:
- зростає;
- не змінюється;
- зменшується.
• У якої речовини за кімнатної температури притягання між молекулами найсильніше?
- вода.
- водень.
- алюміній.
• Молекули льоду, води і водяної пари:
- не відрізняються;
- не дуже відрізняються;
- дуже відрізняються;
• Які з указаних властивостей належать твердим тілам, рідким або газоподібним?
- Важко змінити форму;
- Важко стиснути;
- Займають весь наданий об’єм;
- Легко змінюють форму;
- Не мають власної форми;
- Відстані між молекулами приблизно дорівнюють розмірам молекул;
- Легко стиснути;
- Сильна взаємодія між молекулами.
• Знайти відповідні до змісту слова.
а) всі тіла складаються з а) Менделєєв
б) молекули однієї і тієї самої б) однакові
речовини в) молекул і атомів
в) вчений, який систематизував
хімічні елементи
• Розмістити речовини за їх станом за звичайних умов (тверді речовини, рідини чи гази:
а) кисень; б) молоко; в) цукор; г) залізо; д) ртуть;
е) повітря; є) спирт; ж) алюміній; з) азот; и) скло;
і) цегла; к) бензин; л) мідь; м) дерево.
V. Підсумок уроку
Підсумуємо вивчене
• Практично будь-яка речовина залежно від фізичних умов може існувати в трьох агрегатних станах: твердому, рідкому й газоподібному.
• Фазові переходи агрегатних станів: плавлення; випар і кипіння; сублімація; конденсація.
• Коли речовина переходить з одного стану в інший, змінюється взаємне розташування молекул і характер їхнього руху, однак склад молекул (хімічний склад речовини) залишається незмінним.
VІ. Домашнє завдання
Прочитати теоретичний матеріал за підручником;
вивчити матеріал за конспектом;
опрацювати запитання та завдання для самоперевірки.
1


про публікацію авторської розробки
Додати розробку
