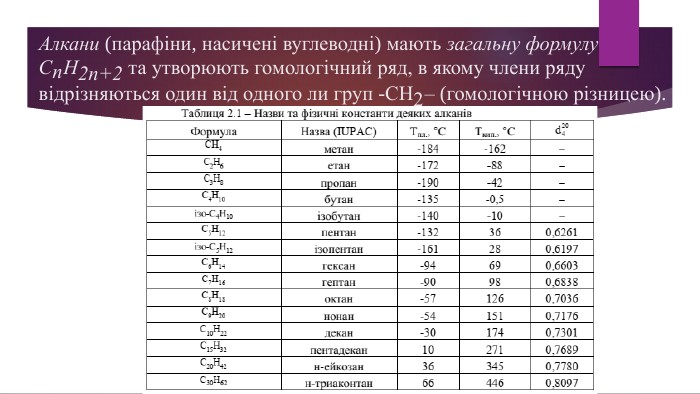
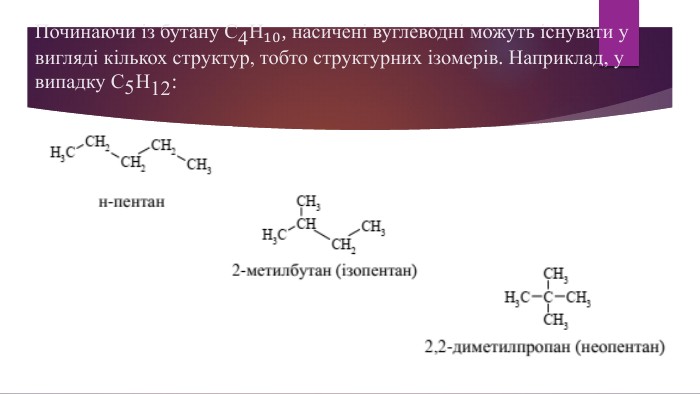
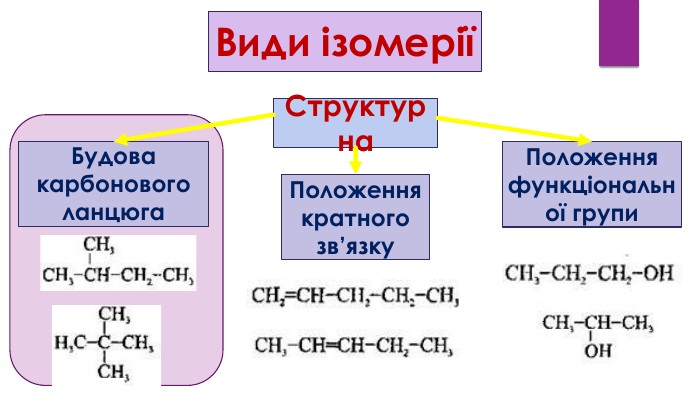
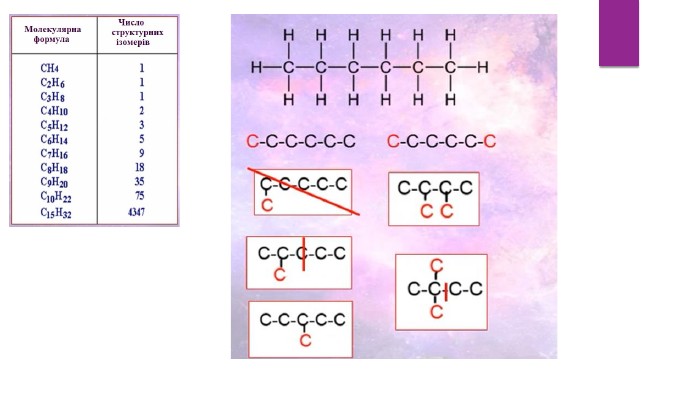
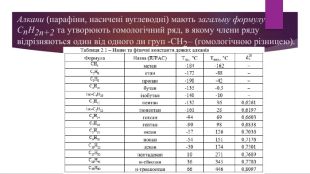
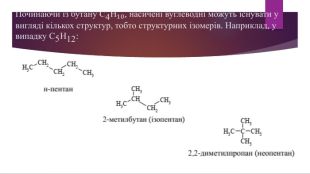
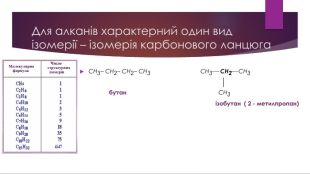
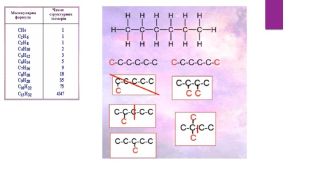
Алкани. Загальна формула алканів, структурна ізомерія, систематична номенклатура. Презентація
Про матеріал
Презентація до теми "Алкани. Загальна формула алканів, структурна ізомерія, систематична номенклатура. " Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку