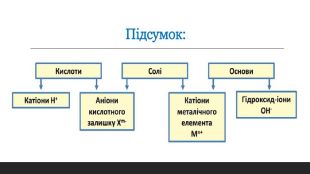
Електролітична дисоціація кислот, основ та солей у водних розчинах
Про матеріал
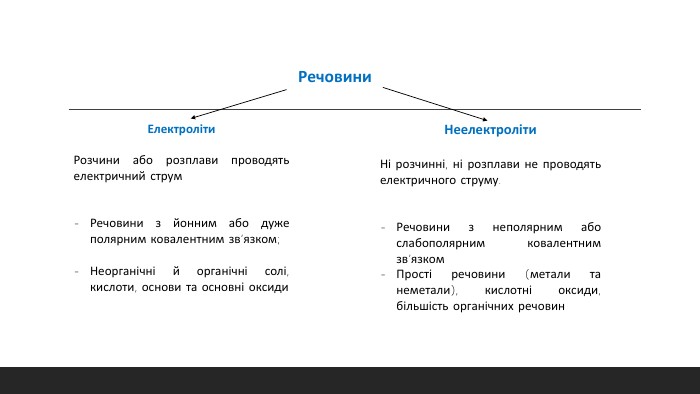
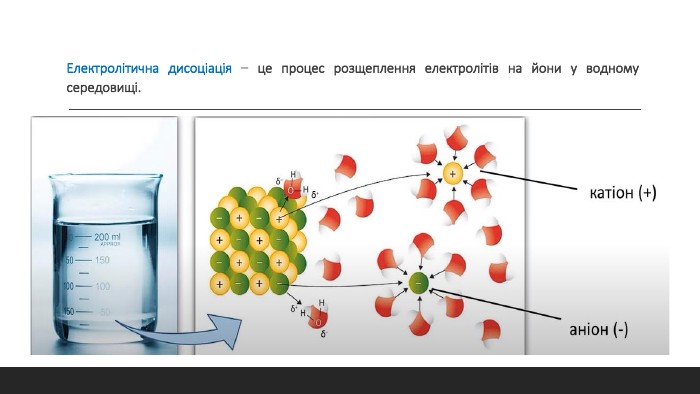
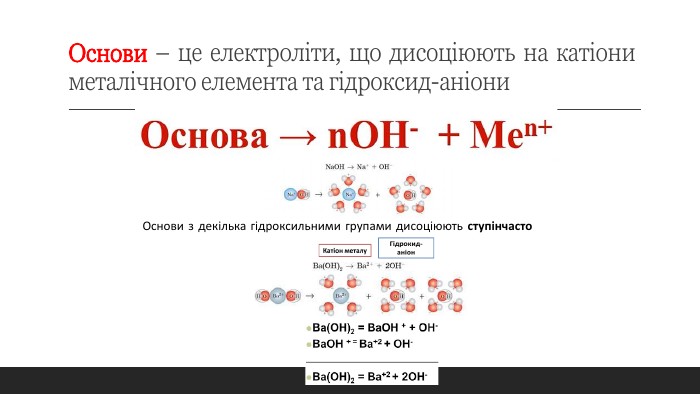
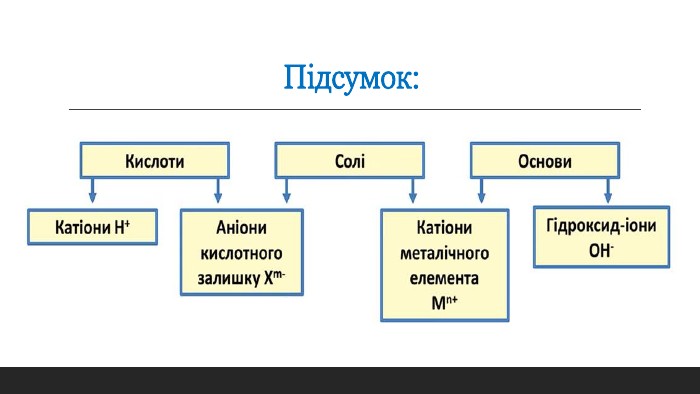
Електролітична дисоціація кислот, основ та солей у водних розчинах. Кислоти, як електроліти. Основи, як електроліти. Солі, як електроліти. Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку