Конспект уроку "Атомне ядро. Протонно-нейтронна модель атомного ядра. Нуклони. Ядерні сили і їхні особливості"
Урок 51 Атомне ядро. Протонно-нейтронна модель атомного ядра. Нуклони. Ядерні сили і їхні особливості
Мета уроку:
Навчальна: Ознайомлення учнів з моделлю ядра атома й з історією відкриття протона і нейтрона.
Розвивальна. Розвивати творчий підхід до навчання як засіб виховання стійкого інтересу до предмета.
Виховна. Виховувати уважність, зібраність, спостережливість.
Тип уроку: урок засвоєння нових знань.
Наочність і обладнання: навчальна презентація, комп’ютер, підручник.
Хід уроку
І. ОРГАНІЗАЦІЙНИЙ ЕТАП
II. АКТУАЛІЗАЦІЯ ОПОРНИХ ЗНАНЬ ТА ВМІНЬ
- Що називають лінійчастим спектром випромінювання?
- Що називають лінійчастим спектром поглинання?
- Назвіть характерні риси спектрального випромінювання молекул.
- Який внесок зробив І.П. Пулюй у дослідження та використання рентгенівського випромінювання?
- Як за допомогою вимірювання атомних та рентгенівських спектрів можна одержати інформацію про елементний склад речовини?
IІІ. ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
- Будова атома та його складники
Протони і нейтрони, маса кожного з яких приблизно 1800 разів більша за масу електрона, утворюють важке позитивне ядро дуже малих розмірів (![]() ). Протони і нейтрони, які разом називають нуклонами, утримуються всередині ядра ядерними силами притягання.
). Протони і нейтрони, які разом називають нуклонами, утримуються всередині ядра ядерними силами притягання.
Зверніть увагу! Між нуклонами немає сил відштовхування.
Різні типи атомних ядер відрізняються один від одного кількістю протонів і нейтронів, що в них містяться. Сумарну кількість нуклонів в атомі називають масовим (нуклонним) числом і позначають символом А. Маса атома зі знаною точністю збігається з масою ядра, оскільки маса електрона набагато менша за масу нуклона.
Кількість протонів у ядрі називають протонним (зарядовим) числом і позначають символом Z. Протонне число легко визначити, скориставшись Періодичною системою хімічних елементів Д. І. Менделєєва. Порядковий номер елемента в періодичній таблиці відповідає кількості протонів у його ядрі.
Щоб визначити кількість нейтронів N
![]()
Для позначення ядра атома хімічного елемента перед символом елемента вгорі вказують нуклонне число А, а внизу – протонне число Z.
Однією з основних характеристик атомного ядра – електричний заряд. До складу атома входить протон – ядра атомів найлегшого ізотопу Гідрогену. Відкриття наявності ще однієї частинки, яка входить до складу атома, було відкрито набагато пізніше, через 12 років. Цією частинкою виявився нейтрон – виявив Резерфорд при проведенні досліду з вивчення властивостей випромінювання, що виникає внаслідок опромінення Берилію ![]() - частинками.
- частинками.
Ізотопи – атоми того самого хімічного елемента, ядра яких містять однакове число протонів, але різну кількість нейтронів.
- Ядерні сили
Ядерні сили є найбільш потужними серед чотирьох відомих на сьогодні взаємодій: гравітаційної, слабкої, електромагнітної та сильної.
Основні властивості
- Коткотривалі сили
- Дуже потужні
- Є силами притягання
- Діють між будь-якими нуклонами
- Властивість насичення – полягає в тому, що нуклон виявляється здатним до ядерної взаємодії одночасно лише з невеликою кількістю нуклонів сусідів.
ІV. ЗАКРІПЛЕННЯ НОВИХ ЗНАНЬ І ВМІНЬ
- У скільки разів приблизно розмір атома більший від розміру атомного ядра?
- У ядрі якого атома нема нейтронів?
- Як охарактеризувати міцність ядер?
- Як за допомогою періодичної системи елементів Менделєєва визначити кількість протонів і нейтронів у певному елементі?
-
Яке припущення (щодо сполуки ядер) дозволяли зробити результати дослідів із взаємодії
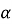 - частинок з ядром атомів різних елементів?
- частинок з ядром атомів різних елементів?
- У ядрі атома хімічного елемента 22 протони і 26 нейтронів. Назвіть цей елемент.
-
Скільки нуклонів у ядрі атома
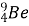 ? Скільки в ньому протонів? нейтронів?
? Скільки в ньому протонів? нейтронів?
V. ПІДБИТТЯ ПІДСУМКІВ УРОКУ
Бесіда за питаннями
- Як охарактеризувати міцність ядер?
- Які частинки входять до складу атома?
- Як за допомогою Періодичної системи хімічних елементів Д.І. Менделєєва визначити кількість протонів і нейтронів у певному елементі?
- Які ізотопи має Оксиген?
VI. Домашнє завдання
Опрацювати § 53,54, Вправа № 26 (2, 3)


про публікацію авторської розробки
Додати розробку
