Масова частка елементів у речовині
Тема. Масова частка елементів у речовині
Цілі: закріпити знання про хімічні формули й уміння обчислювати відносну молекулярну масу; розширити знання про частки з математики для обчислення масової частки елемента в складі речовини; навчити обчислювати масову частку - елемента в складі складних речовин, використовувати поняття «масова частка» для розв'язання задач на визначення хімічних формул.
Тип уроку: поглиблення знань, формування практичних умінь і навичок.
Форми роботи: фронтальне опитування, самостійна робота, евристична бесіда.
Обладнання: періодична система хімічних елементів.
ХІД УРОКУ
I. Організація класу
II. Фронтальне опитування, перевірка домашнього завдання
На які два класи поділяються речовини за складом?
- Які речовини називаються простими?
- Які речовини називаються складними?
- Що таке хімічна формула?
- Що виражає хімічна формула?
- Що таке відносна атомна маса?
- Що таке відносна молекулярна маса?
- Як, знаючи формулу речовини, обчислити відносну молекулярну масу? Перевірка домашнього завдання:
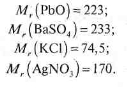
III. Актуалізація опорних знань
• Чи можна стверджувати, що маси кожного атома в молекулі речовини однакові?
(Ні, тому що в усіх елементів різні атомні маси)
• Співвідношення мас атомів у складі молекули складної речовини постійне чи змінне?
(Постійне, тому що постійним є склад речовини)
• Як обчислити співвідношення мас атомів у молекулі?
Розгляньмо на прикладі бінарних сполук.
![]()
Отже, співвідношення мас атомів можна виразити невеликими додатними цілими числами.
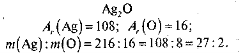
Це співвідношення постійне. Обчислимо співвідношення атомів у молекулі KNO3.
![]()
• Як можна виразити склад речовини у відсотках?
(Якщо прийняти відносну молекулярну масу речовини за 100 %, то маса кожного елемента може бути виражена як масова частка цього елемента в складі молекули) Наприклад:
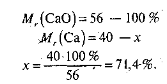
Виражена у відсотках, ця величина є масовою часткою елемента в складі речовини (ώ).
IV. Формування практичних знань і навичок
![]()
де п — число атомів елемента в молекулі; Ar — відносна атомна маса елемента; Мr -— відносна молекулярна маса. Наприклад: Nа2O.
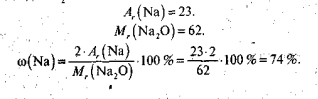
Розв'яжемо наступні задачі. (Біля дошки працює учень.)
Завдання І. Обчисліть масові частки елементів у молекулі вуглекислого газу С02.
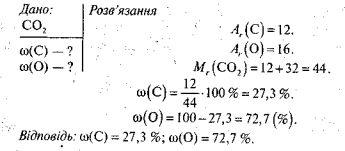
Завдання 2. Самостійна робота з навчальною таблицею 1 до уроку 10 з перевіркою і коригуванням результатів.
- Обчисліть масові частки елементів у складних речовинах з ряду 12 у навчальній таблиці:
![]()
Після закінчення роботи на дошці виписуємо всі отримані учнями результати, визначаємося з помилками і коригуємо.
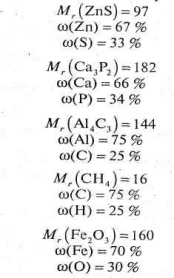
V. Узагальнення і підбиття підсумків
Оцінюємо роботу учнів, виставляємо оцінки.
VI. Домашнє завдання
Прочитати параграф, відповісти на запитання. Обчислити масові співвідношення елементів і масові частки елементів у молекулах: MgCl, NaBr, PH3, CrO3


про публікацію авторської розробки
Додати розробку
