Методична розробка на тему: "Неорганічні речовини"
Міністерство охорони здоров´я України
Комунальний вищий навчальний заклад
І рівня акредитації Полтавської обласної ради
«Лубенське медичне училище»
НЕОРГАНІЧНІ РЕЧОВИНИ
Методичну розробку
теоретичного заняття
з дисципліни «Біологія»
підготувала викладач
Сухенко Т.А.
м. Лубни
Тема: Неорганічні речовини
Навчальні цілі заняття
Фахові компетентності: студент повинен знати про хімічний склад живих організмів;
роль води у клітині; значення мінеральних солей для клітини і організму;
вміти визначати біологічне значення неорганічних сполук як компонентів
живих організмів; з’ясувати біологічний вплив хімічних елементів на
організм; дати визначення - оксиди, луги, мінеральні солі;
складати короткі повідомлення з теми, виконувати випереджаючі
завдання.
Загальні компетентності: студент повинен пояснювати роль води та інших
мінеральних речовин; розпізнавати групи хімічних
елементів; застосовувати знання на практиці; аналітично та творчо
ставитися до роботи, яку виконує; вміти працювати самостійно і в
команді, порівнювати та робити відповідні висновки, розвивати увагу,
пам’ять, навички спілкування, активність, креативність;
виховувати бережливе ставлення до живих організмів та до води, як основної
рідини нашої планети.
Обладнання та матеріали: інтерактивна дошка, підручники, періодична таблиця
хімічних елементів, презентація по темі.
Концепція уроку: показати практичне значення неорганічних сполук і їх біологічну
роль; звернути увагу на єдність хімічного складу живої і неживої
природи; відзначити, що співвідношення елементів в живих і неживих
об’єктах різне; розповісти про проблеми, пов’язані з порушенням вмісту
елементів в організмах.
Методи і методичні прийоми:
1. Інформаційно- рецептивний:
а) словесний: розповідь, пояснення, опис, бесіда, робота з підручником та м/м дошкою.
б) наочний: ілюстрація, демонстрація, ТЗН.
Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення, одержання з тексту та ілюстрацій нових знань, робота з роздатковим матеріалом.
2. Репродуктивний.
Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань.
3. Проблемно- пошуковий: постановка проблемного питання.
Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активіза-ція уваги та мислення.
4. Візуальний: складання схем.
5. Релаксопедичний: психологічне розвантаження.
Базові поняття і терміни: елементарний склад, органогенні елементи, макроелементи,
мікроелементи, ультрамікроелементи, оксиди, неорганічні кислоти, луги,
мінеральні солі, вода, мінеральні солі, гідрофільність, гідрофобність, буферні
системи, кислотно-лужний баланс.
Міжпредметні зв'язки: хімія, фізика, географія, математика, біохімія, латинська
мова, анатомія і фізіологія людини.
Тип заняття: засвоєння нових знань.
Місце заняття в навчальній програмі: поточний.
Структура заняття
І. Організаційний етап.... …………………………………………………… 2 хв
II. Актуалізація опорних знань і мотивація навчально-пізнавальної діяльності 5-7 хв
IIІ. Вивчення нового матеріалу……………………………………….. ………45-50 хв
IV. Узагальнення, систематизація та контроль знань і вмінь студентів ....... 20 хв
V. Самостійна робота студентів................................................... 2-3хв
VІ. Підведення підсумків заняття та оцінювання студентів …………….. …. 5 хв
VІІ. Надання та пояснення домашнього завдання………………………….. 3 хв
Хід заняття
І. Організаційний етап
Викладач вітається, перевіряє готовність до заняття, створює робочий настрій.
ІІ. Актуалізація опорних знань і мотивація навчально-пізнавальної діяльності
Методом бесіди з’ясувати знання студентів про живу та неживу природу, склад повітря, основні властивості живого, рівні організації, що таке життя?
Доведіть:
- на основі чого відбувається єдність живої і неживої природи.
- чи існує єдність хімічного складу організмів.
Проблемні запитання.
- Чому вода має першочергове значення у клітинах живих організмів?
- Чи можлива нормальна життєдіяльність організму без мінеральних солей?
- Чи залежить кількість води та мінеральних солей від вікових категорій людей?
Необхідно підвести студентів до розуміння того, що кожний хімічний елемент у складі живих організмів має своє призначення, тому при порушенні вмісту елементів в організмі людини, тварин і рослин, виникають певні проблеми, які в свою чергу призводять до негативних наслідків.
Повідомити тему, мету та план заняття. Записати в зошиті.
Тема: Неорганічні речовини
Мета заняття: ознайомитися з неорганічними речовинами та елементарним
складом організмів.
План заняття:
- Елементарний склад організмів.
- Класифікація хімічних елементів за їх кількістю в організмах: макроелементи, мікроелементи.
- Роль неорганічних речовин (води, кисню, мінеральних солей) у життєдіяльності організмів.
Поставити проблемне запитання, відповідь на яке повинна бути до кінця заняття:
«Як розпізнати речовини, якщо їх так багато в природі?»
Б.Шоу: «Єдиний шлях, що веде до знань – це діяльність».
III. Вивчення нового матеріалу
Розповідь викладача з елементами бесіди
Живі і неживі тіла планети побудовані з одних і тих же хімічних елементів. Але в живій природі ці елементи характеризуються складністю хімічних сполук. Це зумовлено певною упорядкованістю їх на молекулярному рівні, тобто відмінності між хімічним складом органічного і неорганічного світу виявляється уже на молекулярному рівні.
Біохімія – наука, яка вивчає хімічний склад живих форм, хімічні процеси, хімічні закономірності.
За дослідженнями біохіміка В.О.Енгельгардта «глибока корінна відміна живого від неживого полягає у здатності живого створювати порядок із хаотичного теплового руху молекул».
Хімічні елементи живих організмів створюють два класи сполук – неорганічні і органічні.
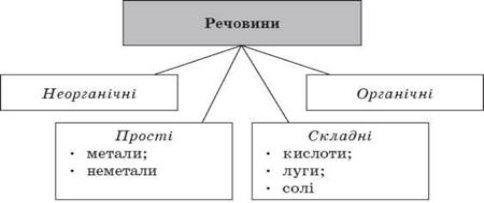
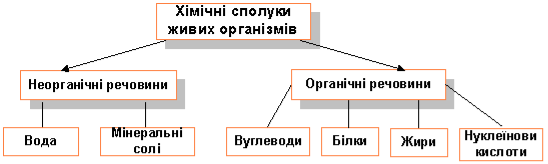
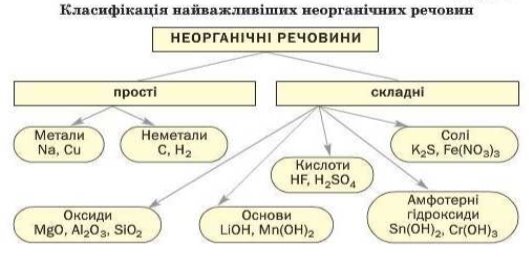
Із відомих хімічних елементів до складу клітин входить понад 80. Елементів, які були б властиві лише живим організмам, у природі не знайдено. Близько 30 елементів наявні в клітинах постійно, а понад 5 потрапляють водою, їжею, вдихаються.
Всі елементи, що входять до складу клітин організмів поділяють на групи: (занотувати)
1. Органогенні – оксисен, нітроген, гідроген, карбон.
2. Макроелементи – кількість їх становить від 0,1% до 0,01 %.
3. Мікроелементи – містяться в кількостях від 0,001% до 0,000001%.
4. Ультрамікроелементи – ті, концентрація яких не перевищує 0, 000001%.
Хімічні елементи, які входять до складу клітин і виконують біологічні функції називають біогенними.
Всі живі організми відрізняються від навколишньої неорганічної природи за кількісним складом хімічних елементів. Хімічні елементи беруть участь у побудові організму у вигляді іонів.
Співвідношення елементів в живих і неживих об’єктах є різним. Якщо в неживих об’єктах на нашій планеті за кількістю атомів найбільш поширеними є О(63 %), Si(21,2 %), Аl(6,5 %), Na(2,4 %), Fe(1,9 %) і Са(1,9 %), то в живих перші місця за вмістом займають Н(64 %), О(25,6 %), С(7,5 %), N(1,25 %), Р(0,24%), S(0,06 %).
Така відмінність обумовлена певними особливостями елементів, які переважають у живих об’єктах. Це прямо пов’язано з їхніми хімічними й фізичними властивостями. Так, Оксиген і Гідроген утворюють воду, що є універсальним розчинником і середовищем, у якому відбуваються біохімічні реакції. Наявність Нітрогену вкрай важлива для утворення найважливіших інформаційних молекул — ДНК і РНК. Фосфор бере участь в утворенні макроергічних зв’язків, тобто є найважливішим компонентом систем забезпечення клітин енергією. А Сульфур відіграє важливу роль у формуванні просторової будови біологічних молекул.
Якщо ж узяти, наприклад, Силіцій, якого надзвичайно багато на нашій планеті, то він, як і Карбон, здатен зв’язуватись із чотирма іншими атомами, але, через більший діаметр свого атома, він гірше утворює макромолекулярні ланцюжки.
Органогенні елементи (занотувати) – це перша група хімічних елементів живих організмів (оксисен, нітроген, гідроген, карбон).
Подібність елементарного хімічного складу клітин всіх організмів свідчить про єдність живої природи. Разом з тим немає природного хімічного елементу, живих організмів, які б не зустрічалися в тілах живої природи. Цим підтверджується спільність живої і неживої природи.
Найбільший відсотковий вміст у клітині складають 4 елементи:
- оксиген(65-70%),
- гідроген(8-10%),
- карбон(15-18%),
- нітроген (2-3%).
Це так звані органогенні елементи.
Оксиген (кисень) – найпоширеніший хімічний елемент на Землі. Масова частка його в оболонці Землі (атмосфера, гідросфера, літосфера) становить приблизно 52%. У вільному стані, тобто як проста речовина, кисень є в повітрі (21%, міститься в природних водах. Біохімічне самоочищення річкової і морської води відбувається з використанням розчиненого у воді О2. Зв‘язаний (тобто як хімічний елемент) кисень входить до складу води, піску, глини, гірських порід і мінералів, а також до складу живих організмів (в організмі людини міститься (65% кисню) .
Гідроген (водень) - у міжзоряному просторі атоми водню трапляються в кілька сотень разів частіше, ніж атоми всіх інших елементів разом узяті. Значення водню у Всесвіті винятково велике. Він відіграє роль “космічного палива”, що дає енергію зіркам, у тому числі й Сонцю. На Землі водень трапляється в основному в хімічно зв‘язаному вигляді. Він входить до складу води, органічних речовин, з яких складаються всі живі організми, а також до складу нафти, вугілля, багатьох мінералів природного газу. В організмі людини міститься біля 10% водню. У вільному стані водень на землі трапляється лише у вулканічних газах. Вільний водень міститься в горючих газах, що виділяються з землі. Він утворюється при гнитті і бродінні органічних речовин і тому міститься в шлункових газах людини і тварин. Вміст водню у гідросфері та літосфері Землі становить 1% за масою.
Карбон (вуглець) – хімічний елемент головної підгрупи 4 групи періодичної системи Д.І. Менделєєва, важливий біологічний елемент, що стоїть в основі всього живого і підтримує його життєдіяльність. Із атомів вуглецю складається скелет молекул білків, вуглеводів, нуклеїнових кислот, ліпідів, вітамінів, гормонів різних матеріалів та ін. Джерелом вуглецю на Землі служить метан і ціанистий водень (синильна кислота) первинної атмосфери. З виникненням життя єдиними джерелом вуглецю для утворення органічної речовини біосфери являється вуглекислий газ біосфери. В залежності від хімічних форм вуглець використовується живими організмами, останні ділять на автотрофні і гетеротрофні.Зелені рослини здійснюють фотосинтез – утворення із атмосферного вуглекислого газу органічних речовин завдяки проненевій енергії Сонця.
Використання в медицині. В медицині вуглець використовується під назвою “вугілля активоване”, чи карбоген, використовують при диспепсії, метеоризмі, харчових та інших отруєннях в якості лікарського засобу. Сполуки елементарного вуглецю, наприклад, його діоксид, використовують в анестезіології та ін галузях медицини.
Нітроген (азот) – хімічний елемент п‘ятої групи періодичної системи Менделєєва.
Загальний вміст азоту в земній корі складає біля 0,016%. Основна його маса знаходиться в повітрі у вільному вигляді. В окремих кількостях вільний азот знаходиться в розчиненому стані у водах океанів. Життя нерозривно пов‘язане із властивостями азотистих речовин – білків. В склад білків в середньому входить 15-17% азоту. При відмиранні організмів вони в процесі кругообігу перетворюються в більш прості сполуки: аміак, амонійні солі, нітрити і нітрати.
Основна маса вільного азоту використовується в промисловості для синтезу аміаку, ціанаміду кальцію і азотної кислоти, які являються вихідними речовинами для одержання азотних добрив. Аміак (сполука азоту і водню) застосовують для виробництва азотної кислоти і азотних добрив. Його використовують для добування аміачної води (розчин аміаку у воді), яку застосовують у с/г (як добриво), в медицині і в повсякденному житті. Аміачну воду іноді називають гідрооксидом амонію, а в побуті – нашатирним спиртом.
2. Наступну групу складають макроелементи – фосфор, калій, сірка, хлор, кальцій, залізо, сумарна частка яких становить до 1,9%.
Інші хімічні елементи (понад 50) належать до мікроелементів (йод, кобальт, марганець, мідь, молібден, цинк).
Ще менше в клітині ультрамікроелементів (свинцю, брому, срібла, золота тощо).
Розповідаючи про вміст у клітині макроелементів, викладач пропонує студентам заповнити таблицю в зошитах. Таблицю можна подати на екрані або намалювати на дошці.
Вміст у клітині та значення для організму макроелементів.
|
Елемент |
Вміст маси клітин, % |
Значення |
|
Фосфор (Р) |
0,2-1,0 |
Входить до складу кісток, білків, нуклеїнових кислот, АТФ. |
|
Калій (К) |
0,15-0,4 |
Основний позитивно заряджений іон в організмі. |
|
Сірка (сульфур, S) |
0,15-0,2 |
Входить до складу білків та інших біомолекул |
|
Хлор (Cl) |
0,05-0,1 |
Негативно заряджений іон в організмі |
|
Кальцій (Са) |
0,04-2,0 |
Основний компонент кісток і черепашок, бере участь у реалізації метаболічних процесів. |
|
Магній (Mg) |
0,02-0,03 |
Головний внутрішньо-клітинний позитивно заряджений іон |
|
Залізо (Ферум, Fe) |
0,01-0,015 |
Входить до складу багатьох біомолекул у тому числі гемоглобіну. |
Фосфор (Р).
Входить в склад важливих біогенних сполук: нуклеотидів, нуклеїнових кислот, фосфоліпідів, ряду вітамінів. Бере участь в різних метаболічних процесах і відіграє важливу роль в життєдіяльності всіх живих організмів. Вміст фосфору в крові є одним із важливих показників складу мінерального обміну і одним із основних діагностичних признаків ряду захворювань і патологічних станів, таких як рахіт, спазмофілія, гіпопаратиреоз, гіперпаратериоз, синдром Лейвуда-Олбрайта.
В тілі людини знаходиться приблизно 1% фосфору, але в переносі на суху вагу – 2,5%. Приблизно 80-87% всього фосфору, який є в організмі людини, знаходиться в скелеті, близько 0,2% - в крові.
В живих організмах фосфор п‘ятивалентний і входить головним чином в склад фосфатів і в меншій степені – в склад піро- і полі фосфатів.
Велика кількість фосфору міститься в апатиті (фтор фосфаті кальцію) зубів. Розчин фосфору в організмі входить в склад неорганічних речовин (фосфати калію і натрію) і деяких органічних сполук.
Найціннішими джерелами легко засвоюваного фосфору є яйця (особливо жовток), печінка, м‘ясо, молоко, сир, боби, горох.
З точки зору клінічного дослідження важливим є визначення фосфору в крові і сечі в крові розрізняють 2 фракції фосфору: кислотно розчинний фосфор і кислотно нерозчинний.
В медичній практиці препарати фосфору мають органічне призначення. Для практичних цілей використовують препарати, які доставляють в організм фосфор або полегшують його доставку. Інколи достатнім є введення в харчовий режим продуктів з високим вмістом фосфору, наприклад риби.
Серед препаратів фосфору розповсюдженими є аденозинтрифосфорна кислота, фітин, кальцій, гліцерофосфат. Таблетки: “Фітоферролактол”, “Церебро-лецітин”, “Ліпоцеребрин”.
Препарати фосфору в малих дозах посилюють ріст і розвиток кісткової тканини, стимулюють кровообіг, гальмують окисні процеси, беруть участь в обміні речовин.
Калій (К).
Відноситься до основних внутрішньо-клітинних катіонів, бере участь у ряді життєво важливих процесів. Деякі сполуки калію використовують в хімікофармакологічниій промисловості і в медицині.
Солі калію широко використовують в вигляді добрив. В організмі людини вміст калію становить 160-250г. Він міняється в залежності від віку, статі.
В великих кількостях калій знаходиться в рослинних продуктах, особливо в абрикосах, персиках, апельсинах, бананах, ананасах, картоплі, помідорах, капусті, моркві.
Як препарати калію в медицині використовуються органічні (калій ацетат, калій аспоролінат, калій оротат) і неорганічні (калій хлорид), солі калію.
Вони підтримують водний баланс, розподіл води, осматичний тиск, кислотно-лужну рівновагу, збудливість м‘язевої і нервової тканин.
Сірка (сульфур S).
Відноситься до біогенних органічних елементів, постійно входить в склад живих організмів і відіграє важливу роль в обміні речовин.
В медицині сірка використовується як лікарський препарат, а в сільському господарстві – для боротьби з шкідниками і хворобами рослин. У людин і тварин особливо багато сірки міститься в кератині волосся, і шерсті, в тканинах нервової системи, хрящах, кістках.
В організмі людини сірка поступає з їжею. В процесі обміну речовин вона переходить в більш оскислену форму, кінцевими продуктами цього процесу є сульфати, які в печінці знезаражують токсичні продукти метаболізму – феноли. Із організму сірка виводиться з сечею і калом.
До препаратів, які використовуються в медичній практиці відносять лікарські засоби, які містять елементарну сірку, яка сама по собі в фармакологічному відношенні практично неактивна. Однак при взаємодії елементарної сірки з деякими органічними речовинами в організмі утворюються сполуки, які володіють фармакологічним ефектом.
В якості препаратів сірки використовують очищену і осаджену сірку. Для зовнішнього вживання випускають очищену сірку, наприклад сірко-карталанна, пасту сірко-цинко-карталонну.
Хлор (Cl).
Іони хлору беруть участь у регуляції водно сольового обміну в організмі, відіграє важливу роль в процесі транспорту іонів через біологічні мембрани і в утворенні біоелектричних потенціалів.
Газоподібний хлор або хімічні сполуки, які містять хлор в активній формі, використовують для беззараження питної води. Сам хлор і багатохлоровмісні сполуки токсичні.
Добова потреба людини в іонах хлору становить приблизно 215 ммоль. Основним джерелом постування хлору з іжею є харчова сіль. Виділення хлору з організму відбувається з сечею і потом.
В медичній практиці препарати хлору використовують як дезинфікуючі і антисептичні засоби.
В якості таких засобів використовується хлороактивні сполуки і хлоровмісні: хлорну воду, гіпохлориди калію, літію, хлоропрохідні ізоціанорової кислоти і її солі. В якості антисептиків використовують антиформін, алоромін Б, пантоцид, хлорне вапно.
Кальцій (Са).
Володіє високою біологічною активністю, є основним структурним компонентом кісток скелета і зубів тварин і людини, а також важливим компонентом системи згортання крові.
Кальцій є незмінним елементом в харчуванні людини. Сполуки кальцію укріплюють захисні сили організму і підвищують його стійкість до зовнішніх факторів і інфекцій.
Вміст кальцію в організмі дорослої людини становить близько 20г на 1 кг ваги людини. Основна частка знаходиться в кістковій і хрящовій тканинах і в зубах. При його недостатності (тетанія, спазмофілія) препарати кальцію використовують в комбінації з ПТГ, при хронічній недостатності кальцію (рахіт, остеоміляція) – з вітаміном Д.
Недостатність може виникнути при великому його розході (ріст, лактація, вагітність), а також при харчовому розладі з недостатньою кількістю кальцію (картопля, хліб, м‘ясо). В цих умовах препарати кальцію приймаються профілактично або додаються в харчові продукти. В зв‘язку з цим, що кальцій бере участь в обміні речовин в кістковій тканині і зубах, його приймають для покращення зрощення переломів, профілактики карієсу.
Кальцій хлорид, кальцій глюконат, кальцій лактат, кальцій гліцерофосфат.
Магній (Mg).
Магній є одним із важливих біоелементів, служить активатором багатьох ферментативних процесів (регулює реакції фосфорного обміну, гліколізу, багато етапів синтезу білків, жирних кислот і ліпідів, синтез і розпад нуклеїнових кислот); потрібний для нормального функціонування нервової і м‘язевої тканин. Сполуки магнію, а особливо його солі, використовуються в медицині у вигляді лікарських препаратів.
В організмі здорової людини міститься близько 20 г магнію. Половина знаходиться в кістках, 1/3 – в м‘язах, решта – в біологічних рідинах, особливо в крові.
Добова потреба магнію становить приблизно 300 мг і повністю задовольняється за рахунок продуктів харчування.
В залежності від розчинності в воді лікарські препарати магнію ділять на 2 групи: добре розчинні (магній сульфат, магній тіосульфат, магній аскорбінат) і практично нерозчинні (магній карбонат, магній трисилікат).
На ЦНС препарати магнію добре розчинної групи діють пригнічено, викликаючи снодійний, наркотичний і протисудорожний ефект. На серцево-судинну систему препарати магію викликають гіпотензійний ефект. Також зменшують протиударний і хвилинний об‘єм серця, пригнічують дихання, знижують тонус скелетної мускулатури. Ці ефекти проявляються при парантеральному введенні. Препарати магнію практично нерозчинні в воді призначаються в основному для прийому в середину.
Натрій (Na).
Один із основних катіонів живих організмів, необхідних для здійснення життєво важливих функцій. Натрій відіграє важливу роль в іонному балансі внутрішнього середовища живого організму. Впливає на стан м‘язевої і серцево-судинної систем. В тілі людини знаходиться у всіх тканинах, в основному в іонізованих формах.
В медицині використовують хлорид натрію, (поміркуйте для чого) натрію гідрокарбонат.
Залізо (Ферум, Fe).
Входить в склад дихальних пігментів, бере участь в переносі кисню до тканин в організмі тварин і людини, стимулює функцію кровотворних органів. В якості лікарського засобу приймається при анемічних і деяких інших патологічних станах.
Організм дорослої людини містить в середньому 4-5 г феруму, з них близько 70% знаходиться в складі гемоглобіну. Залізо, існуюче в плазмі крові, є транспортною формою заліза, яке зв‘язане з білком трансферином.
Вміст заліза в плазмі крові підпорядкований добовим коливанням – він знижується в другій половині дня, обмін заліза в організмі багато в чому залежить від нормального функціонування печінки.
Покази до приймання заліза є залізодефіцитні анемії різної етіології (анемії від крововтрат, анемії вагітних), які проходять з пониженим вмістом заліза в крові, а також стан латентного безсимптомного дефіциту заліза зустрічається у 20-30% практично здорових жінок.
Препарати заліза можуть бути рекомендовані при довгому внутрішньо судинному гемолізі, супроводжуючому постійною втратою заліза, яке виводиться з сечею, при захворюваннях системи крові, складних кровотеч, з розвитком вторинної недостатності заліза.
Основними джерелами заліза в харчових продуктах є продукти тваринного походження (м‘ясо, риба, печінка).
Серед препаратів заліза найбільше застосування отримали: залізо гліцерофосфат, залізо лактат, ферітал, заліза закисного сульфат, таблетки “Гемостимулін”.
Слово «елемент» має безліч значень. Так, наприклад, називають атоми одного виду, що мають однаковий заряд ядра.
А що таке «мікроелементи»? (занотувати)
Так називають хімічні елементи, які є в тваринних і рослинних організмах, а також в організмі людини у дуже малих кількостях. Їх маса становить від 0,001 до 0,000001 % маси тіла. Вони входять до складу ферментів, гормонів і ряду інших важливих сполук.
Наприклад, титану і алюмінію всього по одній тисячній частині процента — саме їх і можна назвати мікроелементами.
На світанку біохімії на такі дрібниці уваги не звертали. Подумаєш, якісь там соті чи тисячні частини процента. Такі кількості тоді й визначати не вміли. Техніка й методи аналізів удосконалювались, і вчені знаходили все більшу й більшу кількість елементів у живих об'єктах. Проте роль мікроелементів довгий час встановити не вдавалось. Навіть і тепер, незважаючи на те, що хімічний аналіз дає можливість визначати мільйонні і навіть стомільйонні частини процента домішок практично у будь-яких зразках, значення багатьох мікроелементів для життєдіяльності рослин і тварин ще не з'ясовано. Проте дещо сьогодні вже відомо.
Відомо, наприклад, що в різних організмах є такі елементи, як кобальт, бор, мідь, марганець, ванадій, йод, фтор, молібден, цинк і навіть... радій. Так, саме радій, хоч і в дуже малих кількостях. І багато хто з учених додержується тієї думки, що, мабуть, в організмі тварин є мало не всі елементи періодичної системи, і визначення їх вмісту — справа недалекого майбутнього.
Наприклад, йод входить до складу гормонів щитовидної залози, a залізо — до складу гемоглобіну. Деякі з них мають велике значення лише для певних систематичних груп організмів. Так, бурі водорості містять багато йоду, молюски — багато Сu, який входить до складу їх дихальних пігментів, а хвощі — багато Si і Сr, які виконують захисні функції.
Ультрамікроелементи (занотувати)
До цієї групи відносять елементи, маса яких становить менше 0,000001 % маси тіла. Це Уран, Радій, Аргентум, Меркурій, Берилій, Цезій, Селен.
Їх біологічна роль мало досліджена. Скоріше за все, вони потрапляють до організму випадково у вигляді домішок у складі необхідних речовин. Проте в ряді випадків було відмічено їхній вплив на організм. Наприклад, препарати, які містили дуже низькі концентрації Аu, виявили суттєвий профілактичний ефект щодо атеросклерозу.
Додаток
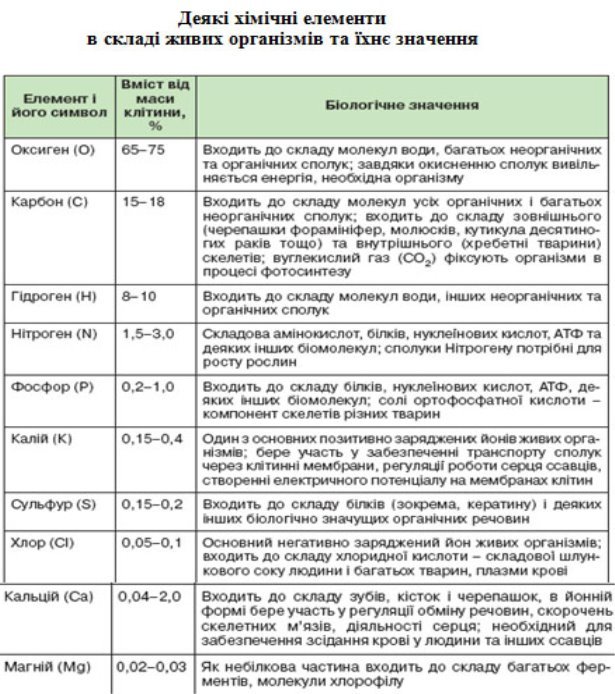
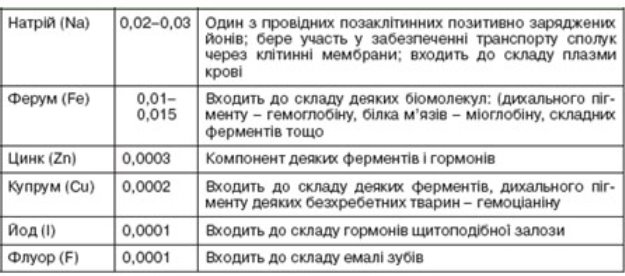
Хімічні елементи живих організмів
|
Хімічні елементи у складі живих організмів |
||
|
Макроелементи |
Мікроелементи |
Ультрамікроелементи |
|
Становлять від 10 до 0,001 % маси тіла |
Становлять від 0,001 до 0,000001 % маси тіла |
Становлять менше 0,000001% маси тіла |
|
С, O, N, P, S, Na, К, Mg, Са, Сl |
Fe, Cu, Zn, Mn, Co, I, Mo, V, Ni, Cr, F, Se, Si, Sn, B, As |
U, Ra, Au, Hg, Se |
Проблеми пов’язані з порушенням умісту елементів.
Порушення вмісту хімічних елементів у живих організмах досить часто призводить до негативних для них наслідків. Причиною негативних наслідків може бути як нестача, так і надлишок елемента. Так, нестача йоду призводить у людини до порушення роботи щитовидної залози, а надлишок важких металів (Hg, Pb, Cu, As тощо) викликає важкі отруєння та порушує роботу печінки й нирок. Нестача Fe у людини викликає анемію, нестача Р підвищує ламкість кісток, а його надлишок викликає ураження нервової системи.
Дефіцит N у рослин пригнічує їхній ріст, викликає пожовтіння й опадання листя та зменшує врожайність. Дефіцит Р також викликає пригнічення росту і зміну забарвлення листків. Різноманітні порушення розвитку рослин і забарвлення їх окремих частин викликає й дефіцит таких елементів, як Fe, Mo, Са, Mg тощо. Надлишок Мn викликає у рослин пожовтіння листків, а надлишок В призводить до відмирання країв листків.
Залізо й марганець відіграють важливу роль у процесі фотосинтезу рослин. Якщо виростити рослину на грунті, в якому немає навіть слідів заліза, то листки й стебла її будуть білі, як папір. Але досить обприскати таку рослину розчином солей заліза, як вона набуває свого природного зеленого забарвлення.
Мідь теж є необхідним елементом у процесі фотосинтезу і впливає на засвоюваність рослинними організмами сполук азоту. При недостатній кількості міді в рослинах дуже слабко утворюються білки, до складу яких входить азот.
Складні органічні сполуки молібдену входять як складові частини в різні ферменти. Саме вони сприяють кращому засвоєнню азоту.
Недостача молібдену часом спричиняється до опіку листків через велике скупчення в них солей азотної кислоти, які, коли немає молібдену, не засвоюються рослинами. Разом з цим молібден впливає на вміст у рослинах фосфору. Коли його немає, не відбувається в рослині перетворення неорганічних фосфатів в органічні.
Недостача молібдену відбивається і на нагромадженні пігментів (барвних речовин) в рослинах — з'являється плямистість і бліде забарвлення листків. Коли немає бору, рослини погано засвоюють фосфор. Бор сприяє також кращому пересуванню по системі рослини різних сахарів.
Мікроелементи відіграють важливу роль не тільки в рослинних, а й у тваринних організмах. Виявилося, що коли в їжі тварин зовсім немає ванадію, тварини втрачають апетит і навіть гинуть, незважаючи на повне забезпечення кормами.
Разом з тим підвищений вміст ванадію у кормі для свиней сприяє тому, що вони швидко ростуть і відкладають товстий шар сала.
Цинк, наприклад, відіграє важливу роль в обміні речовин і входить до складу еритроцитів тварин. Печінка, якщо тварина (і навіть людини) перебуває у збудженому стані, викидає в загальне коло кровообігу марганець, кремній, алюміній, титан і мідь, але при гальмуванні центральної нервової системи — марганець, мідь і титан, а виділення кремнію і алюмінію затримує.
В регулюванні вмісту мікроелементів у крові організму беруть участь, крім печінки, мозок, нирки, легені і м'язи. Встановити роль мікроелементів у процесах росту й розвитку рослин і тварин — важливе і захоплююче завдання хімії і біології. Вивчення цього впливу, безперечно, приведе в недалекому майбутньому до дуже значних результатів. І відкриє науці ще один із шляхів до створення другої природи.
Неогрганічні речовини клітини: оксиди, кислоти, луги.
Складні неорганічні сполуки поділяють на: (занотувати)
- оксиди
- кислоти
- луги
- мінеральні солі
В живих організмах, на відміну від неживих об’єктів, не існує простих речовин. Всі молекули, що входять до живої речовини є сполуками – складними речовинами.
Оксиди – це складні речовини, до складу яких входять 2 елементи, один з яких Оксиген. За складом оксиди поділяють на оксиди металів і оксиди неметалів.
Питання студентам: «Як ви гадаєте, чому оксиди багатьох елементів дуже поширені у природі?»
Наприклад, така добре відома сполука, як звичайний річковий пісок (з деякими домішками) є оксидом з формулою SiO2 – силіцій(IV) оксид (кремнезем). Майже чистим кремнеземом є гірський кришталь. Цей оксид разом з алюміній оксидом Al2O3 входить до складу глин та багатьох інших мінералів. З руд, які містять алюміній оксид Al2O3, виплавляють алюміній. Звичайний наждак – це також алюміній оксид з домішками. Алюміній оксид з невеликим вмістом різних домішок може бути і коштовним каменем (рубін, сапфір). Дуже поширені в природі й оксиди Феруму – це різні залізні руди. Україна має великі запаси залізних руд (Криворізьке та Керченське родовища).
До складу повітря входить карбон(IV) оксид СО2 (вуглекислий газ), об’ємна частка якого в повітрі становить 0,3 %. Однак найпоширенішим оксидом у природі є гідроген оксид Н2О (вода). Вода – джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі. Основні джерела води – моря й океани, річки й озера. Для усіх господарських потреб використовується прісна природна вода після її очищення. Прісної води на Землі мало. Воду потрібно берегти.
Більшість оксидів, а саме оксиди елементів-металів, має немолекулярну будову і дуже високу температуру плавлення. Такі оксиди – тверді речовини. Деякі оксиди (оксиди елементів-неметалів) мають молекулярну будову і за стандартних умов перебувають в рідкому або газуватому стані.
Цікава хвилинка
Цікаво знати, що…
- Всі дорогоцінні камені є різновидами оксидів. Наприклад, рубін – це оксид алюмінію, агат – оксид кремнію, кварц, америст – це різновиди силіцій ІV оксиду, корунд із домішками сполук Титану має інтенсивне синє забарвлення і відомий як сапфір.
- Планета Марс червона завдяки великій кількості оксиду заліза на її поверхні.
- Оксиди входять до складу всіх відомих нам фарб.
- Напевно кожен з вас милувався виробами з кольорового скла. А чи знали ви, що пофарбовані вони за допомогою оксидів? Додавання в скло оксиду заліза робить його кольоровим від блакитного до темно – червоного.
Кислоти – складні речовини, до складу яких входять один, або кілька атомів Гідрогену, здатних заміщуватися на атоми металів, і кислотні залишки.
Важливі функції виконують в організмі і неорганічні кислоти. Так, наприклад, хлоридна кислота створює кисле середовище в шлунку хребетних тварин і людини, забезпечуючи активність ферментів шлункового соку. У людей, в шлунку яких хлоридної кислоти виробляється недостатня кількість, порушуються процеси перетравлення білків, можливе розмноження у шлунку великої кількості шкідливих бактерій тощо. Збільшення секреції хлоридної кислоти також небезпечне для організму людини, зокрема воно спричиняє печію.
Залишки сульфатної кислоти, приєднуючись до нерозчинних у воді сполук, забезпечують їхню розчинність. Це сприяє виведенню таких речовин у розчиненому стані з клітин і організму.
Ортофосфатна кислота необхідна для синтезу АТФ (є універсальним накопичувачем енергії в клітині) та різних типів нуклеїнових кислот.
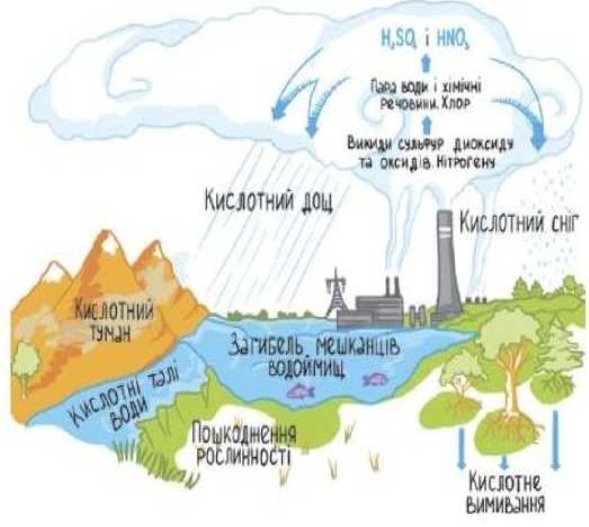
Особливу небезпеку для довкілля становлять кислотні дощі, спричинені забрудненням атмосфери сірчистим газом SO2 (промислові підприємства та автотранспорт викидають в атмосферу понад 160 млн тонн сірчистого газу щорік) та оксидами Нітрогену (N2O, N2O3 і NO2). При з’єднанні з водою атмосфери ці речовини утворюють сильні неорганічні кислоти. На великих територіях промислово розвинених країн зареєстровано опади, кислотність яких перевищує нормальну від 10 до 1000 разів. Від кислотних дощів руйнуються екосистеми прісних водойм, гинуть ліси (мал.1), знижується врожайність грунтів.
Під керівництвом Міжнародного союзу охорони природи та природних ресурсів (МСОП) нині розроблено стратегічні принципи побудови екологічно стабільного суспільства, які погоджено з урядами більшості країн світу. Однією з умов побудови такого суспільства є чітке обмеження (квотування) промислових викидів країнами світу. При цьому країни, які не повністю використовують свої квоти (це стосується, зокрема, України), можуть продавати невикористану частину квоти іншим. Отримані кошти використовують для впровадження методик, спрямованих на поліпшення стану довкілля.

Мал. 1 Промислові об’єкти викидають в атмосферу сірчистий газ (1); наслідком цього є кислотні дощі, які знищують ліси (2)
Луги – складні, добре розчинні у воді речовини, до складу яких входять лужні метали та гідроксильні групи. Слово «луг» означає - водний розин попелу для прання, миття.
До лугів належать розчинні у воді основи. Луги беруть участь у ряді важливих хімічних реакцій, без яких неможливо уявити будь – яке хімічне виробництво. Це тверді речовини білого кольору, добре розчинні у воді. При взаємодії лугів з водою відбувається бурхливе виділення теплоти. Рідкі луги спричиняють руйнівний вплив на скло, вовну, шовк, шкіру. Тверді луги руйнують живі тканини. Небезпечним є потрапляння частинок твердого лугу в очі.
Основи – складні речовини, до складу яких входять катіони металічних елементів і один або кілька аніонів гідроксильних груп.
3.Роль неорганічних речовин (води, кисню, мінеральних солей).
«Вода, у тебе немає ні запаху, ні смаку, тебе неможливо описати, тобою насолоджуються, не відаючи, що ти таке. Неможна сказати, що необхідна для життя – ти саме життя. Ти зповнюєш нас радістю, яку не можливо пояснити нашими почуттями. З тобою повертаються до нас сили, з якими вже розпрощалися. По твоїй милості у нас знову починають підніматися високі джерела нашого серця...» – ці слова написав французький письменник і пілот Антуан де Сент-Екзюпері, після того, як його літак розбився в пустелі і він декілька днів провів під палючим сонцем.
Вода – це колиска життя, адже саме у ній воно виникло, і саме завдяки їй існує. Вода має унікальні особливості, які дозволили цій речовині зайняти найвагоміше місце на планеті.
Поетична хвилинка.
Пробудження життя
Рясні дощі на землю впали.
Ми нетерпляче їх чекали.
Була спекота до знемоги,
Земля пекла нам босі ноги,
І сохло, в’януло зело.
Давно такого не було.
Зазеленіла враз травиця,
Води побільшало в криницях,
До сонця листя потяглося,
Поналивалося колосся.
Птахи й тварини звеселіли,
Живлючим краплям всі раділи.
Дощем врятовані були.
Сади полегшено зітхнули.
Невже спекотні дні минули?
Земля сказала спеці – зась,
Коли водички напилась.
Особливості молекули води.
Формула води – Н2О.
Вода утворює основу внутрішнього середовища організмів: цитоплазма, кров, лімфа, тканинна рідина, рослинний сік… Вміст води в організмах становить 60–70%, а в деяких випадках – до 98 %. Цитоплазма більшості клітин містить приблизно 80 % води. Кров і лімфа людини містять понад 80 % води.
Воді притаманні унікальні хімічні й фізичні властивості.
Молекула води складається з двох атомів Гідрогену, сполучених з атомом Оксигену ковалентними зв’язками. На полюсах молекули води розміщені позитивні і негативний заряди, тобто вона полярна. Завдяки цьому дві сусідні молекули зазвичай взаємно притягуються за рахунок сил електростатичної взаємодії між негативним зарядом атома Оксигену однієї молекули та позитивним зарядом атома Гідрогену іншої. При цьому виникає водневий зв’язок, у 15–20 разів слабший за ковалентний. Коли вода перебуває в рідкому стані, її молекули безперервно рухаються і водневі зв’язки постійно то розриваються, то виникають знову.
Частина молекул води формує водну оболонку навколо деяких сполук (наприклад, білків). Таку воду називають зв’язаною, або структурованою (4–5 % загальної кількості води в організмах). Структурована вода, що формує водну оболонку навколо певних молекул, запобігає їхній взаємодії. Крім того, вода бере участь у підтриманні структури певних молекул, наприклад білків. Решта 95–96 % води має назву вільної: вона не пов’язана з іншими сполуками.
Залежно від температури середовища вода здатна змінювати агрегатний стан. За зниження температури вода з рідкого стану може переходити в твердий, а за підвищення – у газуватий.
Від концентрації йонів Гідрогену, яку оцінюють за водневим показником (рН – значення негативного десяткового логарифма концентрації йонів Н+), залежать структурні особливості та активність макромолекул. Нейтральній реакції розчину відповідає рН 7,0. Якщо його значення нижче – реакція розчину кисла, вище – лужна. Водні розчини, здатні протистояти зміні їхнього показника рН при додаванні певної кількості кислоти або лугу, називають буферними системами. Вони складаються зі слабкої кислоти (донора Н+) і основи (акцептора Н+), здатних відповідно зв’язувати йони гідроксилу (ОН–) та Гідрогену (Н+), завдяки чому рН усередині клітини майже не змінюється.
По відношенню до води всі речовини в природі поділяються на дві групи: гідрофільні – добре розчинні у воді та гідрофобні – практично нерозчинні у воді.
Значення води для людини.
Водний баланс людини.
Вміст води в організмі людини становить близько 65 %. Тобто, якщо маса людини становить 60 кг, то з них 39 кг припадає на воду. Вміст води залежить і від віку: у новонароджених він становить близько 75–80 %, у період завершення росту – 65–70 %, а в людей похилого віку – лише 55–60%. Між різними органами і тканинами людини вода розподілена нерівномірно: найбільше її в крові та нирках – 82–83 %, головному мозку – до 80 %, печінці – 75 %, м’язах – 70–76 %, у жировій тканині – близько 30 %, кістках – близько 20 %.![]()
Оскільки організм людини щоденно витрачає приблизно 2–2,5л води (вона виводиться з неперетравленими рештками їжі, сечею, потом, випаровується з поверхні слизових оболонок ротової порожнини та дихальних шляхів), то така сама її кількість має постійно надходити туди. Шляхи надходження води до організму різні. Крім того, близько 1 л води потрапляє з продуктами харчування, ще майже 300 мл води утворюється внаслідок окиснення жирів, білків і вуглеводів (так звана метаболічна вода). Кількість спожитої за добу води залежить від умов, у яких перебуває людина.
Протягом усього свого життя людина щодня має справу з водою. Вона використовує її для пиття і їжі, для вмивання, влітку - для відпочинку, взимку - для опалення. Для людини вода є більш цінним природним багатством, ніж вугілля, нафта, газ, залізо, тому що вона незамінна.
Без їжі людина може прожити близько 50-ти днів, якщо під час голодування вона буде пити прісну воду, без води вона не проживе й тижня - смерть настане через 5 днів. За даними медичних експериментів при втраті вологи в розмірі 6-8% від ваги тіла людина впадає в напівнепритомний стан, при втраті 10% - починаються галюцинації, при 12% людина не може відновитися без спеціальної медичної допомоги, а при втраті 20% наступає неминуча смерть.
Вміст води в клітинах різних організмів відрізняється, наприклад, вміст води в огірках дорівнює 95%, в моркві - 90, в яблуках - 85. Не відстаємо від рослин і ми. Води мало лише в жировій тканині і кістках - 33%, в м'язах - 77%, в легенях і нирках - 80, в нервовій тканині - 84, а в сірій речовини мозку - 85%. Не випадково автори давньоіндійського філософського тракту “Упанішада” вважали: “… воды размышляли: “Пусть мы станем многим, пусть мы размножимся”.
Вода - дійсно, найбільш дивовижна речовина в природі. Оскільки, вона - універсальний розчинник. В ній розчиняються всі необхідні для живого організму сполуки (органічні і мінеральні речовини, гази); вона має високу теплоємність і одночасно високу для рідин теплопровідність. Ці властивості роблять воду ідеальною для підтримання теплової рівноваги організму.
Досить цікаво дізнатися, що в кашах міститься до 80% води, у хлібі - близько 50%, у м'ясі - 58-67%, в овочах і фруктах - до 90% води, тобто "суха" їжа складається на 50-60% з води.
А близько 3% (0,3л) води утворюється в результату біохімічних процесів у самому організмі. За деякими оцінками за 60 років життя людина випиває близько 50 т води - цілу цистерну! Беручи участь в обміні речовин, вода сприяє зменшенню жирових накопичень, а отже - ваги.
Регулярне споживання води поліпшує мислення й координаційні дії мозку. Людина не повинна обмежувати себе в питті, але набагато корисніше пити часто й потроху. Шкідливо випивати відразу багато рідини, тому що вся рідина всмоктується в кров, і, поки її надлишок не буде виведений з організму нирками, серце одержує зайве навантаження.
Таким чином, можна зробити висновок про те, що роль води для людини величезна. Сьогодні кожна людина може створити для себе умови збереження безцінного водного балансу шляхом правильної організації питного режиму.
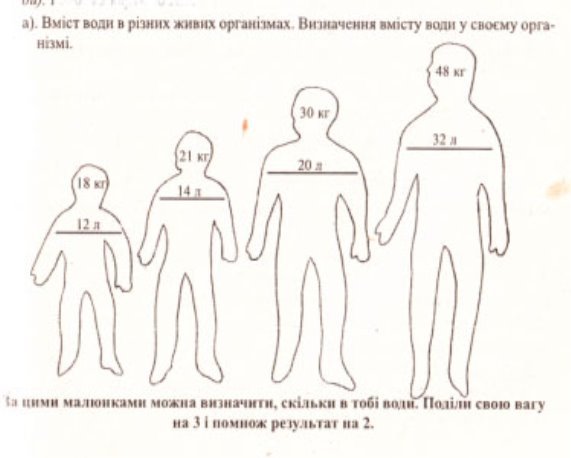
А зараз я вам пропоную дізнатися відсоток води який знаходиться у вашому орнанізмі.
Дослід «Визначння вмісту води у власному організмі»
Для того, щоб знайти масу води, з якої складається наш організм потрібно загальну масу тіла, поділену на 3 помножити на 2. Наприклад:
70/3 X 2=46,6 л.
. Також за цими даними знайдемо к-сть води у відсотках: к-сть води поділимо на вагу тіла і помножимо на 100%. Наприклад:
46,6/70Х100=66,6%
Саме стільки відсотків води повинен містити організм людини вагою у 70 кг. якщо немає відхилень.
Значення води для рослин.
Ми знаємо, що вода входить до складу тіла рослин. Хімічні процеси можуть відбуватися тільки в рідкому середовищі. Вода приймає безпосередню участь у процесах росту рослин.
Всю воду, тісно пов’язану з рослиною К.А.Тімірязєв назвав організаційною водою. Кількість організаційної води, необхідної рослині, дуже велика. Але крім цієї води, рослина потребує ще велику кількість води – тієї, що випаровується листками.
Водний режим рослин складається з п’яти основних процесів:
1. поглинання води рослиною;
2. переміщення води по рослині;
3. виділення води рослиною (газоподібному або крапельнорідкому стані);
4. засвоєння води рослиною;
5. утворення метаболічної води у процесі дихання.
Вода у рослині утворює досить динамічну систему:
- із 1000 г поглинутої води, приблизно 900 г випаровується, а 10 г
затримується у самій рослині;
- із них хімічно зв’язується 1-2 г, а 8-9 г зв’язується нехімічним
шляхом (осмотичним, колоїдно-хімічним).
Більша частина води міститься у вакуолях.
Молоді клітини зовсім не мають вакуолей або вони дуже маленькі і в невеликій кількості. По мірі зростання і розвитку рослини в цитоплазмі починають утворюватися великі вакуолі, які часто зливаються в одну центральну.
Вакуоля містить воду з розчиненими в ній органічними і мінеральними речовинами. Кислий і солодкий смак плодів залежить від вмісту цукрів і кислот у вакуолях клітин плодів. Щавель та кислиця є прикладами рослин, які містять розчинений щавелевокислий калій у клітинному соку.
Різноманітні рослини та їхні органи містять різну кількість води, а сухе насіння або сухі рослини (мохи та лишайники) можуть зберігати життєздатність при невеликому вмісті води.
Вміст води у деяких рослин у %:
- листки трав’янисих рослин – 83-85 %;
- листки дерев – 79-82 %;
- стовбури дерев – 40-55 %;
- соковиті плоди – 94-95 %.
Значення води для тварин.
Тварини дістають воду трьома основними шляхами:
- через пиття;
- разом із соковитими кормами;
- внаслідок метаболізму – за рахунок окислення та розщеплення жирів, білків та вуглеводів.
Але деякі тварини, в основному їхні личинки, можуть вбирати воду через покриви з вологого субстрату або з повітря, насиченого водяною парою.
Втрати води у тварин відбуваються через:
- випаровування покривами;
- зі слизових оболонок дихальних шляхів;
- через виділення з тіла сечі;
- через виділення неперетравлених решток.
Тварини можуть витримувати короткочасні втрати води, але ми знаємо, що втрати води призводять до загибелі швидше, ніж голодування. Витривалість до зневоднення неоднакова для різних видів. Вона завжди вища у тварин, що піддаютьсятепловим перевантаженням. Верблюди переносять втрати до 30%, вівці – до 25%, собаки – до 20%.
Види, які одержують воду в основному через пиття, дуже залежать від наявності водопоїв. Це особливо характерно для великих ссавців, у яких втрати води не можуть компенсуватися надходженням її з кормом, тому вони не можуть існувати далеко від водоймищ. Наприклад, у саванах тварини, а саме слони, антилопи, леви можуть здійснювати значні міграції до водойм.
Питної води потребують і багато птахів. Птахи пустель щодня здійснюють багатокілометрові перельоти до водопоїв і приносять воду пташенятам. Перенесення ними води відбувається надто цікавим способом: вони промочують оперення на грудях, а пташенята віджимають дзьобами змочене водою пір’я. Ластівки й стрижі п’ють воду на льоту, пролітаючи над водоймами.
Вологість повітря важлива для тварин ще тим, що від неї залежить інтенсивність випаровування води з їхньої поверхні тіла. Втрати води через випаровування залежить також від будови самих покривів. Види з добрими регуляторними можливостями мало залежать від вологості повітря.
У залежності від усього сказаного, тварин можна поділити на гігрофілів – вологолюбних та ксерофілів - сухолюбних. Проміжну групу становлять мезофіли.
Додаток
«Жива» та «мертва» вода. Збереження води на планеті.
Розповідь з елементами бесіди:
Хочу вам зачитати казку про воду:
«Лежить Іван-царевич мертвий, над ним уже вороння літає. Звідки не візьмись, прибіг Сірий Вовк і вихопив у ворона вороненя, та й каже:
– Лети, вороне, за живою і мертвою водою. Принеси мені живої та мертвої води, тоді я випущу твоє вороненя.
Нема чого робити, полетів ворон, а Вовк тримає його вороненя. Чи довго летів ворон, чи ні, але приніс він живу і мертву воду. Сірий Вовк окропив мертвою водою рани Івана-царевича і вони загоїлися; окропив живою водою — Іван-царевич ожив».
- Чи знайома вам ця казка?
Через безліч казок та переказів різних народів і часів пройшла легенда про «живу» воду. Вона зцілювала рани, оживляла мертвих, надавала сміливості та стократно збільшувала сили. І не випадково людина наділяла воду такими магічними властивостями. Коріння цих уявлень заховані в глибині віків. Виходить, древні знали про чудодійні властивості води, і знання ці передавали у народному фольклорі.
- Як ви вважаєте, яка вода є «мертвою», а яка «Живою»?
- Хто знає, скільки сьогодні людей на планеті не мають доступу до питної води? (Більше мільярду).
- Вплив технічного розвитку людства позитивно чи негативно впливає на воду? (Негативно).
- Чи повинні ми берегти воду? Чому? (Так, повинні. Запаси питної води скорочується, у подальшому це може призвести до глобальної кризи всього людства).
- Який кожен з нас може зробити посильний вклад к збереження води на планеті?
- Не забруднювати водойми та ґрунт сміттям, відходами, хімічним речовинами,
- не використовувати питну воду для поливу городу,
- економно користуватися водою,
- закручувати кран, коли вода не потрібна,
- садити дерева на берегах водойм, щоб вони не руйнувалися,
- зупиняти інших людей, які забруднюють природу…
Додаток
Цікаві факти про воду.
1. Ми ніколи не будемо мати більше води, ніж маємо зараз.
2. Щодня з поверхні землі випаровується 1,000,000,000,000 (трильйон) тонн води.
3. Вода — єдина субстанція, яка зустрічається в природі в трьох формах: твердій (лід), рідкої і у вигляді газу.
4. 80% земної поверхні вкриті водою.
5. 3% води на землі прісні; більша частина прісної води зберігається у замерзлому стані в льодовиках.
6. Середньостатистична людина складається з води на 50-80%. Ембріон людини складається з води на 95%, дитина на 70-80%, а доросла людина на 50-70%, тобто з віком людина всихає, організм людини зашлаковується і разом зі зменшенням частки води в організмі приходять хвороби і старість.
7. Кров людини на 83% складається з води.
8. Кавун на 93% складається з води.
9. У найглибшій точці світового океану (Маріанський жолоб, 11034 м.) кинутій у воду залізній кульці потрібно більше години, щоб досягти океанського дна.
10. Недалеко від села Кергалан в Азербайджані є горюча вода. Від сірника вода спалахує блакитним полум'ям через наявність у її складі метану.
11. Забруднені підземні води очищаються протягом декількох тисячоліть.
12. Людина може обходитися 30 діб без їжі і менше тижня без води.
13. У склянці води міститься близько 8,000,000,000,000,000,000,000,000 (8 септіліонов) молекул.
14. Вода — це основний розчинник в людському організмі. З її допомогою переносяться всі корисні речовини, вона ж виводить з організму шлаки та шкідливі речовини. У водних розчинах відбуваються всі хімічні реакції в нашому організмі.
15. Давно відзначений взаємозв'язок якості води, її хімічного та бактеріологічного складу, стану здоров'я та рівня захворюваності населення.
16. Середньостатистична людина, користуючись водопровідною водою, за своє життя пропускає через організм від 80кг до 100кг хімічної бруду. І саме тому так важливо бути впевненим в якості води, яку ви вживаєте.
17. У складі мантії Землі води міститься в 10-12 разів більше, ніж у Світовому океані.
18. Вживання кофеїну й алкоголю призводить до обезводнення. На кожну випиту чашку кави або порцію алкоголю треба додатково випити склянку води.
19. Морська вода замерзає при температурі — 1,91 ° C
20. Вода відбиває 5% сонячних променів, у той час як сніг —близько 85%. Під лід океану проникає тільки 2% сонячного світла.
Функції води в організмах.
1. Збереження об’єму клітин організмів.
2. Створення пружності клітин (тургор).
3. Універсальний розчинник.
4. Середовище, де відбуваються хімічні реакції.
5. Безпосередня участь в хімічних реакціях.
6. Забезпечення рівномірного розподілу тепла в організмі.
7. Створення водного балансу організму.
8. Захист організму від коливань температури.
9. Змащувальний матеріал в органах.
10. Забезпечення транспорту речовин (поживних, продуктів обміну).
Вода дійсно дивовижна речовина в природі.
Всі тіла при охолодженні стискуються, а вода - розширюється;
на її поверхні можуть плавати тіла, важчі за воду;
вона ніколи не буває в природі абсолютно чистою ;
вода навіть може подолати гравітацію!
Звернення викладача до студентів
- Чим можна пояснити ці дивовижні властивості води?
Відповідь студентів
- Мабуть, хімічною будовою та фізично-хімічними властивостями води.
Викладач: - Дійсно, так. Тому вдома заповните текстову схему пригадаючи хімічну будову, фізичні властивості та біологічні функції води, заповнюючи
Закинчити схему
Додаток
Функції води:
- Метаболічна функція. Вода є полярним розчинником, середовищем для біохімічних реакцій, кінцевим продуктом багатьох біохімічних реакцій.
- Транспортна функція. Вода забезпечує перенесення молекул усередині клітини, з однієї клітини до іншої.. вода є головним компонентом транспортної системи рослин і внутрішнього середовища тварин.
- Терморегуляторна функція. Вода забезпечує рівномірний розподіл тепла всередині організму, а під час потовиділення у тварин і транспірації у рослин охолоджує організм.
- Вода як реагент. Вода може виступати, як реагент, тобто брати участь у хімічних реакціях. Вода використовуються як джерело водню у процесі фотосинтезу.
- Деякі інші функції води. Вода в організмі – складник змащувальних рідин. Вода входить до складу жовчі, слини та слизів, що полегшують пересування речовин кишечником, створюють вологе середовище на слизових оболонках дихальних шляхів.
Кисень відіграє особливу роль у природі, він виступає одночасно, як будівник, і як руйнівник. Окислюючи органічні речовини, кисень підтримує дихання, а отже і життя. Енергія що при цьому вивільняється , забезпечує життєдіяльність організмів. Проте, за участю кисню в природі постійно відбуваються і руйнівні процеси: іржавіння металів, горіння речовин, гниття рослинних і тваринних решток.
Фізіологічна дія: атмосферний кисень є життєво важливим для всіх живих організмів (виняток становлять анаеробні бактерії). Він бере участь у процесах дихання. Крізь легені кисень потрапляє у кров, розноситься з нею по всьому організму і в клітинах забезпечує перебіг реакції окислення. Реакції окиснення відбуваються і в рослинах, які також поглинають кисень під час дихання.
В медичній практиці збагачені киснем газові суміші використовуються для вдихання при станах, що супроводжуються кисневою недостатністю: при захворюваннях дихальних шляхів (пневмоніях, набряку легень та інше) серцево-судинної системи (декомпенсація серцевої діяльності, коронарна недостатність та ін.), при хірургічних операціях, що проходять в умовах гіпербаричної оксигенації, при отруєннях вуглекислим газом, синильною кислотою, хлором, фосгеном, при травмах і ураженнях, що супроводжуються порушенням функції дихання і окисних процесів.
Випускають медичний кисень в сталевих герметичних балонах, пофарбованих в синій колір. Зберігають в прохолодному місці. Стиснений кисень не має контактувати із жирними речовинами, оскільки швидке окислення їх протікає екзотермічно і може привести до спалаху і вибуху. В аптеках кисень відпускають в спеціальних кисневих подушках.
В анестезіології кисень широко використовують в суміші із засобами для інгаляційного наркозу, а також призначають в післяопераційний період.
Кисень ефективний для лікування гельмінтозів, аскаридозу, трихоцефальозу. Кисень володіє антисептичними властивостями, він використовується для анаеробної інфекції, але тривале вдихання чистого кисню, особливо при його поступленні (якщо перевищує 1 атм.) викликає запалення слизових оболонок дихальних шляхів та інші патологічні зміни в організмі.
Мінеральні солі
Солі – складні речовини, утворені катіонами металічних елементів і аніонами кислотних залишків.
Важливу роль у життєдіяльності клітини відіграють мінеральні солі, молекули яких у водному розчині розпадаються на катіони й аніони. Ряд катіонів і аніонів необхідний для синтезу важливих органічних речовин.
Неорганічні натрієві й калієві солі нітратної та ортофосфатної кислот, кальцієва сіль сульфатної кислоти є важливими складовими мінерального живлення рослин, тому їх вносять в грунт як добрива для підживлення рослин.
Від солей значною мірою залежать надходження води до клітини та буферні властивості клітин і тканин.
Буферність – здатність клітин підтримувати слаболужну реакцію (рН) свого вмісту на сталому рівні (близько до нейтральної реакції), незважаючи на те, що в процесі обміну речовин безперервно утворюються кислі і лужні продукти.
Якщо концентрація солей у клітині вища, ніж у середовищі, то вода буде надходити у клітину. У клітині, за умови її нормального функціонування, підтримується її чітко визначений якісний і кількісний склад солей. Підвищення вмісту йонів Калію, наприклад, спричиняє токсичний вплив на серцевий м’яз. Відкладення Кальцію в кістках можливе лише за умови присутності йонів Фосфору, коли співвідношення Кальцію та Фосфору становить 2:1, а відкладення Фосфору можливе лише за умови присутності вітаміну D. Хлоридна кислота створює кисле середовище у шлунку тварин і людини й у спеціальних органах комахоїдних рослин, прискорюючи перетравлення білків їжі.
Мінеральні солі у великій кількості перебувають у клітинах опірних органів - черепашок, хітинових панцерів, кісток. У цитоплазмі інших клітин велика частина солей міститься в дисоційованому стані у вигляді катіонів і аніонів -К+,Na+, Ca+, Cl-, HCO3-.
Щодоби до організму людини має надходити 12-15 г кухонної солі (NaCl). Всмоктування солей починається ще в шлунку, а завершується в кишечнику. Рецептори, розташовані у стінках кровоносних судин і тканинах, здатні визначати концентрацію солей. Імпульси від цих рецепторів надходять до гіпоталамуса, який, у свою чергу, регулює діяльність залоз внутрішньої секреції. Залежно від вмісту солей в організмі під впливом нейрогуморальної регуляції змінюється їхній вміст у сечі.
Через порушення обміну речовин солі можуть відкладатися у суглобах, що спричиняє важкі захворювання – остеохондроз та подагру, за яких спотворюються суглоби кінцівок, втрачається гнучкість хребта, розвиваються напади болю в нирках. Ці захворювання можуть призвести до зменшення рухомості та втрати працездатності. Щоб їх уникнути, необхідно вести активний спосіб життя, не зловживати м’ясними та жирними стравами, сіллю та іншими приправами, відмовитися від алкоголю.
У порожнинах органів або їхніх вивідних проток можуть формуватися щільні утворення – “камені”. Найчастіше вони утворюються в нирках, жовчному міхурі, ниркових мисках і сечовому міхурі при відкладанні там кальцієвих солей органічних (сечова та щавлева) або неорганічних (карбонатної чи ортофосфатної) кислот. Унаслідок розвивається сечокам’яна хвороба – камені, поступово збільшуючись, спочатку викликають болі в поперековій ділянці, а потім, просуваючись через сечовивідні шляхи, – напади дуже сильного болю. Інколи камені закупорюють сечоводи і тоді, аби врятувати життя хворого, застосовують хірургічне втручання.
Студенти об’єднуються у групи по 3, вивчають один із мінеральних речовин, прочитавши відповідний розділ підручника та працюючи із роздатковим матеріалом (5 хв). Виступи представників (експертів) про виконану роботу (назвати мінеральну речовину, розповісти про її значення для живих організмів). Заповнити таблицю.
Значення деяких мінеральних речовин для живих організмів
|
Мінеральна речовина |
Значення для живих організмів |
|
Mg |
У рослинних і тваринних організмах магній міститься в кількостях близько 0,01 %, а до складу хлорофілу входить до 2 % . За нестачі магнію припиняється ріст і розвиток рослин. Накопичується він переважно в насінні. Уведення магнієвих сполук у ґрунт помітно підвищує врожайність деяких культурних рослин. У тварин магній є будівельним матеріалом для кісткової тканини (приблизно 70 % усього магнію). Крім цього він бере участь у багатьох процесах клітинного метаболізму й необхідний для правильного функціонування різноманітних ферментів |
|
Na |
Натрій є основним позаклітинним катіоном. Він бере участь у підтриманні кислотно-лужної рівноваги і входить до складу бікарбонатної, фосфатної буферних систем. Обмін Натрію є основою водно-сольового обміну організму. Натрій забезпечує постійність осмотичного тиску в організмі. За участі його йонів передається збудження по нервовому волокну, від них залежить нервово-м'язова активність. Разом з Калієм Натрій відіграє основну роль у скоротливій функції міокарда |
|
Ca |
Кальцій є основним структурним елементом кісткових тканин, впливає на проникність клітинних мембран, бере участь у роботі багатьох ферментних систем, передачі нервових імпульсів, м'язовому скороченні, відіграє важливу роль у всіх стадіях зсідання крові. У крові кальцій міститься в неорганічних сполуках і білкових комплексах. Його йони, будучи наявними в різних білкових структурах, керують функціями, життєвим циклом клітин. У рослинній клітині кальцій регулює фізико-хімічний стан цитоплазми: підтримує колоїдний стан, визначає поряд з магнієм та іншими елементами кислотність середовища. Завдяки стабільності стану цитоплазми спостерігається тургор рослини, відбувається активний обмін і синтез сполук |
|
K |
Калій є у складі тканин рослинних і тваринних організмів. Однією з найважливіших функцій Калію є підтримка потенціалу клітинної мембрани. Концентрація йонів Калію впливає на осмотичний тиск у клітинах — тиск розчину на напівпроникну перетинку, яка відокремлює його від розчинника або розчину меншої концентрації. Конкурентність між йонами Калію та Натрію обумовлює участь Калію в регуляції кислотно-лужної рівноваги в організмі |
|
Cl |
Хлор у формі хлорид-аніона бере участь у регуляції тургору в деяких рослинах. Переміщаючись разом з Калієм, він підтримує в клітинах електронейтральність. Однак уміст хлориду рідко досягає такого високого рівня, як уміст Калію. Відомо також, що хлор стимулює фотосинтетичне фосфорилювання, але його точна біохімічна роль у цьому процесі ще не встановлена |
|
I |
Основною фізіологічною роллю Іоду є участь у метаболізмі щитовидної залози та гормонів, які вона виробляє. Нестача Іоду призводить до виникнення характерних симптомів: слабкості, пожовтіння шкіри, відчуття холоду й сухості. Лікування тиреоїдними гормонами або Іодом усуває ці симптоми. Недолік тиреоїдних гормонів може призвести до збільшення щитовидної залози. В окремих випадках утворюється зоб. Нестача Іоду особливо сильно позначається на здоров'ї дітей — вони відстають у фізичному й розумовому розвитку. Надлишок гормонів щитовидної залози призводить до виснаження, нервозності, тремору, втрати ваги та підвищеної пітливості. Це пов'язано з підвищенням пероксидазної активності та, внаслідок цього, зі збільшенням іодування тиреоглобуліном. Надлишок гормонів може бути наслідком пухлини щитовидної залози. Для лікування використовують радіоактивні ізотопи Іоду, що легко засвоюються клітинами щитовидної залози |
|
Хлоридна кислота |
Виробляється у шлунку хребетних тварин. Відіграє важливу роль у процесах травлення |
ІV. Узагальнення, систематизація та контроль знань студентів
Осмислення об’єктивних зв’язків та взаємозалежностей у вивченому матеріалі.
Чим обумовлене неоднакове співвідношення хімічних елементів в живих і неживих об’єктах?
Співвідношення елементів в живих і неживих об’єктах різне. Така відмінність обумовлена певними особливостями елементів, які переважають у живих об’єктах. Це прямо пов’язано з їхніми фізичними та хімічними властивостями.
Дайте відповідь на запитання, поставлене ще на початку заняття:
- Як розпізнати речовини, якщо їх так багато в природі?
(За хімічними і фізичними властивостями)
Понятійне опитування «Добери пару»
Один студент називає термін або поняття і пояснює його значення, другий добирає до нього пару і знову пояснює його значення. І так далі.
Органогенні елементи: оксиген, гідроген, нітроген, карбон.
Макроелементи: Магній, Калій, Натрій, Кальцій, Ферум, Сульфур, Фосфор.
Мікроелементи: Бор, Кобальт, Купрум, Молібден, Цинк, Валадій, Йод, Бром.
Ультрамікроелементи: Уран, Радій, Аргентум, Меркурій, Берилій, Цезій, Селен.
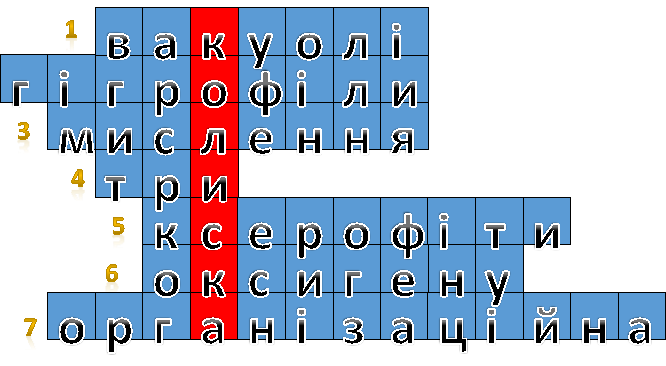
Кросворд 1

Кросворд 2

Метод «Пошта»
Для роботи використовують три поштові скриньки (конверти):
- Макроелементи
- Мікроелементи
- Ультрамікроелементи
Конверти можуть бути умовними (наприклад, можна написати їхні назви на дош-ці). Студенти мають покласти до відповідної кишені (або за допомогою магніту закріпити на дошці під відповідним написом) за встановлений час і не помилитися адресою із наявних листів-елементів, що адресовані саме тому адресату, якому вони відповідають.
Закінчити речення:
- Простими називають речовини, які…
- Складними називають речовини, які…
- Основи – це…
- Кислоти – це…
- Оксиди – це…
- Луги – це…
V. Самостійна робота студентів
Робота зі словником (виписати терміни).
Понятійний апарат:
|
Біохімія |
|
|
Органогенні елементи |
|
|
Мікроелементи |
|
|
Макроелементи |
|
|
Ультрамікроелементи |
|
|
Буферність |
|
VІ. Підведення підсумків заняття та оцінювання студентів
Студенти самостійно підбивають підсумки заняття, формулюючи висновки.
Технологія «незакінчені речення».
Студенти працюють із незакінченими реченнями:
«Заняття важливе тому, що…»
«Для себе я з’ясував, що…»
«Я знаю…», «Я вмію…»
Створення «ситуації успіху»
Об’єктивне аргументування оцінки за заняття. Похвала.
Сьогодні на занятті за активну роботу, правильні відповіді, високий рівень засвоєння даної теми студенти отримують такі оцінки
______________________________________________________________________
______________________________________________________________________
______________________________________________________________________
самопідготовку та творчу роботу вдома –
______________________________________________________________________
______________________________________________________________________
______________________________________________________________________
______________________________________________________________________
Залишилося трішечки докласти зусиль, повторивши теоретичний матеріал і результат буде найвищий,-
______________________________________________________________________
______________________________________________________________________
Таким студентам, як
______________________________________________________________________
я бажаю не зупинятися, вчитися перемагати себе і обставини.
Пробудіть свої амбіції. Покажіть власний результат ______________________________________________________________________
Діти, а яке відкриття ви зробили для себе сьогодні?
Чи є у вас питання з теми, на які б ви хотіли отримати відповідь?
VІІ. Надання та пояснення домашнього завдання
Завдання для студентів всієї групи.
1. Прочитати: підручник Р. О. Сабадишин, С. Є. Бухальська «Медична біологія»,
стор. 58-60.
2. Продовжити роботу зі словником, дописати визначення новим термінам.
3. Дати відповідь на питання: «Чи можлива нормальна життєдіяльність організму без мінеральних солей?»
Індивідуальні завдання.
1. Підготувати повідомлення із ЗМІ, інтернету з теми «Проблеми пов’язані з порушенням вмісту елементів».
2. Підготувати презентацію «Основні класи неорганічних сполук».
3.Приготувати повідомлення про: «Вимоги до питної води та її якості».
Наше заняття підійшло до закінчення. Я всім бажаю бути щасливими, здоровими й отримувати задоволення від власних досягнень! Дякую за увагу!
Додаток
План-схема заняття
|
Етапи заняття |
Форми і методи навчальної діяльності |
Результати діяльності |
|
І. Організаційний етап |
Бесіда. Ігрова розминка «Мій настрій». |
Створення сприятливої психологічної атмосфери, оцінка готовності до роботи. |
|
ІІ. Актуалізація опорних знань і мотивація навчально-пізнавальної діяльності |
Репродуктивна бесіда. Встановлення «Містка» між раніше вивченими поняттями та тими, що будуть засвоєні на занятті.
Постановка проблемного завдання.
Записи плану заняття в зошиті. |
Підвести студентів до вивчення теми «Неорганічні речовини» є надзвичайно важливою.
Розвиток активного відношення до навчання.
Розвиток пізнавального інтересу. |
|
ІІІ. Вивчення нового матеріалу |
Бесіда з елементами наочності.
Технологія кооперативного навчання (робота в групах з використанням підручника)
Цікава хвилинка. |
Розповідь з демонструванням слайдів, відеофрагментів.
Створення колективної опорної схеми.
Розвиток пізнавального інтересу, самостійна об-робка нової інформації, самоорганізація студен-тів, вміння цінувати свою особистість.
Перехід до іншого виду діяльності. |
|
ІV. Узагальнення, систематизація та контроль знань і вмінь студентів |
Понятійне опитування – «добери пару».
«Пошта».
Розв’язання кросворду. |
Установлення студентами рівня власних знань |
|
V. Самостійна робота студентів |
Робота зі словником (виписати терміни) Робота з підручником |
Розвиток пізнавального інтересу |
|
VІ. Підведення підсумків заняття та оцінювання студентів
|
Технологія «незакінчені речення»
Аргументація оцінювання студентів (створення «ситуації успіху») |
Оцінка студентами влас-ної роботи на занятті.
Об’єктивне аргументу-вання оцінки за заняття |
|
VІІ. Надання та пояснення домашнього завдання
|
Особистісно орієнтована технологія (диференціація домашнього завдання) |
Засвоєння навчального матеріалу, самостійна обробка нової інформації, вміння використ. сучасні комп’ютерні технології. |
Додаток
Додаток
Фронтальне опитування.
- Яке завдання біології , як науки про основи життєдіяльності людини?
- Що вивчає наука біологія?
- Які біологічні явища Ви знаєте?
- Назвіть найвизначніші моменти у вивченні органічного світу.
- Що являють собою давні організми?
Письмове опитування.
- Дайте визначення поняттю "біологія". З якими науками тісно пов'язана біологія?
- Назвіть вчених та їх досягнення у розвитку медицини.
- Які основні методи дослідження біології Вам відомі?
- Яка мета біологічних досліджень?
- Дайте характеристику поняттю "життя".
- Назвати основні ознаки живого.
- Які фундаментальні властивості живого Ви знаєте?
- Заповніть таблицю:
Рівні організації живого
|
Рівні організації |
Властиві ознаки |
|
Молекулярний Клітинний |
|
- Заповніть таблицю:
Рівні організації живого
|
Рівні організації |
Властиві ознаки |
|
Тканинний Органний |
|
10. Заповніть таблицю:
Рівні організації живого
|
Рівні організації |
Властиві ознаки |
|
Організмовий Популяційно-видовий |
|
|
|
|
- Заповніть таблицю:
Рівні організації живого
|
Рівні організації |
Властиві ознаки |
|
Біогеоценотичний Біосферний |
|
Усне індивідуальне опитування.
- Охарактеризувати предмет і завдання біології, як науки про живі організми.
- Які Вам відомі вчені - біологи України? Їх внесок у розвиток біології, як науки.
- Рівні організації та ознаки живого, біологічні явища, які їх характеризують.
- Охарактеризуйте чим відрізняються живі організми від організмів неживої природи?
- Які існують форми життя на Землі?
- Перерахувати відкриття, знахідки, гіпотези в біології, які є результатом діяльності вчених усього світу.
Тести програмованого контрою.
1. Вкажіть, хто із дослідників у 1802 році вперше запропонував термін «біологія»:
а) Ж.-Б. Ламарк; г) Т. Шванн;
б) Ч. Дарвін; д) Г. Мендель.
в) К. Лінней;
2. Визначте, яка наука вивчає прокаріотичні організми:
а) вірусологія; г) бактеріологія;
б) мікологія; д) іхтіологія.
в) альгологія;
3. Визначте, яка наука займається вивченням грибів:
а) бріологія; г) мікологія;
б) альгологія; д) теріологія;
в) ботаніка; е) ентомологія,
4. Зазначте, яка наука вивчає шляхи історичного розвитку певних систематичних груп:
а) онтологія;
б) систематика;
в) палеонтологія;
5. Зазначте, яка наука вивчає закономірності історичного розвитку живої матерії:
а) онтологія; г) філогенія;
б) систематика; д) еволюційне вчення.
в) палеонтологія;
6. Вкажіть, хто створив у першій половині XX ст. учення про ноосферу:
а) О. Ковалевський; г) В. Вернадський;
б) С. Навашин; д) І. Мечніков.
в) І. Шмальгаузен;
- Розташуйте по порядку рівні організації живої матерії, починаючи від найнижчого:
а) біоценотичний; д) біогеоценотичний;
б) молекулярний; е) популяційно-видовий;
в) клітинний; є) організмовий.
г) біосферний;
8. З'ясуйте, як називається метод дослідження та демонстрації процесів та функцій за допомогою спрощеної імітації:
а) моніторинг; в) опис;
б) моделювання; г) експеримент.
9. З'ясуйте, як називається науково обґрунтоване припущення, яке висувають для пояснення факту, який безпосередньо не спостерігається:
а) факт; г) правило;
б) гіпотеза; д) закон.
в) теорія;
10. Назвіть, які науки займаються вивченням тварин:
а) ліхенологія; д) іхтіологія;
б) бріологія; е) герпетологія;
в) орнітологія; є) мікологія.
г) теріологія;
Відповіді до тестів:
- а
- г
- г
- г
- д
- г
- б, в, є, е, а, д, г
- б
- б
- в, г, д, е
Додаток
Карта ООД для роботи з літературою по темі:
"Вступ. Короткий нарис історії розвитку біології"
|
Питання, що вивчаються |
Вказівки до завдання |
Самостійний запис |
|
1. Біологія, як наука. |
Дати визначення |
Біологія - система наук про життя в усіх його проявах на всіх рівнях організації живого. |
|
2. Предмет біології. |
Дати визначення |
Предметом вивчення біології є живі організми, їх будова, функції, зв'язки між собою і довкіллям, природні угруповання, оболонка життя в цілому. |
|
3. Зв'язок біології з іншими науками. |
Коротко описати |
Цитологія, молекулярна біологія, генетика, екологія, філогенетика, біотехнологія, генна інженерія, медична біологія. |
|
4. Основні методи дослідження біології. |
Перелічити |
|
|
5. Мета біологічних досліджень. |
Коротко описати |
Мета біологічних досліджень полягає у пізнанні сутності життя і закономірностей його прояву. |
|
6. Основні ознаки живого. |
Перелічити |
|
|
7. Властивості живого. |
Коротко описати |
|
|
8. Рівні організації живої матерії. |
Дати визначення |
Рівні організації живої матерії - це відносно гомогенні біологічні системи, для яких характерні певний тип взаємодії елементів, просторовий часовий масштаб процесів. |
|
9. Рівні організації живого. |
Перелічити |
|
|
10. Властивості живих організмів. |
Перелічити |
|
|
11. Різноманітність існуючих форм життя. |
Коротко описати |
|
|
12. Вчені - біологи України. |
Перелічити. |
|
Додаток
Карта ООД для роботи з літературою по темі:
" Елементарний склад організмів. Неорганічні сполуки клітини"
|
Питання, що вивчаються |
Вказівки до завдання |
Самостійний запис |
|
Вміст хімічних елементів у клітині 1. Біологія. |
Дати визначення |
|
|
2. Групи хімічних елементів. |
Перелічити |
1. 2. 3. |
|
3. Органогенні елементи. |
Коротко описати |
|
|
4. Оксиген. |
Коротко описати |
|
|
5. Карбон. |
Коротко описати |
|
|
6. Гідроген. |
Коротко описати |
|
|
7. Нітроген. |
Коротко описати |
|
|
Неорганічні речовини клітини 1. Вода, її роль. |
Коротко описати |
|
|
2. Вміст води в клітинах різних організмів. |
Охарактеризувати коротко |
|
|
3. Функції води в організмі. |
Охарактеризувати коротко |
|
|
4. Регуляція надходження води в клітини. |
Коротко описати |
|
|
5. Фізіологічні властивості води. |
Перелічити |
1. 2. 3. |
|
6. Хімічні властивості води. |
Перелічити |
1. 1. 3. |
|
7. Фізичні властивості води. |
Перелічити |
1. 2. 3. |
|
8. Агрегатні стани води. |
Перелічити |
1. 2. 3. |
|
9. Тургор і об'єм. |
Дати визначення |
|
|
10. Роль мінеральних солей в організмі. |
Перелічити |
|
|
11. Шляхи надходження мінеральних солей в організм. |
Перелічити |
|
|
12. Функції мінеральних солей. |
Перелічити |
|
|
13. Інші неорганічні компоненти клітин. |
Перелічити |
|
Фронтальні запитання вчителя:
- Чи може людина прожити без води? (Ні).
- Скільки днів людина може прожити без води? (Близько трьох днів).
- Чи могло б існувати життя на планеті без води? (Ні).
- Хто знає, скільки води міститься в організмі людини? (2/3 маси, 65 – 70 %).
- Чи знаєте ви, де саме, на думку вчених, виникло Життя? (У воді).
Самостійна робота
- З чого складається молекула води?
- Скільки води міститься в організмі людини?
3. Скільки днів людина може прожити без води?
4.Скільки води потрібно вживати за добу?
5. Перерахуйте симптоми зневоднення організму?
6.Де в рослинах найбільше міститься води?
7. В яких рослинах найбільше міститься води?
8.Перерахуйте основні шляхи попадання води в організм тварин?
9. Яка безхребетна тварина найбільше складається з води?
Додаток



про публікацію авторської розробки
Додати розробку
