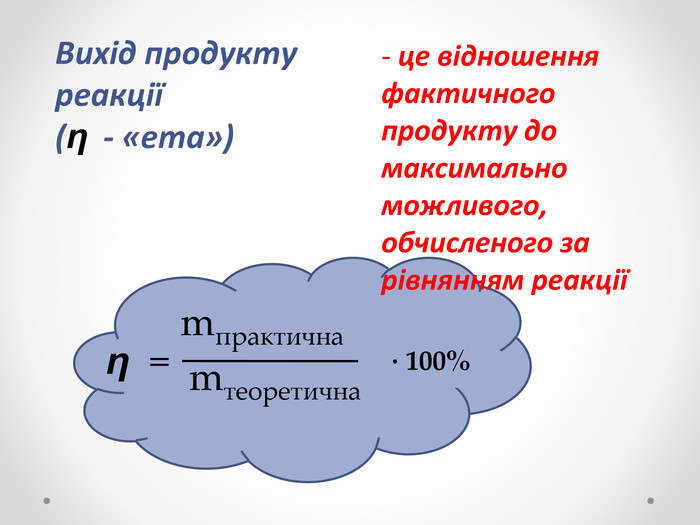
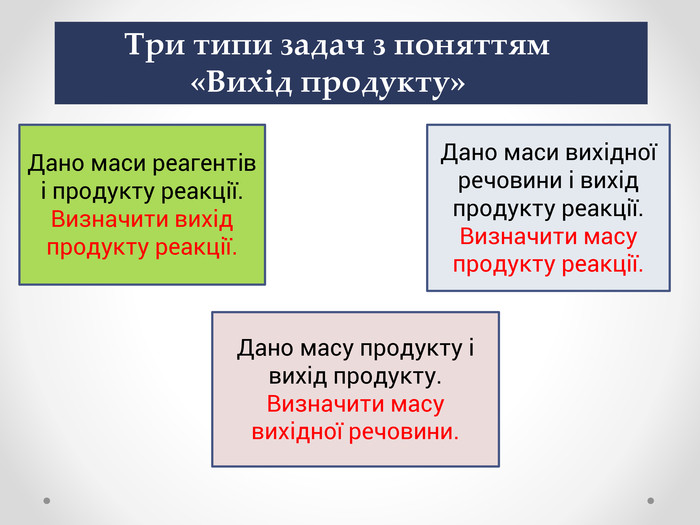
Обчислення за хімічними рівняннями відносного виходу продукту реакції.
Про матеріал
Презентація до уроку розв’язування розрахункових задач на обчислення за хімічними рівняннями відносного виходу продукту реакції. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку