Оксиген. Поширеність Оксигену в природі. Кисень, склад його молекули, поширеність у природі. Фізичні властивості кисню
• повторити класифікацію речовин; закріпити знання учнів про елементи метали і неметали та прості речовини на прикладі Оксигену й кисню; дати поняття про Оксиген – хімічний елемент і кисень – просту речовину; ознайомити учнів з поширенням кисню в природі, його фізіологічною дією; • розвивати вміння учнів самостійно здобувати знання , використовувати раніше набуті знання в новій навчальній ситуації; • виховувати творчу , допитливу особистість
Тема. Оксиген. Поширеність Оксигену в природі. Кисень, склад його молекули, поширеність у природі. Фізичні властивості кисню
Мета:
- повторити класифікацію речовин; закріпити знання учнів про елементи метали і неметали та прості речовини на прикладі Оксигену й кисню; дати поняття про Оксиген – хімічний елемент і кисень – просту речовину; ознайомити учнів з поширенням кисню в природі, його фізіологічною дією;
- розвивати вміння учнів самостійно здобувати знання , використовувати раніше набуті знання в новій навчальній ситуації;
- виховувати творчу , допитливу особистість
Обладнання та реактиви: періодична система хімічних елементів, модель молекули кисню.
Базові поняття та терміни: Оксиген, кисень, хімічний елемент, проста речовина
Тип уроку: вивчення нового матеріалу
Хід уроку
І. Організаційний момент
Привітання вчителя. Емоційне налаштування учнів на урок.
ІІ. Мотивація навчальної діяльності
Оголошення теми, мети та завдань уроку.
Учитель: Ми розпочинаємо роботу над темою «Кисень». Сьогодні ми познайомимось з хімічним елементом Оксигеном і утвореною ним простою речовиною киснем, дізнаємось про те, чому хімічний елемент Оксиген вважають одним з найпоширеніших в природі, а речовину кисень – найважливішою в житті живих організмів. Отримані на уроці знання знадобляться вам не лише на наших наступних уроках , а і у вашому повсякденному житті. Відомий вчений Й. Я. Берцеліус зазначав: «Кисень – це речовина, навколо якої обертається земна хімія». Отже, вперед за новими знаннями.
ІІІ. Актуалізація опорних знань учнів.
Метод «Мікрофон»
1.Що таке хімічний елемент?
2.Що таке речовина?
3.Які речовини називаються простими?
4.Які речовини називаються складними?
5.На які дві групи можна умовно поділити всі хімічні елементи?
Хімічний диктант
1. Який вчений та в якому році визначив об’ємні частки кисню та азоту в повітрі? (А.Лавуаз’є у 1774 році)
2. Повітря – це… (складна суміш близько 15 різних газів)
3. Встановіть відповідність між компонентам повітря та їх об’ємними частками:
|
А. 78% |
1. Кисень О2 |
|
Б. 0,04% |
2. Карбон (IV) оксид СО2 |
|
|
3. Інші гази |
|
Г. 0,03% |
4. Аргон Ar |
|
Д. 0,93% |
5. Азот N2 |
Вчитель: Одним з найпоширеніших хімічних елементів на нашій планеті є Оксиген, який утворює просту речовину кисень.
ІV. Вивчення нового матеріалу.
Поширеність Оксигену і кисню в природі.
Бесіда вчителя з учнями:
Оксиген. Хімічний елемент Оксиген можна з повним правом назвати всюдисущим. Чому ж? Спробуємо розібратися. Якби ми вигукнули : «Оксиген!», ехо пішло б звідусіль: з – під землі, бо пісок, глина, багато гірських порід і мінералів містять Оксиген; з морів та річок, бо він входить до складу молекули води; з повітря ( чому?), бо 1/5 об’єму повітря – це проста речовина кисень, молекула якої утворена двома атомами Оксигену. Навіть у живих організмах багато Оксигену.
Я скрізь навколо тебе є,
бо Оксиген – ім’я моє.
Я у деревах, у траві,
в твоїх я жилах, у крові.
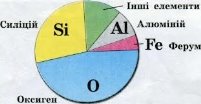
Оксиген у природі
На поверхні нашої планети Оксиген – найпоширеніший елемент. Він становить 49% від маси земної кори. Вода – найпоширеніша сполука Оксисену. Гідросфера містить 86-89% Оксисену за масою. Як нам уже відомо у атмосфері цього елементу 21%. Живі організми також містять велику кількість Оксисену приблизно 60-62%.
По активності у природі Оксиген посідає друге місце після Флуору. Через це він утворює сполуки майже з усіма елементами.
Про роль кисню в природі написані тисячі книг. Усі живі організми дихають киснем і в безкисневій атмосфері просто не можливе життя. Лише деякі мікроорганізми – анаеробні бактерії, живуть без кисню. Без кисню неможливий процес горіння.
Запитання до учнів:
Згадайте з уроків біології, природознавства, завдяки якому процесу кисень відновлюється в атмосфері? (процес фотосинтезу)
6 СО2 + 6 Н2О → С6Н12О6 + 6 О2
Оксиген утворює дві прості речовини: кисень (О2) та озон (О3).
Кисень – головний компонент повітря. Він підтримує дихання (С6Н12О6 + 6 О2→6 СО2 + 6 Н2О) та горіння (Проста реч. + О2 = оксид).
Оксиди - це бінарні сполуки хімічних елементів з оксисеном.
Оксидів дуже багато. Як іх називають? Назва оксиду складається з двох слів: назва хімічного елемента та слова «оксид». Наприклад
СаО – кальцій оксид. ZnO – цинк оксид. А якщо оксид утворюєть елементом який має змінну валентність, то потрібно післі назви елемента зазначати його валентність.
CuO - купрум(ІІ) оксид; Cu2O - купрум(І) оксид.
Усі живі організми дихають киснем і в безкисневій атмосфері просто не можливе життя. Лише деякі мікроорганізми – анаеробні бактерії, живуть без кисню.
Графічна формула кисню має такий вигляд: О = О.
Чи знаєте ви, чому при подорожі високо в горах стає важче дихати? Бо найбільше кисню міститься в нижніх шарах атмосфери.
Самостійна робота з підручником
Прочитайте розділ «Фізичні властивості кисню» і заповніть таблицю
Фізичні властивості кисню
|
Агрегатний стан - |
газ |
|
Запах - |
не має |
|
Смак - |
не має |
|
Колір - |
не має (але товстий шар кисню при заломленні променів світла яскраво-блакитний) |
|
Добре, чи погано розчиняється у воді - |
Погано (малорозчинний в 1 л Н2О при T=20 оС розчиняється 31 мл кисню – 0,004% за масою) |
|
Важчий чи легший за повітря - |
Важчий (1 л повітря при T=0 оС 1,29г, а кисню – 1,43) |
Відкриття кисню.
- У 1772 році славетний шведський фармацевт Карл Вільгельм Шеєле (1742-1786) після численних дослідів з розкладу селітри (KNO3, NaNO3) одержав «вогненне повітря», в якому скіпка, що ледь жевріла, загорялася яскравим полум'ям. Шеєле повторив дослід зі спалювання фосфору, але у «вогненному повітрі» після згоряння фосфору колба цілком заповнювалася водою. Утім, таємниця вогню так і залишалася для вченого таємницею, тому що до кінця днів він залишався прихильником теорії «флогістону».
- У 1774 році протестантський священник, англієць Джозеф Прістлі (1733-1804) шляхом розкладання меркурій оксиду в герметично закритій посудині (Пристлі направляв на цю сполуку сонячні промені за допомогою могутньої лінзи).
t
2HgО → 2Hg + O2↑
Однак Пристлі спочатку не зрозумів, що відкрив нову просту речовину, він вважав, що виділив одну зі складових частин повітря (і назвав цей газ "дефлогістованим повітрям", «покращеним повітрям»). Про своє відкриття Пристлі повідомив видатного французького хіміка Антуана Лавуазьє.
Шеєле добув кисень раніше, ніж Прістлі, але опублікував свої результати пізніше. Тому першовідкривачем кисню вважають Дж. Прістлі.
V.Узагальнення та систематизація знань.
1. Дай відповіді на питання.
1.Які фізичні властивості має кисень?
2. Яка поширеність кисню в різних оболонках землі?
3. Які речовини називають оксидами.
4. Який вчений та в якому році відкрив «покращене повітря»?
5. Обчисліть молекулярну масу кисню.
6. обчисліть у скільки разів кисень важчий за повітря.
7. Оксиген міститься у мінералах: гематиті Fe2O3, кварці SiO2, піролюзиті MnO2. У яких з них масова частка Оксисену найбільша?
Хвилинка – цікавинка:
- Рідкий кисень , як і залізо притягується до магніту.
- Організм дорослого чоловіка щодоби споживає приблизно 900 г кисню, а жінки – 600 г
VІ. Підсумок уроку.
VІІ. Домашнє завдання.
Опрацювати параграф, відповісти на запитання.
Творче завдання: Створити малюнки, що відображають: склад молекули кисню; фізичні властивості кисню; речовини, які містять атоми Оксисену


про публікацію авторської розробки
Додати розробку

