Презентація "Багатоатомні спирти"


















![Методи одержання багатоатомних спиртів1) Гідратація етиленових вуглеводнів у присутності окисників: СН2=СН2+ [О] +Н2 О → СН2 ОН—СН2 ОН2) Гідроліз галогенопохідних алканів водними розчинами лугів: С2 Н4 Cl2 + 2 КОН = С2 Н4(ОН)2 + 2 КCl С3 Н5 Cl3 + 3 КОН = С3 Н5(ОН)3 + 3 КCl3) Лужний гідроліз жирів. Методи одержання багатоатомних спиртів1) Гідратація етиленових вуглеводнів у присутності окисників: СН2=СН2+ [О] +Н2 О → СН2 ОН—СН2 ОН2) Гідроліз галогенопохідних алканів водними розчинами лугів: С2 Н4 Cl2 + 2 КОН = С2 Н4(ОН)2 + 2 КCl С3 Н5 Cl3 + 3 КОН = С3 Н5(ОН)3 + 3 КCl3) Лужний гідроліз жирів.](/uploads/files/752735/435594/490807_images/21.jpg)
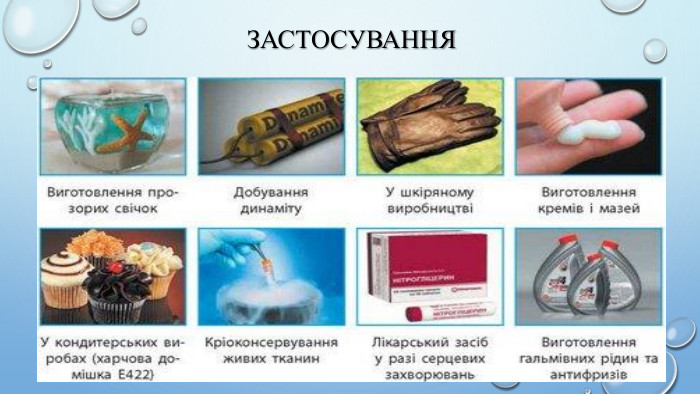


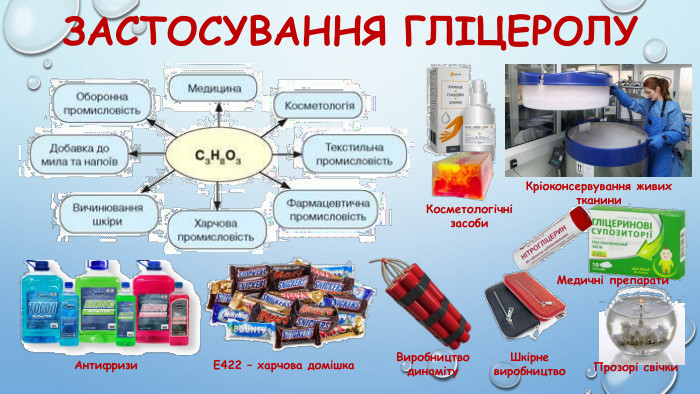






6. Увідповідніть рівняння хімічної реакції з її типом. Рівняння хімічних реакцій. Типи реакціїА C2 H5 OH + 3 O2 → 2 CO2 + 3 H2 O1 часткове окиснення. Б C2 H5 OH + HBr → C2 H5 Br + H2 O2 дегідратація. В C2 H5 OH → CH2 = CH2 + H2 О3 повне окиснення. Г 2 CH3 OH + O2 → 2 НСОН + 2 H2 О4 гідратація 5 заміщення
номенклатура. Двохатомні спирти називають – діоли або гліколі;Триатомні спирти називають – тріоли або гліцероли;Найпростішим представником двоатомних спиртів є етиленгліколь (гліколь), триатомних спиртів – гліцерол (гліцерин). Формула етандіолу ( етиленгліколю) СН2 ОН –СН2 ОН (С2 Н4(ОН)2), пропантріолу-1,2,3 (гліцеролу): СН2 ОН –СНОН –СН2 ОН (С3 Н5(ОН)3).
Фізичні властивості Етиленгліколь: Безбарвна, в’язка рідина; - Солодкий на смак;Температура плавлення – 11,5℃;Температура кипіння – 197,8℃;Добро розчинний у воді. Отруйний. Гліцерин: Безбарвна, в’язка, гігроскопічна рідина;Солодка на смак;Змішується з водою у будь-якому співвідношенні;Температура плавлення - 18℃;Температура кипіння - 290℃.
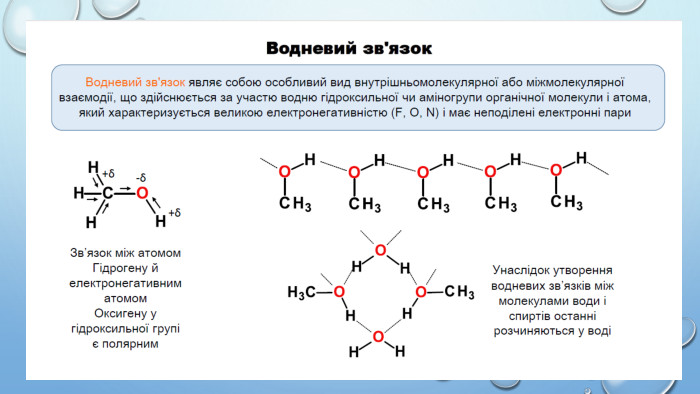
Фізичні властивості багатоатомних спиртів. З-поміж загальних фізичних властивостей багатоатомних спиртів необхідно відзначити, що це в’язкі речовини, добре розчинні у воді й погано розчинні в органічних розчинниках. Властивості багатоатомних спиртів визначаються наявністю водневого зв’язку. Більша кількість гідроксильних груп зумовлює утворення більшої кількості водневих зв’язків. Це зумовлює велику в’язкість і високу температуру кипіння цих речовин, а також розчиненність їх у воді та інших спиртах. Дослід 1. Розчинення гліцеролу у воді. https://www.youtube.com/watch?v=cx9miyk_y9w
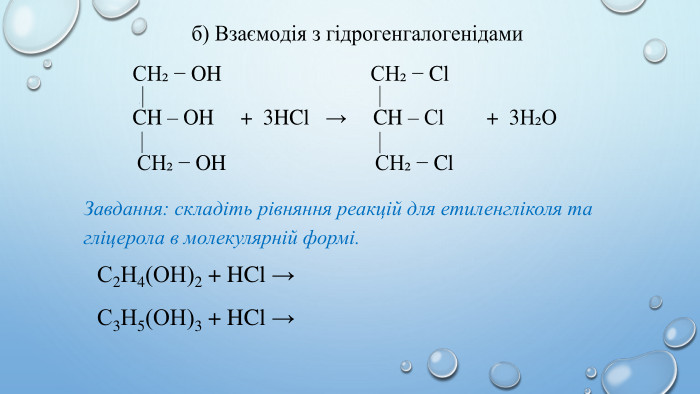
Хімічні властивості багатоатомних спиртів Для багатоатомних спиртів характерними є основні реакції одноатомних спиртів. На відміну від останніх вони можуть утворювати похідні за однією або кількома гідроксильними групами, залежно від умов проведення реакцій. Повне окиснення (горіння)Завдання: складіть рівняння реакцій горіння для етиленгліколю та гліцеролу. С2 Н4(ОН)2 + О2 → СО2 + Н2 ОС3 Н5(ОН)3 + О2 → СО2 + Н2 О
Методи одержання багатоатомних спиртів1) Гідратація етиленових вуглеводнів у присутності окисників: СН2=СН2+ [О] +Н2 О → СН2 ОН—СН2 ОН2) Гідроліз галогенопохідних алканів водними розчинами лугів: С2 Н4 Cl2 + 2 КОН = С2 Н4(ОН)2 + 2 КCl С3 Н5 Cl3 + 3 КОН = С3 Н5(ОН)3 + 3 КCl3) Лужний гідроліз жирів.
Закріплення знань. Речовина містить 39,1% карбону, 8,7% гідрогену та 52,2% оксигену. Виведіть її молекулярну формулу, якщо молярна маса речовини - 92 г/моль. Обчисліть масу (г) гліцеролу, що вступить у реакцію з металічним натрієм масою 13,8 г. Обчисліть об’єм (л) кисню (н. У.), Який необхідно використати на спалювання гліцеролу масою 9,2 г.
2. Укажіть молекулярну формулу гліцеролу.3. Укажіть спільну ознаку, характерну для етанолу та гліцеролу. А за нормальних умов тверді речовини Б взаємодіють із металічним натрієм В містять декілька гідроксильних груп Г мають однаковий колір полум’я під час горіння. А C3 H5(ОН)3 В СH3 ОНБ С2 Н5 ОНГ С3 Н7 ОН


про публікацію авторської розробки
Додати розробку