Презентація до уроку на тему " Лужні та лужноземельні метали"
В презентації наданий матеріал, який характеризує властивості ,застосування в промисловості та значення для життєдіяльності людини лужних та лужноземельних металів.



















1. Узагальнити і систематизувати знання про лужні та лужноземельні метали. 2. Вміти характеризувати елементи за положенням в періодичній таблиці. 3. Знати фізичні і хімічні властивості . 4. Вміти пояснити біологічну роль елементів та значеня в промисловості.5. Захист довкілля від шкідливого впливу мийних засобів.4. 4. Цілепокладання:
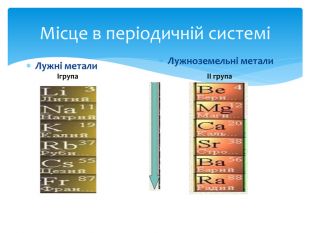
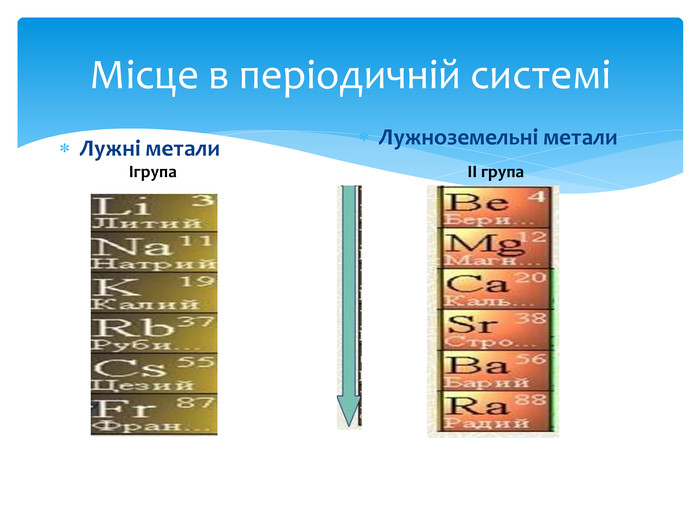
Фізичні властивостіЛужні метали. Лужні метали — м'які (натрій ріжеться ножем, як вершкове масло, інші трохи жорсткіші) метали від сріблисто-білого до сірого кольору з характерним блиском, що дуже швидко тьмяніють на повітрі. Легкоплавкі й рухливі. Агресивні, вибухонебезпечні (зберігаються під шаром гасу (керосин))Лужноземельні метали. Практично всі ці елементи являють собою тверді речовини сіруватого кольору (принаймні, при нормальних умовах і кімнатній температурі)Володіють вищими за лужні метали t°пл. і t°кип., потенціалами іонізації, щільністю і твердістю. Знайдіть у підручнику , які фізичні властивості має магній, чи дуже вони відрізняються від властивостей лужноземельних металів
Хімічні властивостіЛужні метали 1. Легко реагують із киснем повітря. Літій при окисленні утворює оксид Li2 O, решта - перексиди й супероксиди:4 Li + O2 = 2 Li2 O4 Na + O2 = 2 Na2 O4 K + O2 = 2 K2 O 2. Легко й з вибухом реагують із водою:2 Na + 2 H2 O = 2 Na. OH + H2 3. Легко реагують із неметалами:2 Na + S = Na2 S2 K + Br2 = 2 KBr4. Специфічні властивості:2 К+Н2 =2 КН (гідрид калію)Лужноземельні метали1. Взаємодіють з простими речовинами: 2 Me0 +O2 → 2 Me+2 O-2 Me0 +H2 → Me+2 H2 Me0 +Cl02 → Me+2 Cl2 Me0 +S0 → Me+2 S-2 Me0 +2 HCl → Me+2 Cl2 + H2 Me0 +2 HOH → Me+2(OH)2 +Н2 Ca2 Sr2+Ba2+
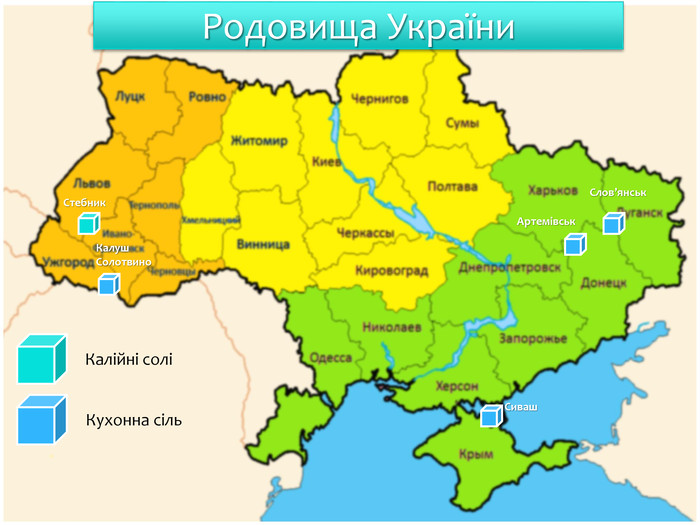
Поширення в природіУ природі лужні елементи трапляються лише у вигляді солей. Найважливішими мінералами Натрію є кам’яна сіль або галіт Na. Cl, чилійська селітра Na. NO3, глауберова сіль або мірабіліт Na2 SO4 • 10 H2 O. Велика кількість солей Натрію кристалізується при випаровуванні морської води. Масова частка Натрію у земній корі становить 2,6 %. Калій, як і Натрій, є досить розповсюдженим хімічним елементом. Масова частка Калію в земній корі — 2,5%. Природні солі Калію : сильвін KCl, сильвініт КCl ∙ Na. Cl карналіт КCl ∙ Mg. Cl2 ∙ 6 H2 OКалій входить до складу польових шпатів і слюди. Літій досить широко поширений в земній корі польовий шпат
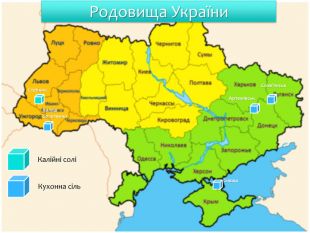
Поширення в природіУ зв'язку з високою хімічною активністю у вільному стані в природі він не зустрічаються, а тільки у вигляді різних сполук. Деякі з них, як хлорид калію, утворюють потужні родовищ. Найбагатші у світі родовища солей калію у вигляді мінералів сильвіну KCl, сильвініту KCl·Na. Cl, карналіту КCl ∙ Mg. Cl2 ∙ 6 H2 O і каїніту KCl·Mg. SO4·3 H2 O розташовані поблизу м. Солікамська. Крім того, значні поклади сполук калію знайдені в Білорусії (м. Солігорськ) і в Україні (м. Калуш і м. Стебник у Прикарпатті).хлорид калію нітрат калію
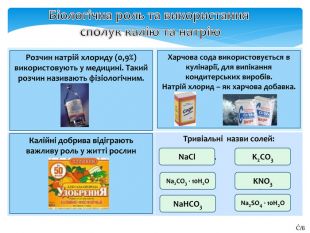
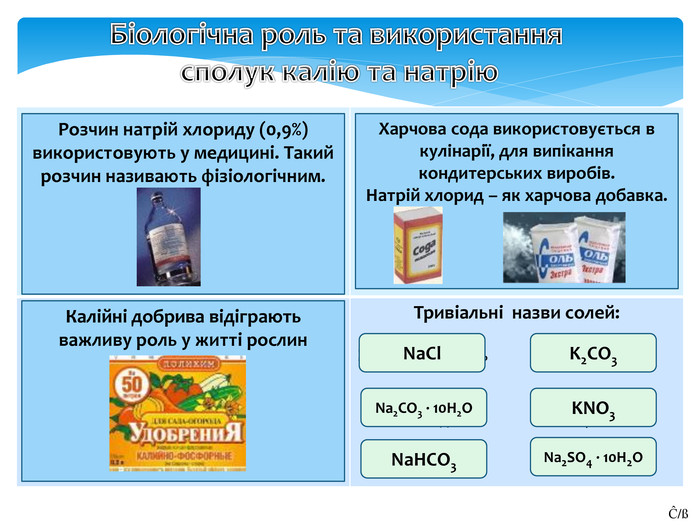
Біологічна роль та використання сполук калію та натрію{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}Сколько воды и хлорида натрия нужно взять для приготовления физиологического раствора массой 0,5 кг?4,5г соли495,5 г воды Смесь хлорида и гидрокарбоната натрия массой 15 г обработали уксусной кислотой, при этом выделилось 2,8 л (н.у.) газа. Определите массовые доли в процентах компонентов смеси.70% Na. HCO330% Na. Cl. Хлорид калия - очень ценное минеральное удобрение. Рассчитайте массовую долю калия (%) в этом веществе.52%Тривіальні назви солей: Поваренная сольответ. Розчин натрій хлориду (0,9%) використовують у медицині. Такий розчин називають фізіологічним.ответ. Харчова сода використовується в кулінарії, для випікання кондитерських виробів. Натрій хлорид – як харчова добавка.ответ. Калійні добрива відіграють важливу роль у житті рослин Na. Cl. Кристалли-ческая сода. Na2 CO3 · 10 H2 OПитьевая сода. Na. HCO3поташ. K2 CO3 Калийная селитра. KNO3 Глауберова соль. Na2 SO4 · 10 H2 OĈ/ß
Поширення в природі лужноземельних металів. У зв'язку з високою хімічною активністю у вільному стані в природі вони не зустрічаються, а тільки у вигляді різних сполук. Наприклад: Гіпс Ca. SO4∙ 2 H2 O , барітова каша Ba. SO4 Апатит Ca3(PO4)2 , вапняк,мармур Ca. CO3 Вапно Са(ОН)2 Та інші.
Біологічна роль та використання магнію{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A} Магній входить до складу хлорофілу і, отже, відіграє незамінну роль у фотосинтезі і в газообміні планети; загальний вміст магнію в тканинах рослин на Землі за деякими оцінками складає близько 1011 тонн. Крім хлорофілу, магній у всіх тканинах рослин бере участь також в утворенні жирів, у перетворенні фосфорних сполук. Особливо багато магнію в соку каучуконосних рослин. Брак магнію призводить до зменшення кількості хлорофілу і до побледнению і зміні забарвлення листя на червону і жовту Англійська сіль (Mg. SO4 ? 7 H2 O ) використовується як проносне і жовчогінний засіб. При ін'єкціях вона викликає стан, близький до наркотичного , і використовується для боротьби з судомами, для лікування гіпертонії, психічного збудження ; в поєднанні з іншими препаратами - для знеболювання при пологах. Водні розчини тіосульфату магнію використовуються для лікування опіків та інших захворювань шкіри. Біла магнезія ( Mg. CO3 ) входить до складу зубних порошків і присипок ; крім того, вона зменшує кислотність шлункового соку. Палена магнезія ( Mg. O ) теж нейтралізує шлунковий сік . Крім того, вона застосовується всередину при кислотних отруєннях.Ĉ/ß
Перевірка знань Порівняйте атоми елементів, поставивши знаки <,> або = замість *: а) заряд ядра: Mg * Ca, Na * Mg, Ca * К; б) число електронних шарів: Mg * Ca, Na * Mg, Ca * К; в) число електронів на зовнішньому рівні: Mg * Ca, Na * Mg, Ca * К; г) радіус атома: Mg * Ca, Na * Mg, Ca * K


про публікацію авторської розробки
Додати розробку