Презентація до уроку на тему: " Загальна характеристика солей"
В презентації наданий матеріал про властивості, добування ,застосування та значення для житттєдіяльності людей солей.



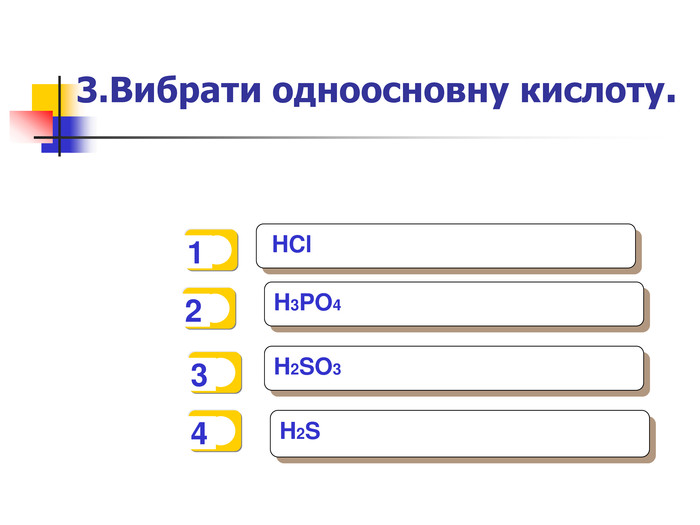






























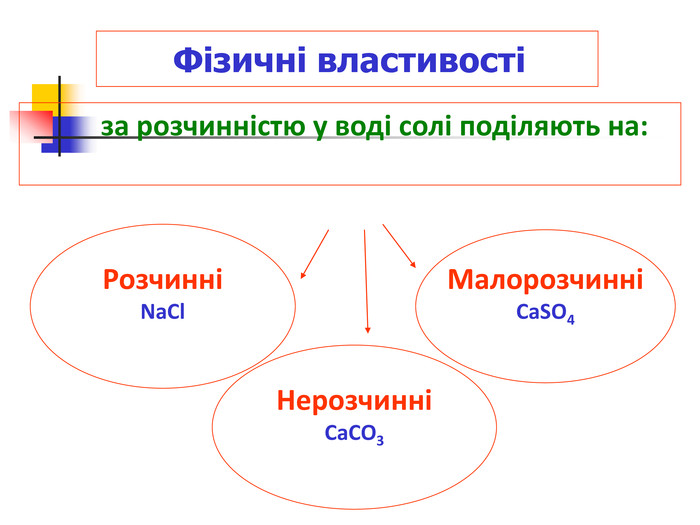











Поширення солей в природі. Поварена сіль NaCl Слово "сіль" пішло від грецького терміну "hals" – що означало "море", а мінералогічнкий термін повареної солі – галліт Це мінерал, який є основною необхідною речовиною для життєдіяльності, а також одним з найбільш важливих промислових сировинних мінералів
Алгоритм складання формул солей 1.На початку формули ставиться метал,а за ним кислотний залишок 2.Проставляються над йонами їх заряди 3.Знаходять найменше спільне кратне зарядів.(НСК) 4.При діленні НСК на заряди йонів отримуємо індекси. Ферум(ІІІ) сульфат VI III II III II FeSO4→ Fe2(SO4)3
-
 Потапова Галина Іванівна 10.03.2025 в 22:01ДякуюЗагальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Потапова Галина Іванівна 10.03.2025 в 22:01ДякуюЗагальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку