Презентація до уроку" Основні положення МКТ"
Дану презентацію можна використовувати як матеріал до уроку, при пояснені нового матеріалу так і для самостійного опрацювання учнями теми " Основні положення МКТ"





















![Молярний об’єм – це об’єм одного моля речовини: Концентрація молекул (n) – число молекул в одиниці об'єму. [n]=м⁻³ Молярний об’єм – це об’єм одного моля речовини: Концентрація молекул (n) – число молекул в одиниці об'єму. [n]=м⁻³](/uploads/files/1966715/267756/291829_images/25.jpg)











З яких частинок складаються всі речовини?2. Чи можна стверджувати, що молекула є найменшою частинкою речовини?3. Як розміщені молекули в речовині: щільно чи з проміжками?4. Який характер руху молекул у речовині?5. Як залежить рух молекул від температури речовини?6. Як сили діють між молекулами в речовині?
Досягнення молекулярної фізики широко використовують в інших науках про природу. З її успіхами, зокрема, нерозривно пов'язаний розвиток хімії і біології. В процесі розвитку в молекулярній фізиці виділилися самостійні розділи, наприклад: фізична хімія, фізична кінетика, молекулярна біологія, фізика твердого тіла та ін. Основні поняття молекулярної фізики використовують у деяких спеціальних галузях науки, зокрема, у фізиці металів, полімерів і плазми, кристалофізиці, фізико-хімічній механікі.
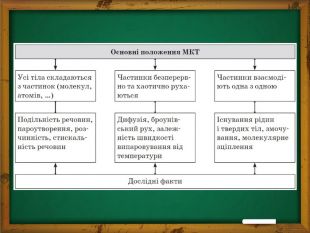
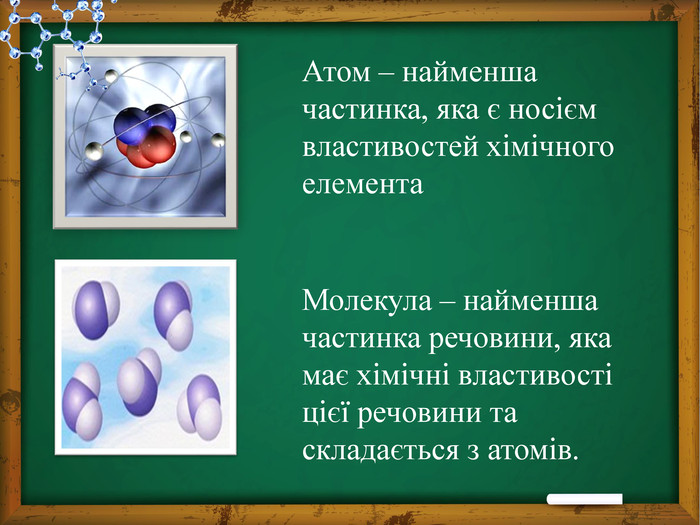
Молекулярно-кінетичною теорією називають вчення про будову і властивості речовини на основі уявлень про існування атомів і молекул як найменших частинок хімічних речовин. У XVIIІ ст. прихильник і пропагандист МКТ М. Ломоносов сформулював основні положення цієї теорії, які не зазнали суттєвих змін і до сьогодні.
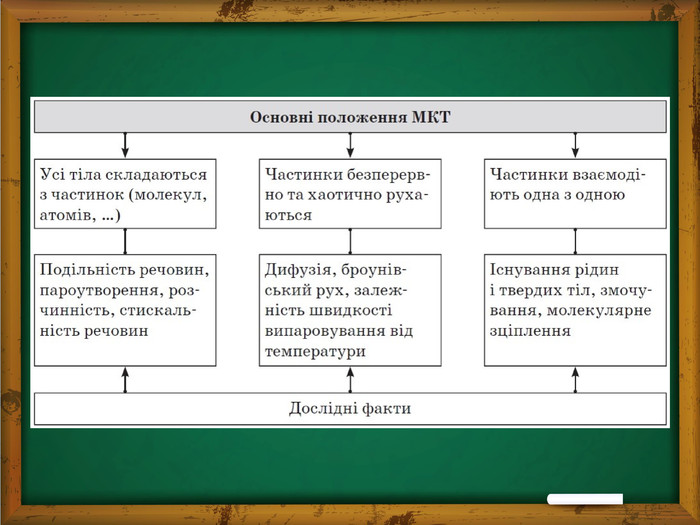
В основі МКТ речовини лежать три основні положення.1) Всі речовини утворені з найдрібніших частинок — атомів, молекул, йонів, тобто мають дискретну будову; між частинками є проміжки. Молекули й атоми являють собою електрично нейтральні частинки. За певних умов молекули й атоми можуть набувати додаткового електричного заряду та перетворюватися на позитивні або негативні іони.2) Атоми й молекули перебувають у невпинному безладному (хаотичному) русі ; такий рух називають тепловим.3) Частинки взаємодіють одна з одною(притягуються та відштовхуються) силами, що мають електричну природу.
Будь-яка речовина складається з найдрібніших частинок — молекул чи атомів. Всі речовини складаються з молекул, розділених проміжками (дискретне будова речовини). У 1647 р. П'єр Гассенді (франц.) ввів слово «молекула» (molecula, зменшувальне від лат. Moles - маса)Молекула речовини - дрібна частка, зберігає його хімічні властивості. Атом в перекладі з грецького означає "неподільний". Найважливіші положення МКТ:
3. У 1 см2 повітря стільки молекул, що, взявши таку саму кількість піщинок, можна було б засипати територію великого підприємства.4. Якщо взяти таку кількість цеглин, скільки молекул міститься в 1 см3 повітря, то цегла б щільно вкрила поверхню Землі шаром заввишки 120 м (висота 40-поверхового будинку).5. У краплі води діаметром 0,1 мм приблизно 1016 молекул, що майже в мільйон разів більше, ніж людей, які мешкають на Землі.6. Як що молекулу води (d ≈ 3 ⋅ 10–10 м ) з більшити в мільйон разів, то вона матиме розмір крапки (≈ 0,3 мм). Унаслідок такого самого збільшення товщина волосини (0,1 мм) виявиться 100 м, діаметр вишні (1 см) — 10 км, а середній зріст людини (170 см) — 1700 км.
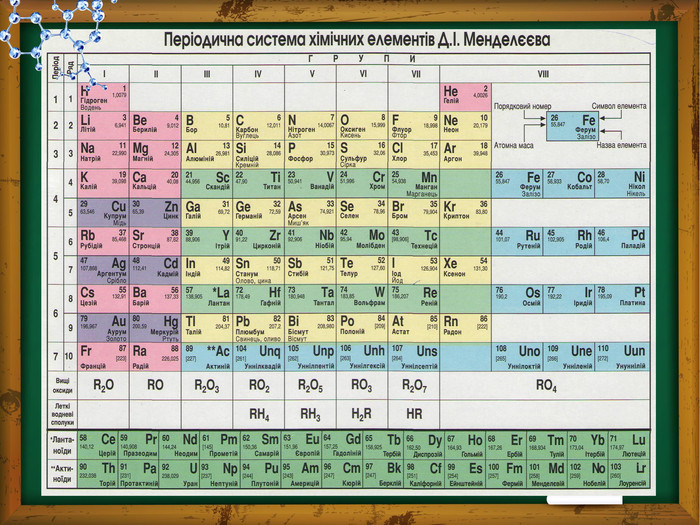
Молекули та атоми дуже маленькі, а тому незручно їх вимірювати в кілограмах, вводимо позасистемну одиницю вимірювання - атомну одиницю маси, яка дорівнює 1/12 маси молекули карбону 1/12 тос = 1а.о.м. = 1,66∙10-27кг. Відносною молекулярною (або атомною масою) речовини називають відношення маси молекули (або атома) т0 даної речовини до 1/12маси атома карбону тос.
Сінквейн Розмір молекул дуже малий, тому їх кількість у макроскопічному тілі велика, що незручно для розрахунків. Тому використовують відносну кількість молекул, порівнюючи з 1 молем. Один моль – це кількість речовини, що містить стільки ж молекул, скільки атомів Карбону міститься в 12г карбону. Незалежно від агрегатного стану, моль речовини містить однакове число молекул N А = 6,02 • 1023 моль-1 (стала Авогадро).
Сінквейн Кількість речовини ν – це кількість молей, тобто відношення числа молекул (чи атомів) N у даному тілі до числа молекул (чи атомів) NА в 1 молі. Фізичну величину, що визначає число молекул у певному тілі, називають кількістю речовини. У СІ кількість речовини виражають у молях.
Задача. Всім відомо, що в організмі люди 70 % води. Будемо вважати,що середня маса учня вашого віку 50 кг. Скільки молекул води в організмі учня?N=NA ∗ m. M 1. Знаходимо молярну масу води. M(H2 О) = (1 * 2 + 16) * 10-3 КГМОЛЬ 2. Знаходимо масу тіла(70%)m = 50 * 0,7 = 35 кг. N = 6,02 * 1023 1моль ∗ 35 кг18 ∗10−2 ∗ кгмоль = = 11,7 * 1026 шт. Відповідь: 11,7 * 1026 штук молекул води в організмі учня. Дано: Н2 О – 70%m = 50 кг. N - ?NA = 6,02 * 1023 1моль
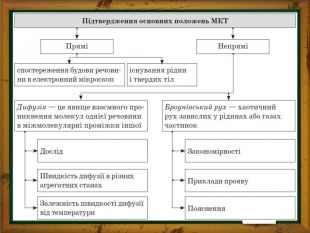
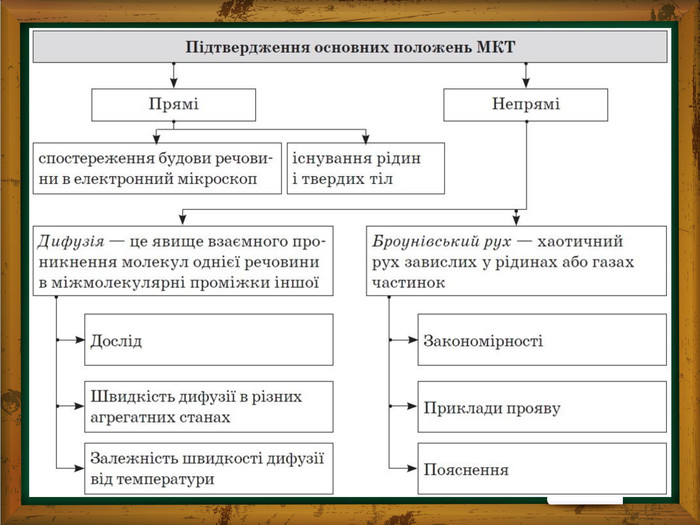
Броунівський рух – це хаотичний, тепловий рух найдрібніших мікроскопічних частинок, зважених у рідині або газі. 1827 р. відкритий англійським ботаніком Р. Броуном; 1905 р. створена А. Ейнштейном теорія броунівського руху ;1908-1911 pp. французський фізик Ж. Перрена експериментально підтвердив теорію Ейнштейна Дослідне підтвердження існування молекул.
Дифузією називається явище проникнення двох або кількох дотичних речовин одна в одну. Найшвидше процес протікає в газі, якщо він неоднорідний за складом. Дифузія призводить до утворення однорідної суміші, незалежно від густини компонентів. Перегляньте відео. Комп’ютерний експеримент «Властивості газів. Дифузія.»https://phet.colorado.edu/sims/html/diffusion/latest/diffusion_uk.html. Дифузія
Різновидом дифузії є осмос ( від грец.osmos — поштовх, тиск) — процес однобічної дифузії крізь напівпроникну перегородку (мембрану) молекул розчинника в бік більшої концентрації розчиненої речовини. У природі завдяки осмосу поживні речовини та вода проникають із ґрунту в корені рослин, із травного тракту — в організми істот і безпосередньо в клітини; кисень із легеневих альвеол надходить у кров тощо. Жан-Антуан Нолле
Домашнє завдання. Підручник «Фізика 10», рівень стандарту, за редакцією В. Г. Бар’яхтара §26,вправа 26 №1,2 – середній рівень;вправа 26 № 1-4 – достатній рівень;вправа 26 № 1-5 – високий рівень. Перегляньте відео. Комп’ютерний експеримент «Властивості газів. Дифузія.»https://phet.colorado.edu/sims/html/diffusion/latest/diffusion_uk.html
-
 Бондаренко Тетяна Оленксандрівна 26.02.2024 в 20:12Дуже дякую. Об'ємно подано. Мені вистачило матеріалу для декількох уроків.Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Бондаренко Тетяна Оленксандрівна 26.02.2024 в 20:12Дуже дякую. Об'ємно подано. Мені вистачило матеріалу для декількох уроків.Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку