Презентація до уроку: "Реакції йонного обміну"


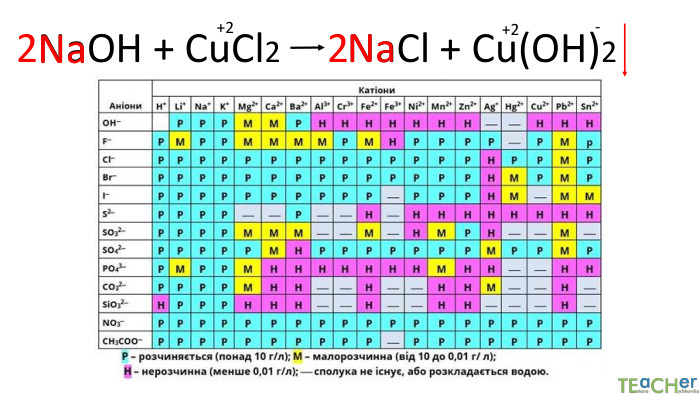
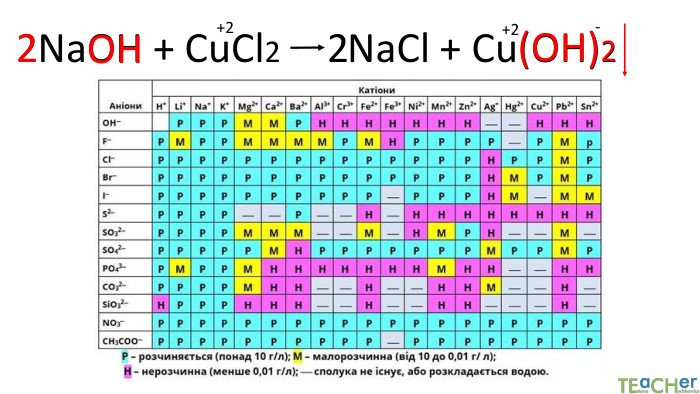
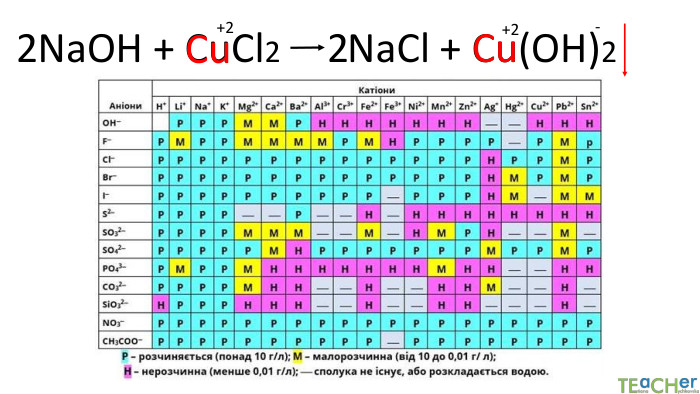

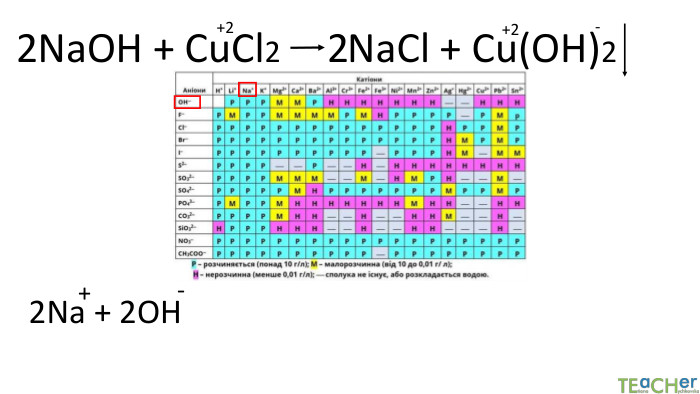

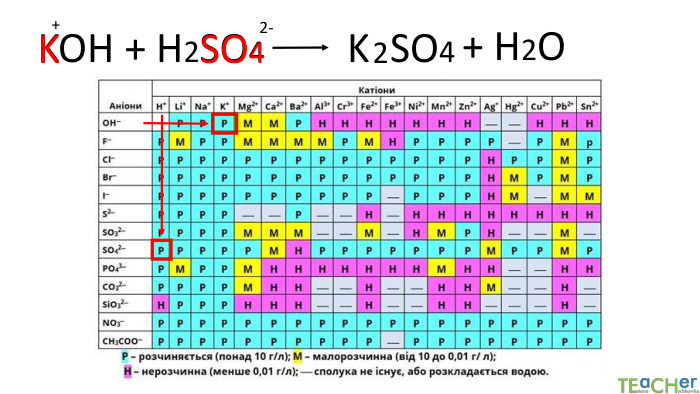
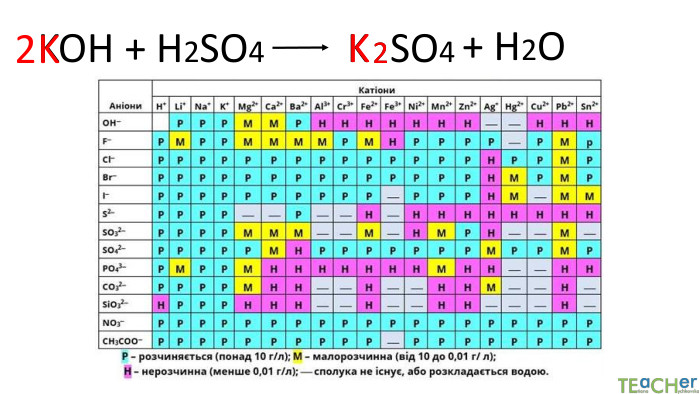
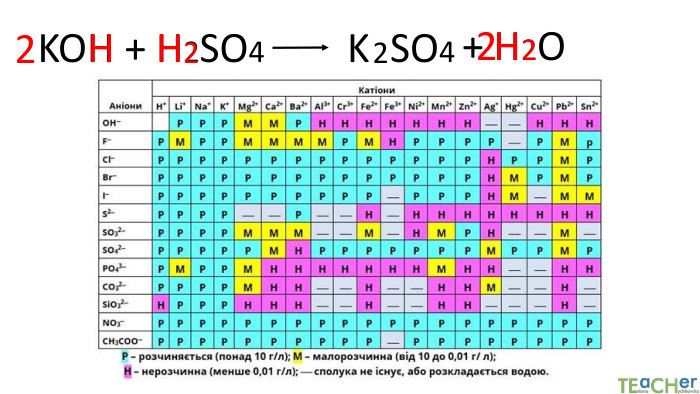
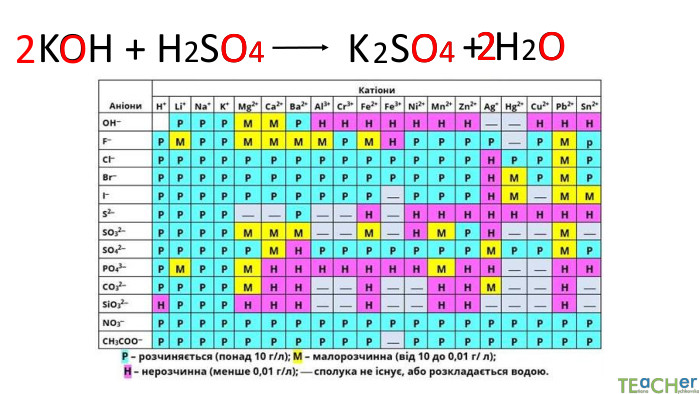








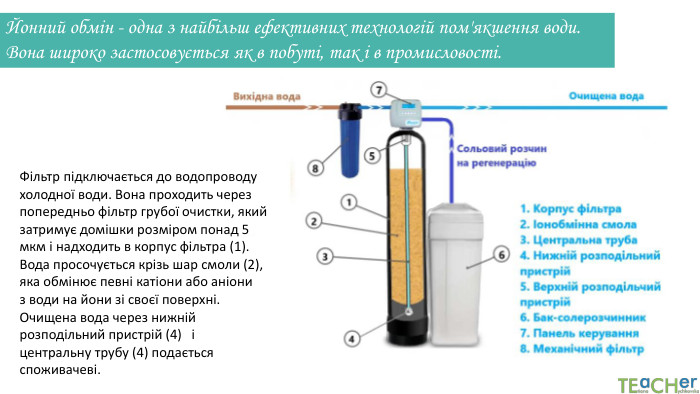



Йонний обмін - одна з найбільш ефективних технологій пом'якшення води. Вона широко застосовується як в побуті, так і в промисловості. Фільтр підключається до водопроводу холодної води. Вона проходить через попередньо фільтр грубої очистки, який затримує домішки розміром понад 5 мкм і надходить в корпус фільтра (1). Вода просочується крізь шар смоли (2), яка обмінює певні катіони або аніони з води на йони зі своєї поверхні. Очищена вода через нижній розподільний пристрій (4) і центральну трубу (4) подається споживачеві.
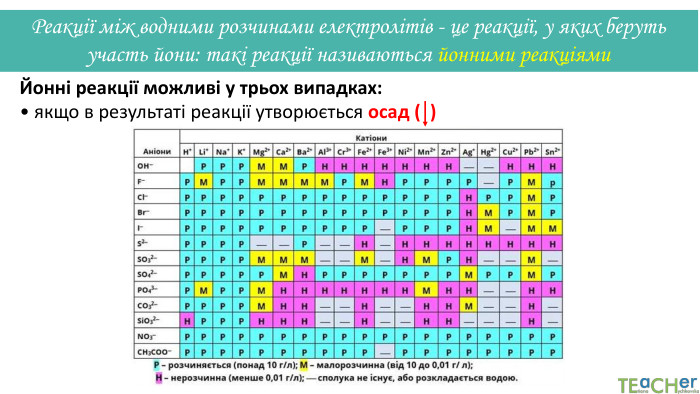
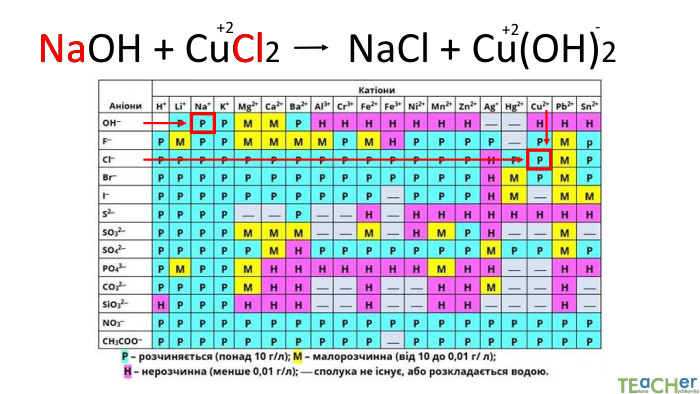
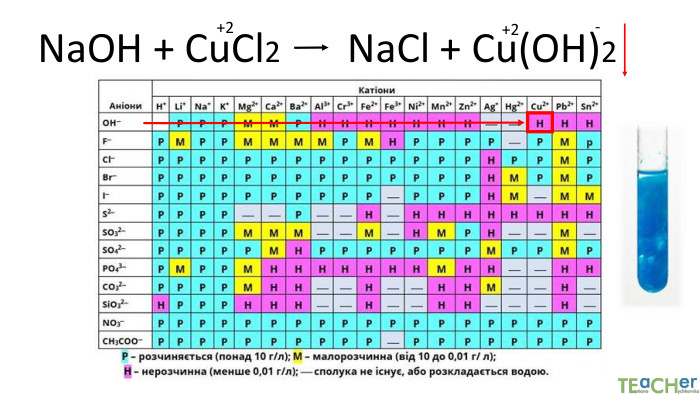
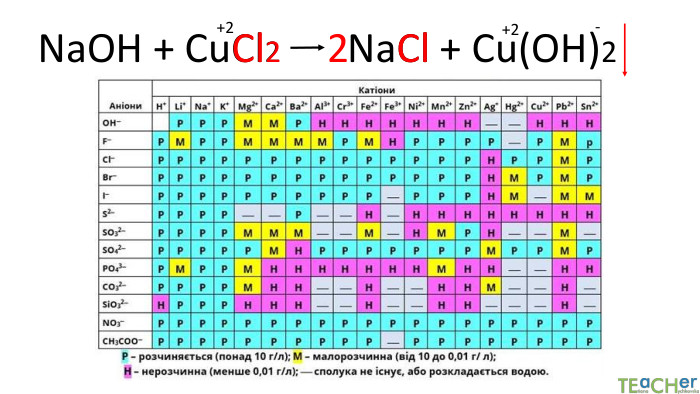
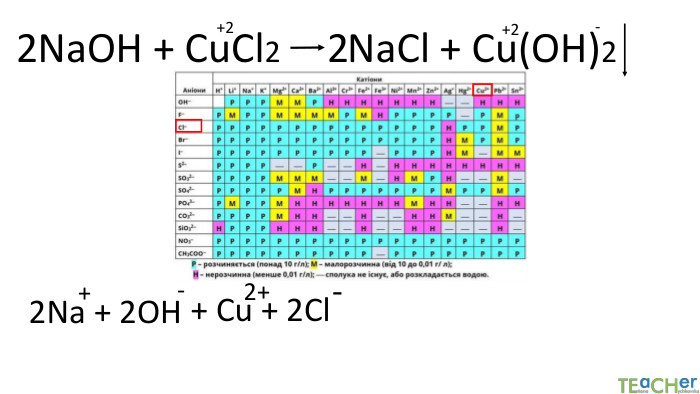
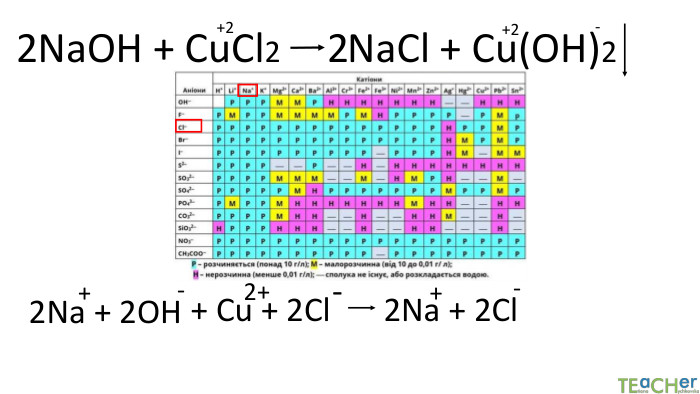
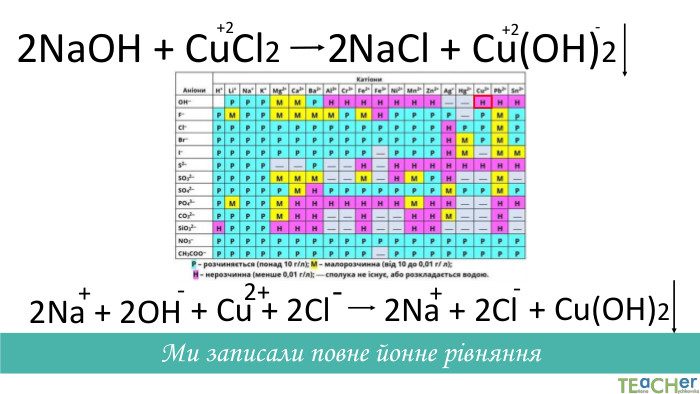
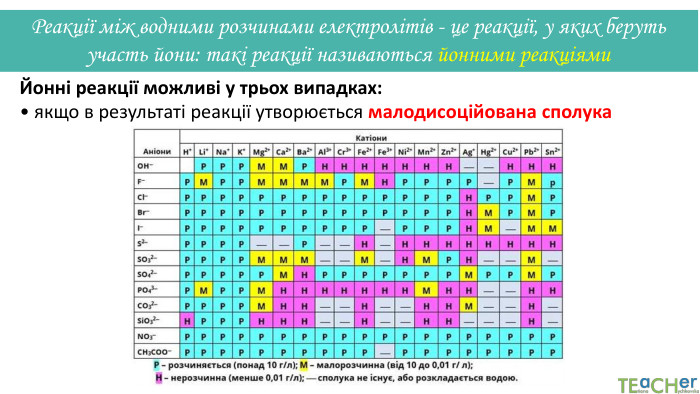
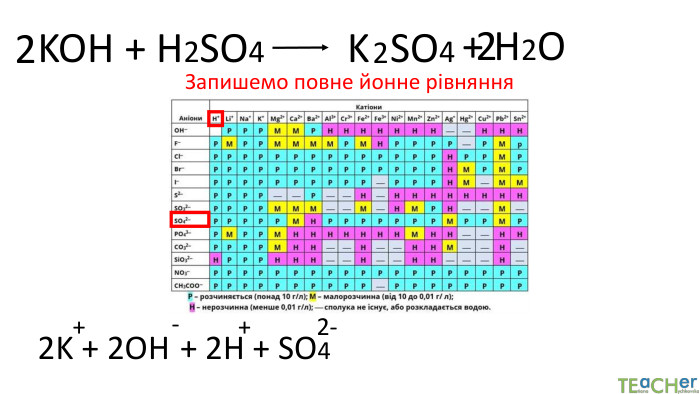
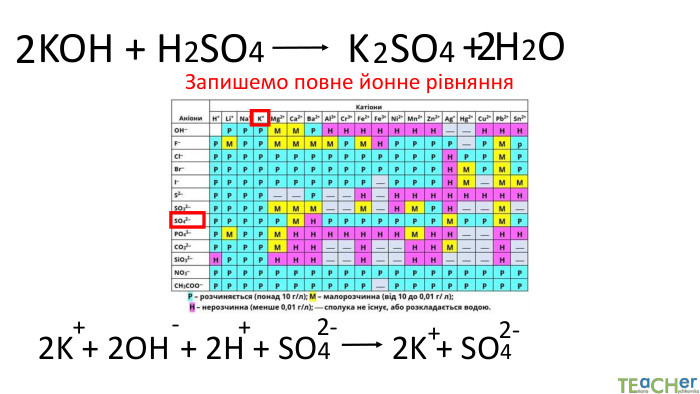
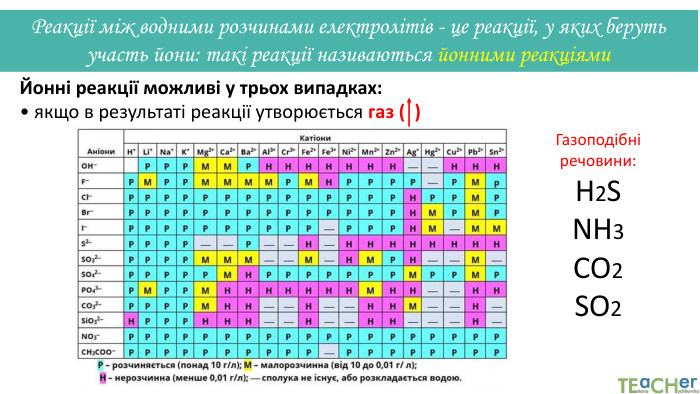
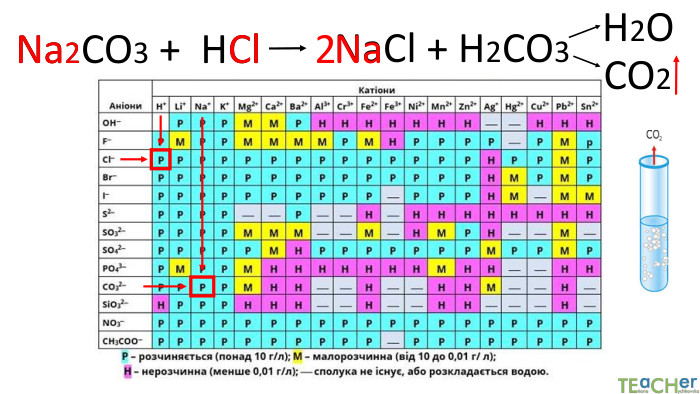
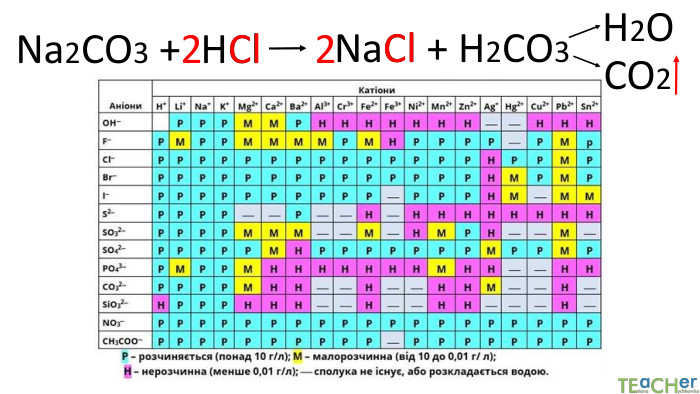
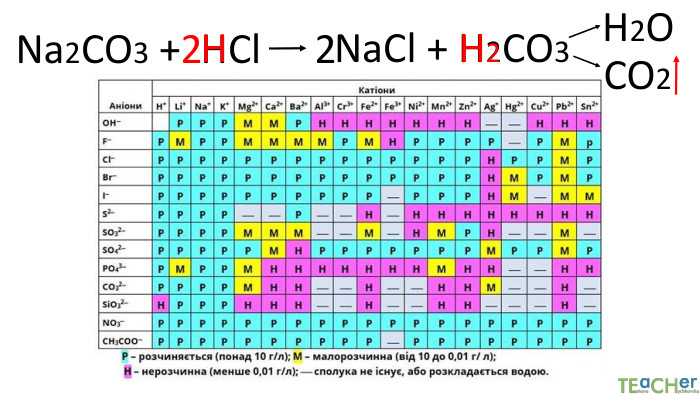
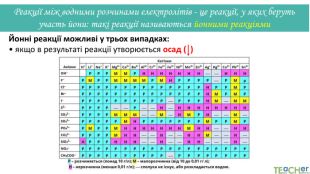
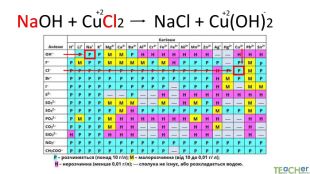
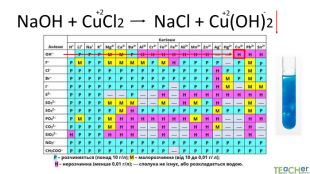
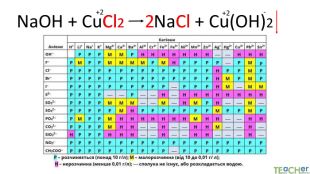
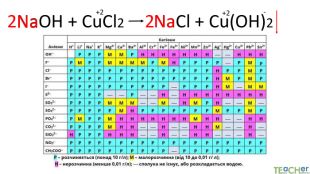
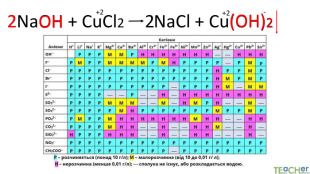
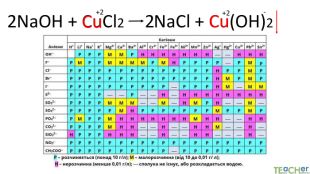
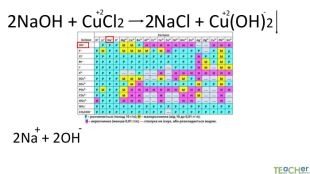
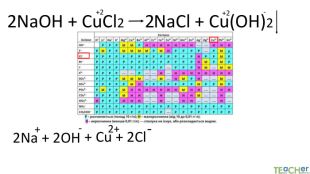
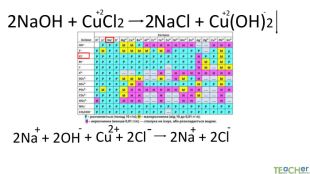
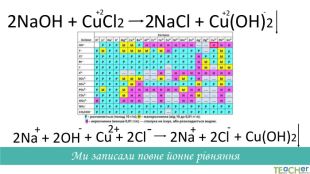
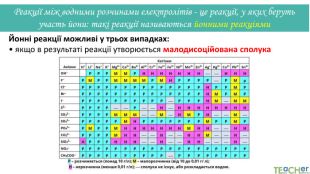
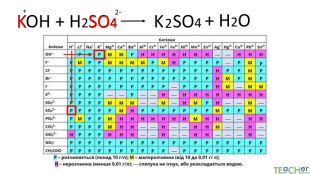
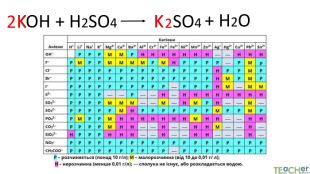
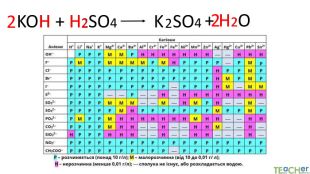
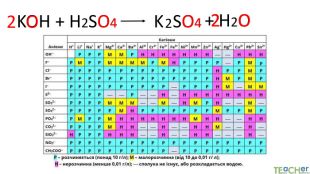
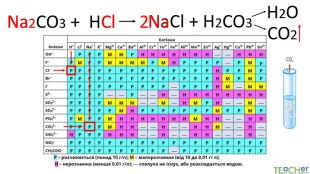
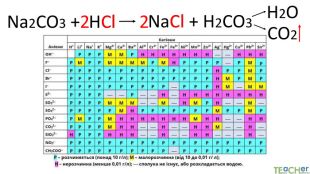
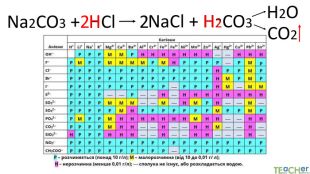
Коротко про головне. Хімічні реакції між йонами називають йонними реакціями. Йонні реакції можливі лише у тому випадку, якщо між йонами відбувається хімічна взаємодія і утворюються одна зі сполук:• нерозчинна речовина, що випадає у вигляді осаду;• газоподібна речовина;• молекули малодисоційованної речовини (слабкого електроліту).


про публікацію авторської розробки
Додати розробку




















-

Фертак Наталя Володимирівна
29.10.2025 в 17:24
дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бицина Оксана Валеріївна
20.10.2025 в 09:17
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Оноприенко Ирина Петрівна
17.10.2024 в 06:48
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Потапова Галина Іванівна
12.10.2024 в 10:33
дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пашаєва Тетяна Миколаївна
22.09.2024 в 21:06
Дуже вдячна!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 2 відгука