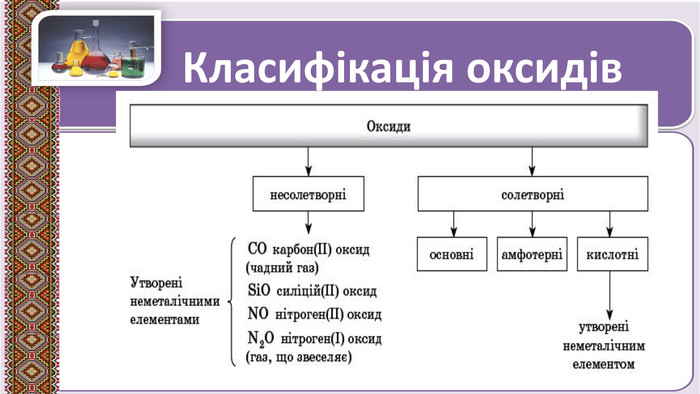
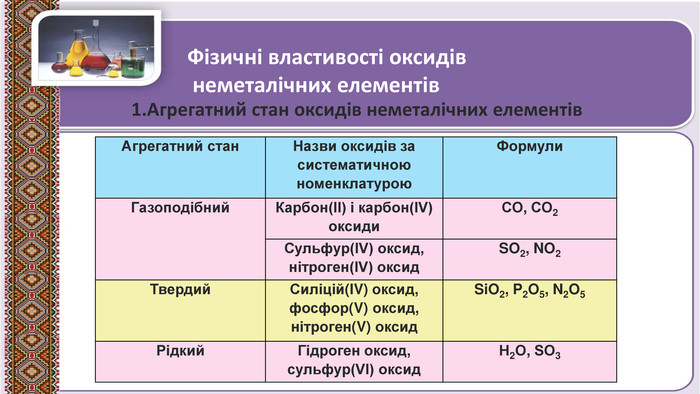
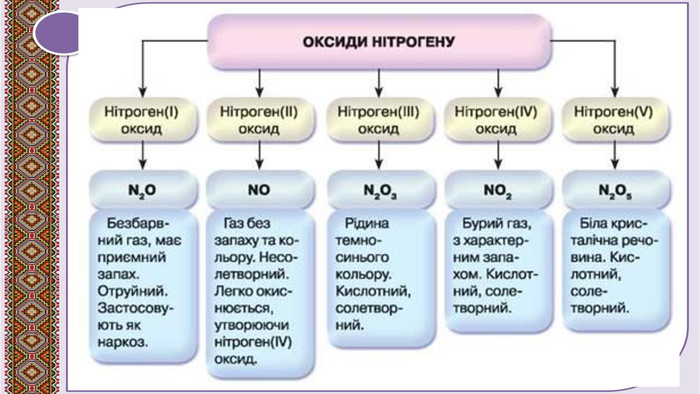
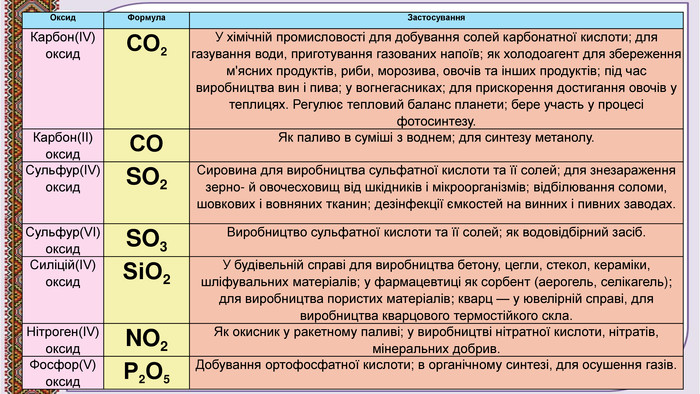
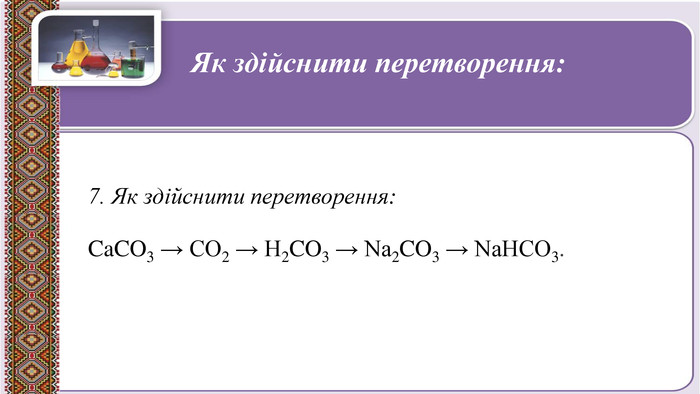
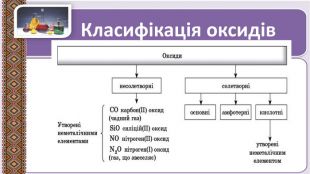
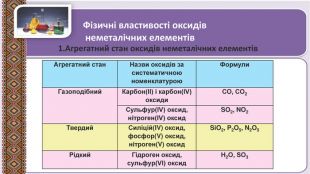
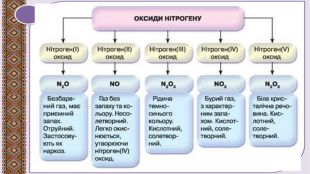
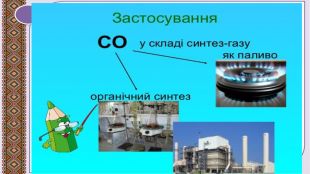
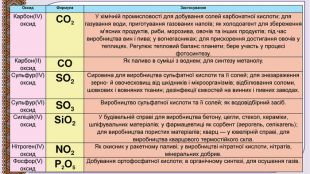
Презентація до уроку в 11 класі "Оксиди неметалічних елементів"
Про матеріал
Презентація до уроку в 11 класі "Оксиди неметалічних елементів" .Пропонується для вивчення теми як онлайн, так і офлайн. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку


![6. Розчин амоніаку не взаємодіє з кислотами.7. Водний розчин амоніаку виявляє основні властивості.8. Хлоридна кислота входить до складу шлункового соку. 9. Йон амонію позначається [NH4 ].¯ 10. Фенолфталеїн у водному розчині амоніаку набуває малинового забарвлення. 11. Якісним реактивом на солі амонію є розчин лугу. 12. Амоніак застосовують як холодоагент. 6. Розчин амоніаку не взаємодіє з кислотами.7. Водний розчин амоніаку виявляє основні властивості.8. Хлоридна кислота входить до складу шлункового соку. 9. Йон амонію позначається [NH4 ].¯ 10. Фенолфталеїн у водному розчині амоніаку набуває малинового забарвлення. 11. Якісним реактивом на солі амонію є розчин лугу. 12. Амоніак застосовують як холодоагент.](/uploads/files/96066/210531/226588_images/3.jpg)