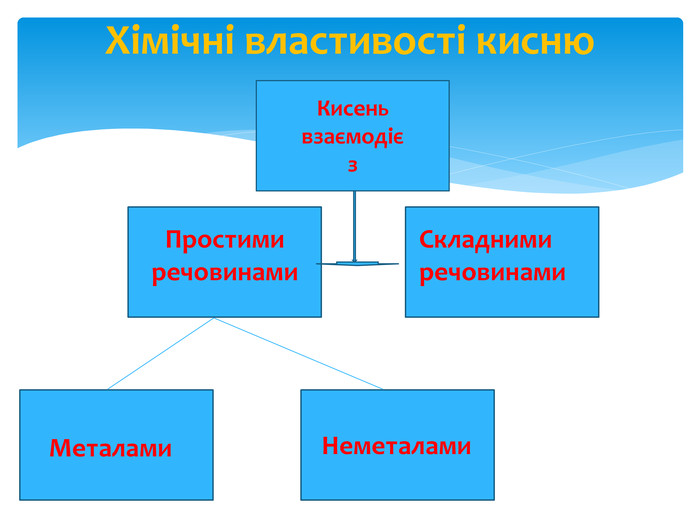
Презентація "Хімічні властивості кисню"
Про матеріал
Презентація допоможе повноцінно і цікаво (з відеоматеріалами) викласти матеріал уроку Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



































-

Салімон Галина Максимівна
23.02.2024 в 20:14
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Тихончук Олександр
22.02.2023 в 19:32
Прекрасна змістовна презентація, яка охоплює практично всі аспекти, передбачені навчальною програмою. Хотілося б лише, щоб вона була яскравішою і викликала в семикласників естетичне задоволення.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Гончарова Тетяна Олександрівна
21.04.2022 в 14:15
Дякую за розроблений матеріал!
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Ivanenko Olena
01.02.2022 в 08:00
Щиро дякую. Чудова презентація. Допомогла в підготовці до уроку.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-
Смолкіна Наталія Валеріївна
03.04.2020 в 15:16
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
Показати ще 2 відгука