Презентація "Історія вивчення атома. Ядерна модель атома.
Про матеріал
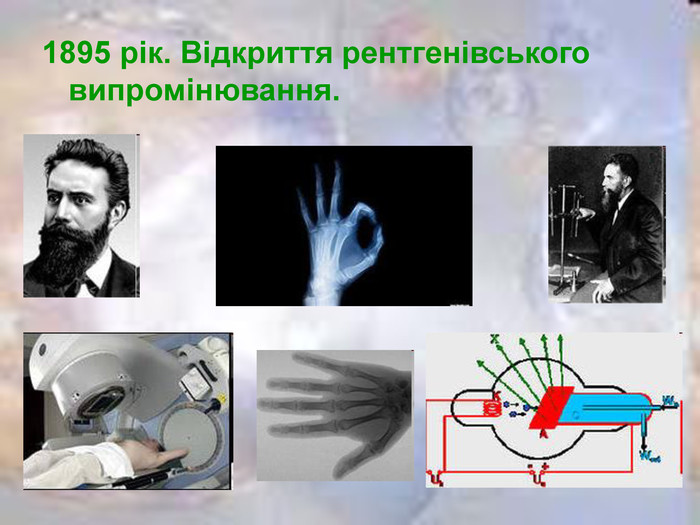
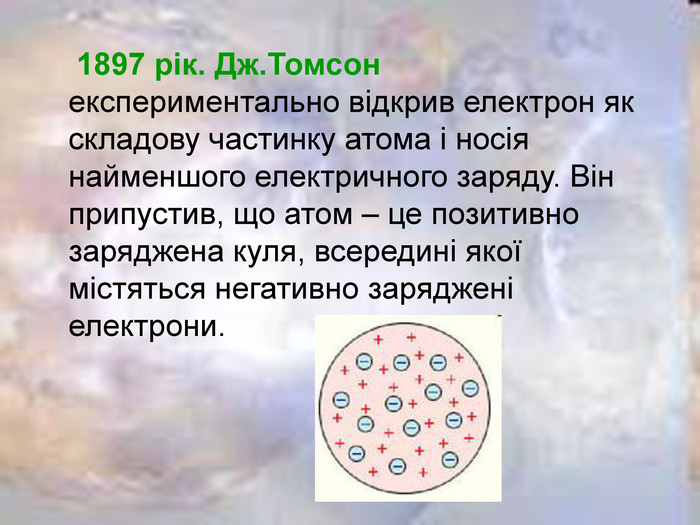
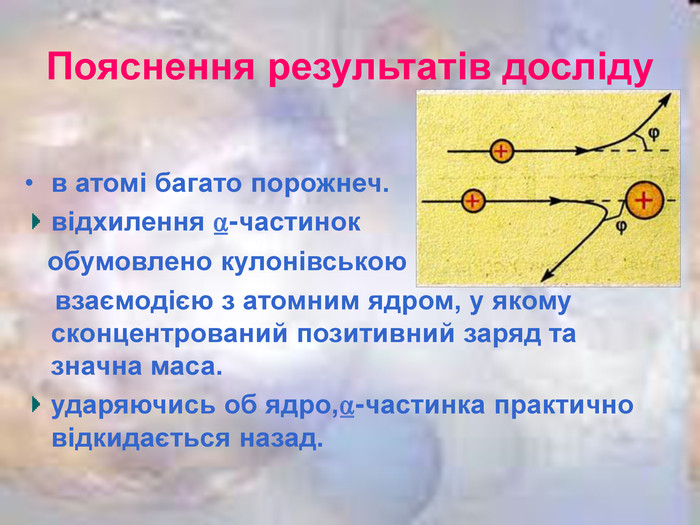
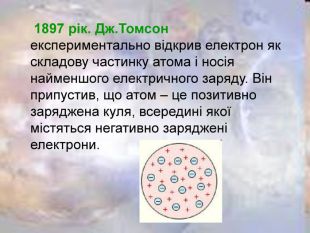
Презентацію "Історія вивчення атома. Ядерна модель атома" можна використати на першому уроці вивчення розділу "Атомна та ядерна фізика". В презентації міститься інформація про історію розвитку вчення про атом, схема та результати дослідів Резерфорда.
Перегляд файлу
Зміст слайдів
ppt
До підручника
Фізика (рівень стандарту) 11 клас (Сиротюк В.Д., Баштовий В.І.)
До уроку
§ 43. Історія вивчення атома Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку