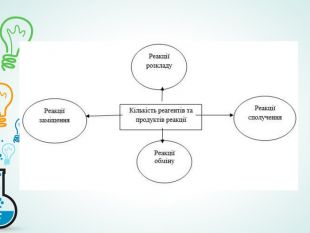
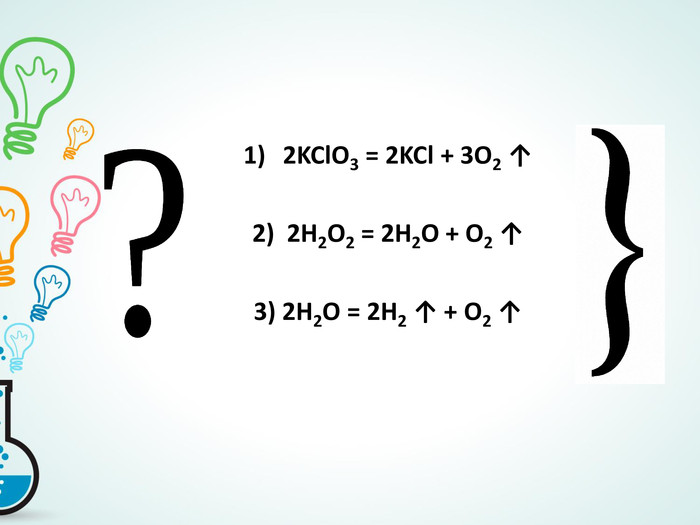Презентація "Класифікація хімічних реакцій за кількістю і складом реагентів та продуктів реакції"
Про матеріал
Презентація допоможе реалізувати наступні завдання:
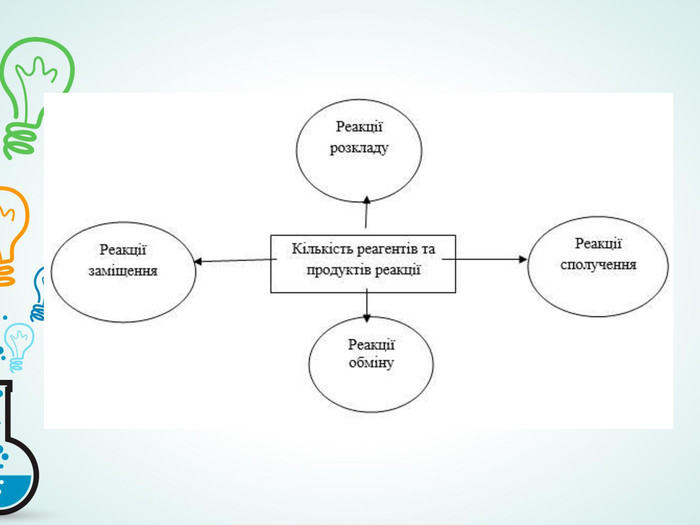
- узагальнити й систематизувати знання про хімічні реакції;
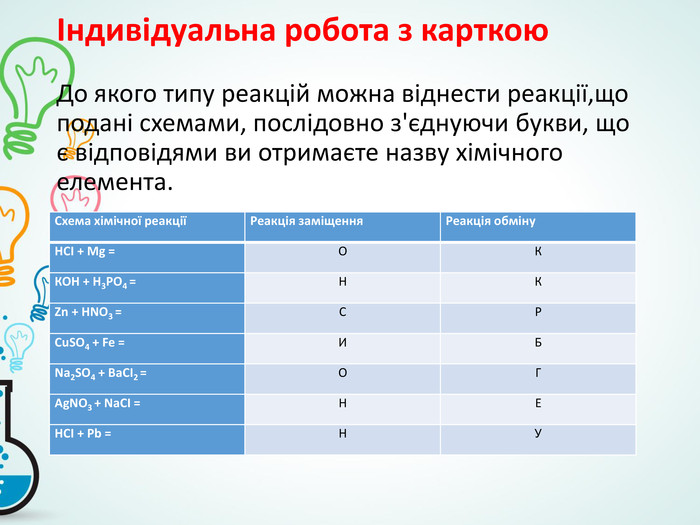
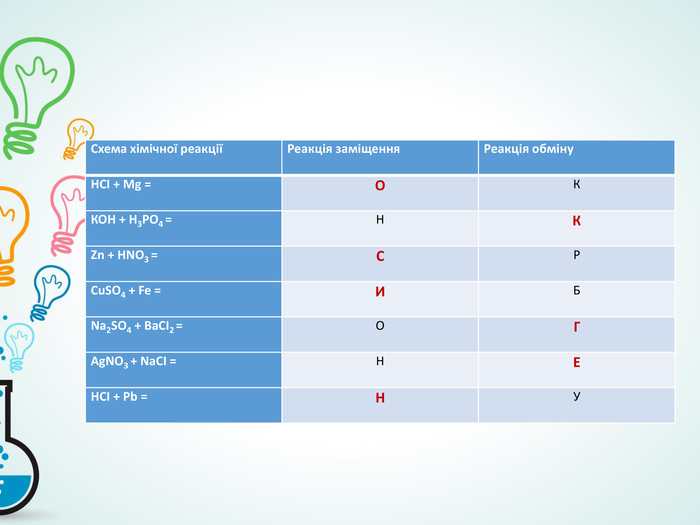
- розвивати вміння й навички визначення типів хімічних реакцій за рівняння-ми;
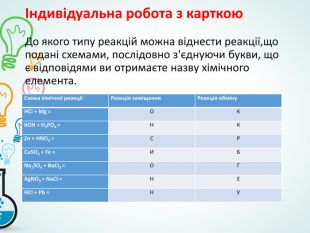
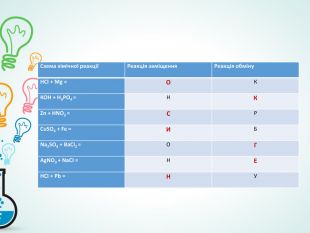
- продовжити формування вміння складати рівняння хімічних реакцій, розміщення коефіцієнтів на основі закону збереження мас.
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку