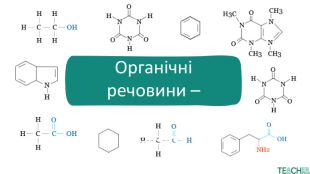
Презентація: "Ковалентні карбон-карбонові зв'язки у молекулах органічних сполук"


























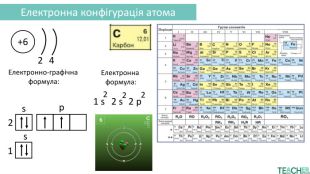
Гібридизація орбіталей атома карбону. S-орбіталі – це найпростіші орбіталі, що мають сферичну форму, центр яких знаходиться в ядріp-орбіталі – орієнтовані вздовж осей x, y та z, мають чітку гантелеподібну форму з двома частками, розділеними вузловою площиною, що проходить через ядро. Гібридизація орбіталей — це процес змішування атомних орбіталей одного атома, які мають різну форму та енергію, з утворенням такої ж самої кількості нових, але уже однакових за формою та енергією гібридних орбіталей
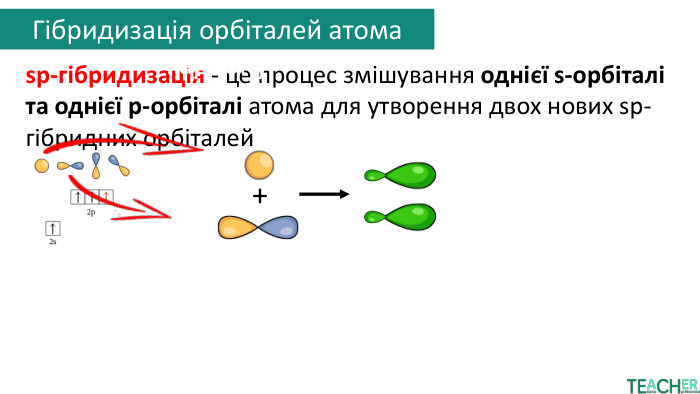
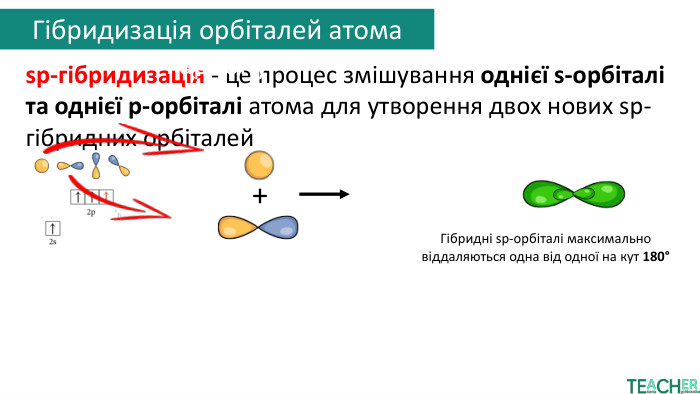
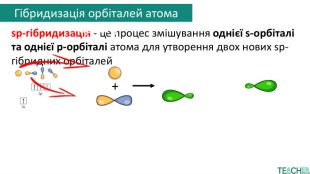
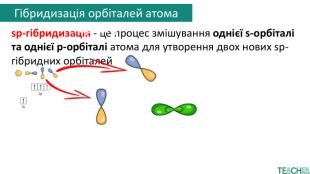
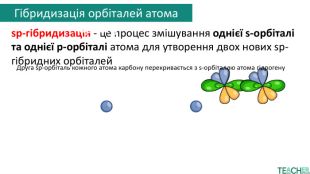
sp-гібридизація - це процес змішування однієї s-орбіталі та однієї p-орбіталі атома для утворення двох нових sp-гібридних орбіталей+атом карбонуутворення зв’язкуатом карбонуσ-зв'язок. Сигма-зв'язок (σ-зв'язок) — це тип ковалентного зв'язку, що утворюється шляхом осьового перекриття електронних орбіталей між двома атомами вздовж лінії, яка їх з'єднуєπ-зв'язок. Пі-зв'язок (π-зв'язок) — це хімічний зв'язок, що утворюється при бічному перекриванні атомних орбіталейπ-зв'язок. Гібридизація орбіталей атома карбону
Друга sp-орбіталь кожного атома карбону перекривається з s-орбіталлю атома гідрогену. Так утворюється молекула етину та решти алкінів. Гібридизація орбіталей атома карбонуsp-гібридизація - це процес змішування однієї s-орбіталі та однієї p-орбіталі атома для утворення двох нових sp-гібридних орбіталей
sp²-гібридизація - це процес змішування однієї s- та двох p-атомних орбіталей, що призводить до утворення трьох однакових sp²-гібридних орбіталей, які розташовуються в одній площині під кутом 120°Дві інші -орбіталі кожного атома карбону перекриваються з s-орбіталями атомів гідрогенуsp2 Гібридизація орбіталей атома карбону
sp²-гібридизація - це процес змішування однієї s- та двох p-атомних орбіталей, що призводить до утворення трьох однакових sp²-гібридних орбіталей, які розташовуються в одній площині під кутом 120°Так утворюється молекула етену та решти алкенів. Дві інші -орбіталі кожного атома карбону перекриваються з s-орбіталями атомів гідрогенуsp2 Гібридизація орбіталей атома карбону
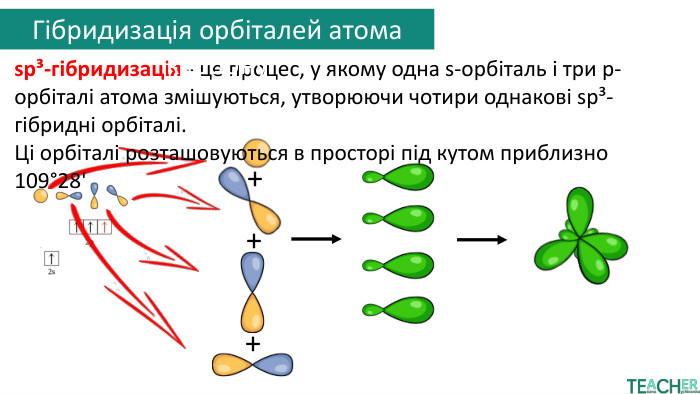
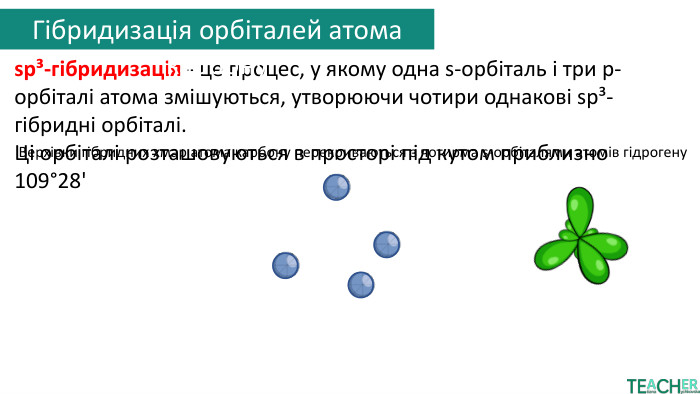
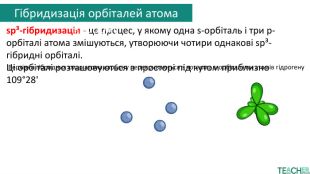
sp³-гібридизація - це процес, у якому одна s-орбіталь і три p-орбіталі атома змішуються, утворюючи чотири однакові sp³-гібридні орбіталі. Ці орбіталі розташовуються в просторі під кутом приблизно 109°28'Верхівки гібридних хмар атома карбону перекриваються з чотирма s-орбіталями атомів гідрогену. Гібридизація орбіталей атома карбону
Верхівки гібридних хмар атома карбону перекриваються з чотирма s-орбіталями атомів гідрогену. Так утворюється молекула етану та решти алканів. Гібридизація орбіталей атома карбонуsp³-гібридизація - це процес, у якому одна s-орбіталь і три p-орбіталі атома змішуються, утворюючи чотири однакові sp³-гібридні орбіталі. Ці орбіталі розташовуються в просторі під кутом приблизно 109°28'
Коротко про головне. У молекулах органічних сполук атоми Карбону здатні з’єднуватися між собою за допомогою ковалентних зв’язків трьох типів:одинарний (σ-зв’язок) – утворюється завдяки лінійному перекриванню орбіталей; такий зв’язок дозволяє атомам вільно обертатися і характерний для насичених сполук (алканів);подвійний (σ + π) – складається з одного σ- та одного π-зв’язку; він міцніший за одинарний, але обертання навколо нього неможливе. Подвійні зв’язки визначають властивості ненасичених сполук (алкенів);потрійний (σ + 2π) – найміцніший і найкоротший зв’язок; складається з одного σ- та двох π-зв’язків, зустрічається у алкінах


про публікацію авторської розробки
Додати розробку

























-

Шевченко Любов Олександрівна
30.09.2025 в 08:22
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шепета Людмила Юріівна
19.09.2025 в 10:01
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пашаєва Тетяна Миколаївна
10.09.2025 в 19:34
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Жорняк Антоніна
09.09.2025 в 08:45
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Переверзєва Інна
25.08.2025 в 22:38
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 2 відгука