Презентація «Маса атома елемента та молекулярна маса» 7 клас
Про матеріал
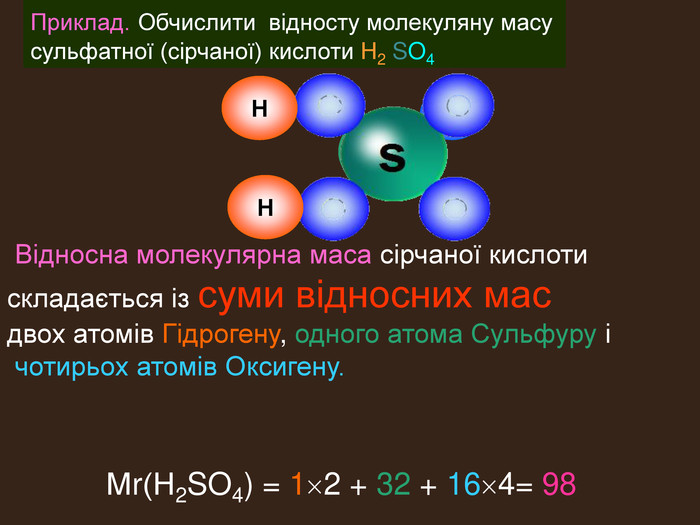
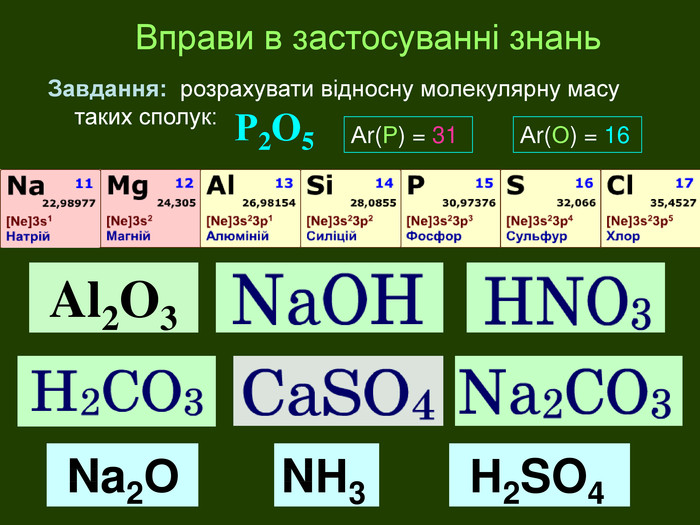
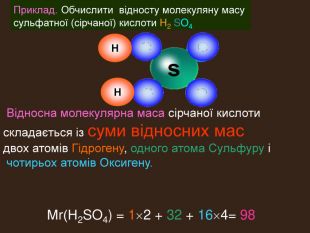
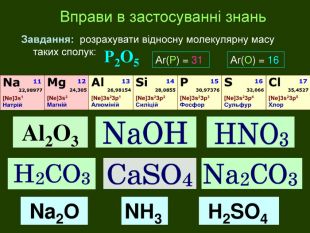
| Маса атома. Атомна одиниця маси. Відносні атомні маси хімічних елементів. Відносна молекулярна маса, її обчислення за хімічною формулою. Розв'язання розрахункових задач №1:«Обчислення відносної молекулярної маси речовини за її формулою.» |
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



































-

Шубіна Вікторія Вікторівна
01.04.2024 в 20:53
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Велика Наталія Миколаївна
08.11.2022 в 20:43
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Зачосенко Олена Іванівна
02.11.2021 в 17:42
Просто дякую.
Ви - молодець!!!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Palamarsctuk Olena
10.11.2020 в 10:47
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

12 ЕКО
19.10.2020 в 21:13
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Година Марина Леонiдiвна
07.10.2020 в 19:10
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Ковіна Ольга Юріївна
04.10.2020 в 20:07
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Кудлай Наталія Олександрівна
14.10.2019 в 20:23
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 5 відгуків