Презентація на тему "Основні положення МКТ"
















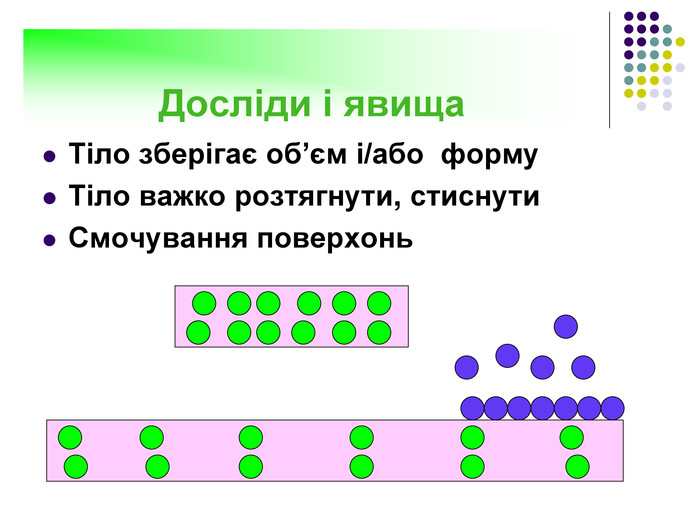









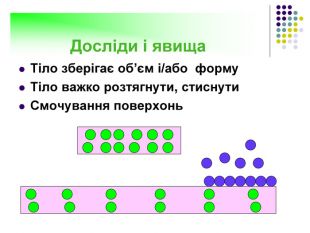
Встановити відповідність:1. Молекули рухаються з величезними швидкостями. 2. Тіла зберігають форму і об'єм.3. Атоми коливаються біля положення рівноваги.4. Відстань між молекулами перевищує розмір молекул.5. Молекули коливаються, періодично перескакуючи на нове місце. 6. Тіла зберігають форму, але не зберігають об'єм. А. Тверді тіла Б. Рідини. В. Гази. Відповіді:1-В2-А3-А4-В5-Б6-Б
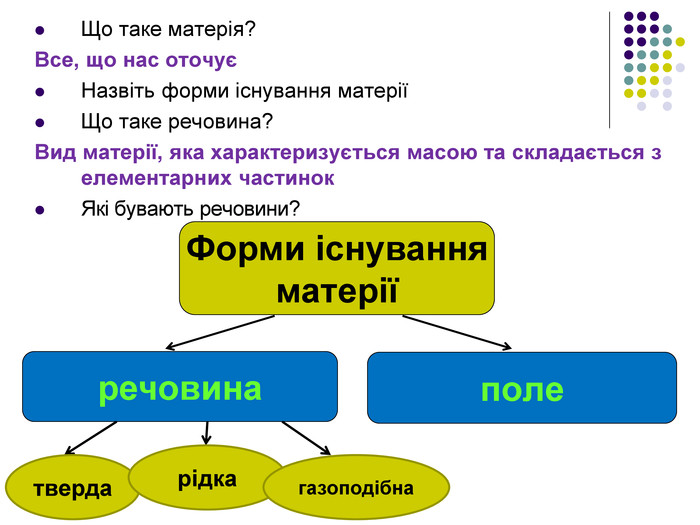
«Все складається з частинок ... речі відрізняються один від одного частинками, з яких складаються, їх порядком і розташуванням ...»Слово «атом» було внесено у фізику давньогрецьким ученим Демокритом дві з половиною тисячі років тому, який висунув гіпотезу про існування найдрібніших частинок ще в ІV столітті до н.е
Молекулярно-кінетична теоріясформувалася наприкінці дев'ятнадцятого століття. Джон Дальтон ввів поняття хімічного елемента (1804)Джозеф Лошмідт розрахував масу атомів (1865)Амедео Авогадро порахував кількість частинок. Отто Штерн виміряв швидкість молекул (1920)Д.І. Менделєєв об'єднав всі атоми в Періодичну систему. Ернест Резерфорд створив ядерну модель атома
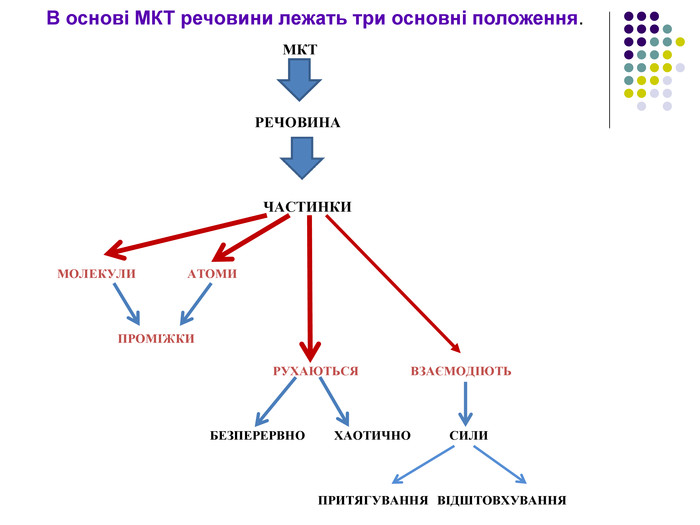
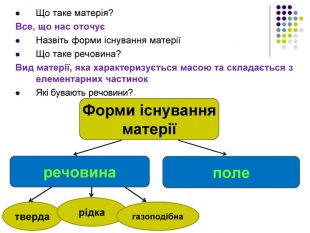
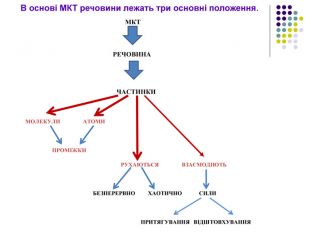
Молекулярна фізика — це розділ фізики, який розглядає властивості тіл як сумарний результат руху та взаємодії величезної кількості молекул, з яких складаються ці тіла. Основою молекулярної фізики є молекулярно-кінетична теорія будови речовини (МКТ). Мета молекулярно-кінетичної теорії — пояснення властивостей макроскопічних тіл і теплових процесів на основі уявлень про те, що всі тіла складаються з окремих частинок, які хаотично рухаються. Основна задача МКТ – встановити зв’язок між мікроскопічними і макроскопічними параметрами речовини.
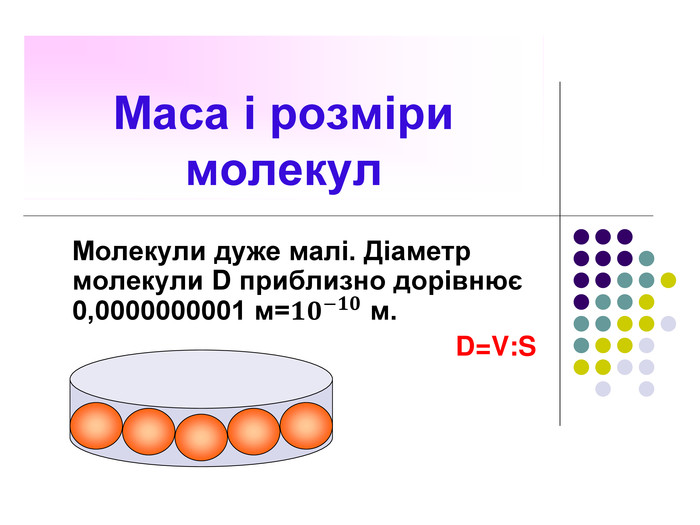
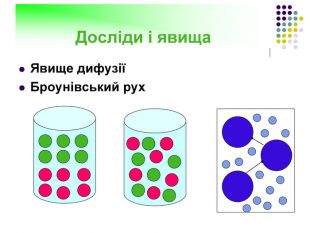
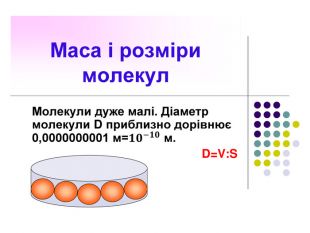
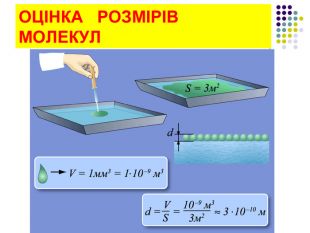
1. Будь-яка речовина складається з найдрібніших частинок — молекул чи атомів. Всі речовини складаються з молекул, розділених проміжками (дискретне будова речовини). У 1647 р. П'єр Гассенді (франц.) ввів слово «молекула» (molecula, зменшувальне від лат. Moles - маса)Молекула речовини - дрібна частка, зберігає його хімічні властивості. Атом в перекладі з грецького означає "неподільний".
Відносна молекулярна (або атомна) маса речовини Мr – це відношення маси молекули (або атома) даної речовини до 1/12 маси атома карбону. 𝑀𝑟=𝑚01/12𝑚𝑜𝑐 Молярна маса - маса 1 моля речовини. М = Мr ∙ 10-3 кг/моль. Наприклад, М(Н𝟐) = 2∙10-3 кг/моль, М(СО𝟐) = (12+2∙16)∙ 10-3 =44∙ 10-3 кг/моль.
Фізичні величин. Кількість речовини ν – число молекул речовини в будь-якому тілі Nа=6 ·10 ²³ моль−𝟏- число Авогадро. Один моль – це кількість речовини, в якій міститься стільки ж атомів або молекул, скільки атомів міститься у карбону масою 0,012 кг. Концентрація n – це кількість молекул (або атомів) в одиниці об’єму.n = 𝑵𝑽, 𝒏=1м−𝟑. ν=𝑚𝑀=𝑁𝑁𝑎
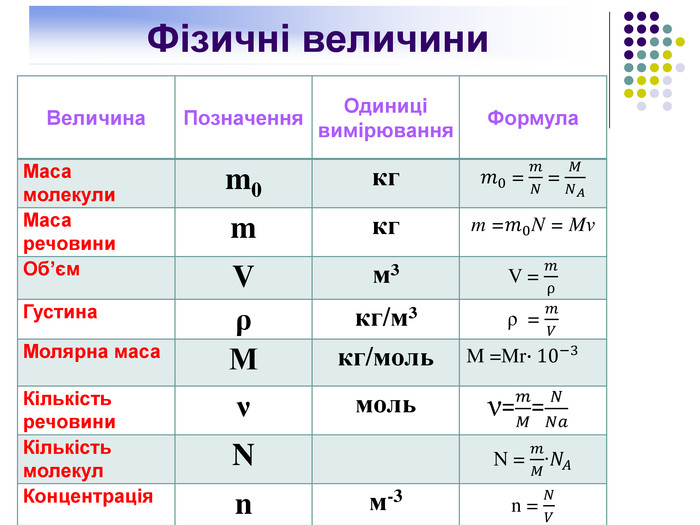
Фізичні величини{5 DA37 D80-6434-44 D0-A028-1 B22 A696006 F}Величина. Позначення. Одиниці вимірювання. Формула. Маса молекулиm0кг𝑚0 = 𝑚𝑁 = 𝑀𝑁𝐴Маса речовиниmкгm =𝑚0 N = MνОб’єм. Vм³V = 𝑚ρГустинаρкг/м³ρ = 𝑚𝑉Молярна маса. Мкг/моль. M =Mr∙10−3 Кількість речовиниνмоль. Кількість молекул. N N = 𝑚𝑀∙𝑁𝐴Концентраціяnм-3n = 𝑁𝑉{5 DA37 D80-6434-44 D0-A028-1 B22 A696006 F}Величина. Позначення. Одиниці вимірювання. Формула. Маса молекулиm0кг. Маса речовиниmкг. Об’єм. Vм³Густинаρкг/м³Молярна маса. Мкг/моль. Кількість речовиниνмоль. Кількість молекул. N Концентраціяnм-3
Ідеальний газ - теоретична модель газу, в якій нехтують розмірами і взаємодією часток газу, а враховують лише їх пружні зіткнення. Відстань між молекулами значно більша за їхні розміри. Сила взаємодії між молекулами газів практично відсутня. Взаємодія між молекулами відбувається лише під час короткочасних зіткнень.Ідеальний газ – набір не взаємодіючих матеріальних точок. Реальні розрідженні гази поводяться подібно до ідеального газу.
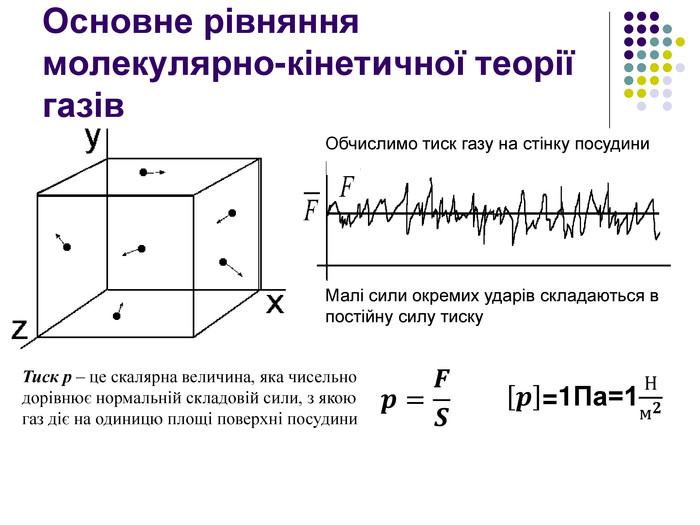
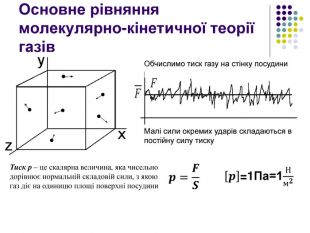
Основне рівняння молекулярно-кінетичної теорії газів. Обчислимо тиск газу на стінку посудини. Малі сили окремих ударів складаються в постійну силу тиску𝒑=𝑭𝑺 Тиск p – це скалярна величина, яка чисельно дорівнює нормальній складовій сили, з якою газ діє на одиницю площі поверхні посудини 𝒑=1 Па=1 Нм𝟐
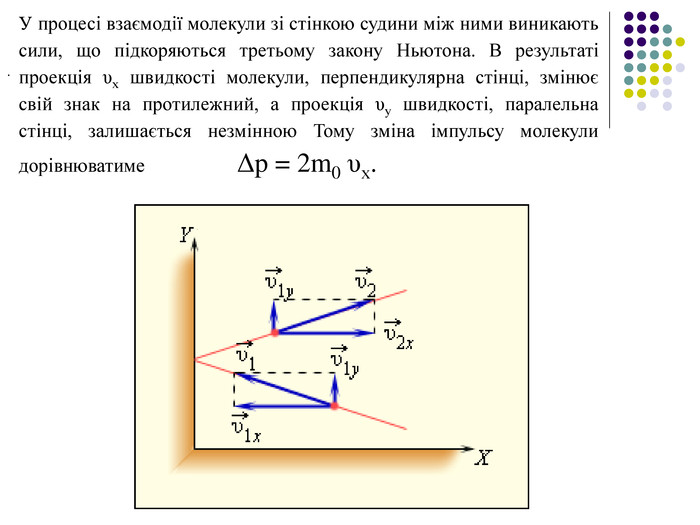
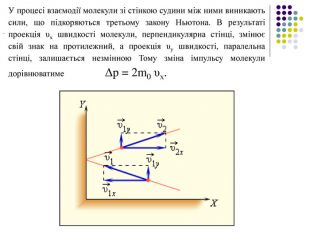
У процесі взаємодії молекули зі стінкою судини між ними виникають сили, що підкоряються третьому закону Ньютона. В результаті проекція υх швидкості молекули, перпендикулярна стінці, змінює свій знак на протилежний, а проекція υу швидкості, паралельна стінці, залишається незмінною Тому зміна імпульсу молекули дорівнюватиме Δp = 2m0 υх. .
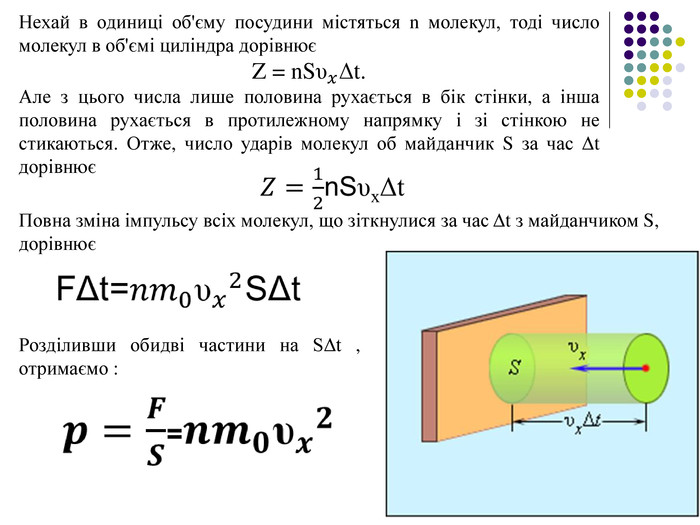
Нехай в одиниці об'єму посудини містяться n молекул, тоді число молекул в об'ємі циліндра дорівнює Z = n. Sυ𝑥Δt. Але з цього числа лише половина рухається в бік стінки, а інша половина рухається в протилежному напрямку і зі стінкою не стикаються. Отже, число ударів молекул об майданчик S за час Δt дорівнює Повна зміна імпульсу всіх молекул, що зіткнулися за час Δt з майданчиком S, дорівнює Розділивши обидві частини на SΔt , отримаємо :
Так як всі напрямки для векторів швидкостей молекул рівноймовірні, середнє значення квадратів їх проекцій на координатні осі рівні між собою: Остання рівність випливає з теореми Піфагора, квадрат швидкості молекули дорівнює сумі квадратів проекцій швидкості на координатні вісі: Формула для тиску газу на стінку посудини запишеться у вигляді𝒑=𝟏𝟑𝒏𝒎𝟎υ𝒙𝟐 Це рівняння встановлює зв'язок між тиском p ідеального газу, масою молекули m0, концентрацією молекул n і середнім значенням квадрата швидкості. Його називають основним рівнянням молекулярно - кінетичної теорії газів.
Гра «Доміно»… сили притягання і відштовхування. Газ, взаємодія між молекулами якого дуже мала, називають ...… кількість речовини«Молекула» в перекладі з латинської означає ...…броунівським. Дифузія доводить, що ...… електронів і ядра. У твердих тілах притягання між молекулами дуже велике, ....… ідеальним. У молях вимірюють ...… маса. Атом складається з …… тому що дуже малі проміжки між молекулами. Рух зважених в газі або рідини частинок називають ...… атоми і молекули перебувають у безперервному хаотичному (тепловому) русі. Між молекулами діють …
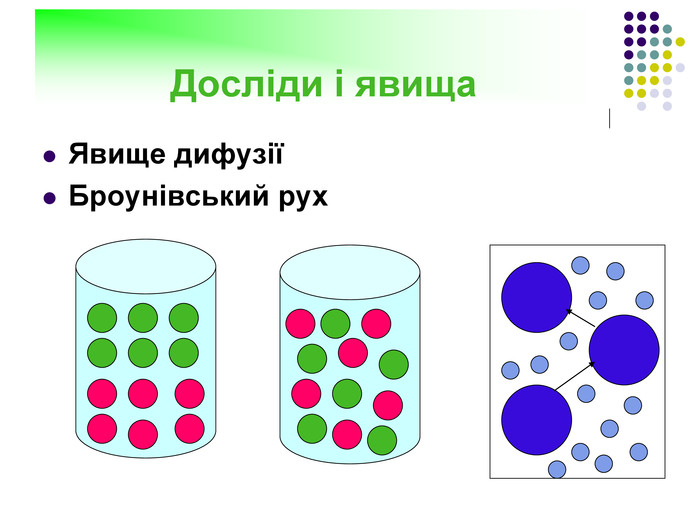
ПРАВИЛЬНІ ВІДПОВІДІГаз, взаємодія між молекулами якого дуже мала, називають ... … ідеальним«Молекула» в перекладі з латинської означає ... … маса. Дифузія доводить, що ... … атоми і молекули перебувають у безперервному хаотичному (тепловому) русі. У твердих тілах притягання між молекулами дуже велике, .... … тому що дуже малі проміжки між молекулами. У молях вимірюють ... … кількість речовини. Атом складається з …… електронів і ядра. Рух зважених в газі або рідини частинок називають ...…броунівським. Між молекулами діють …… сили притягання і відштовхування
Дякуюза роботу і увагу!1. Вивчити теоретичний матеріал за підручником. Гончаренко С. У. Фізика: Пробний навчальний посібник для шкіл ІІІ ступеня, гімназії і класів гуманітарного профілю. 10 кл.- К.: Освіта, 1995, с. 5-42.2. Виконати експериментальне завдання. Провести один із дослідів.2.1 На дно двох склянок із водою (в одній склянці — холодна вода, в другій – гаряча) покласти по однаковому шматочку сухої фарби. Через кожні півгодини вимірювати рівень забарвленої води. Пояснити результати досліду.2.2 Взяти два шматочки скла (можна два однакові дзеркальця), вимити, висушити й притиснути одне до одного. Легко чи важко їх роз’єднати? Те саме виконати з мокрим склом. Пояснити результати досліду.3. Прочитати поему Лукреція Кара «О природе вещей» і відповісти на запитання:1. Якими рядками підтверджуються положення МКТ? Підкреслити2. Перерахувати фізичні явища, про які йде мова в поемі?

про публікацію авторської розробки
Додати розробку




























-

Рокоча Юлія Миколаївна
29.01.2023 в 23:29
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бондар Галина
16.01.2023 в 20:12
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пугач Ксенія
25.01.2022 в 06:50
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Рибенцева Альона Геннадіївна
12.04.2021 в 19:36
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бондар Галина Василівна
07.02.2021 в 19:35
Дякую
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
4.0
-

Фелько Олег
20.01.2021 в 19:53
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Svirepova Viktoria
20.01.2021 в 10:24
Загальна:
4.3
Структурованість
4.0
Оригінальність викладу
5.0
Відповідність темі
4.0
Показати ще 4 відгука