Презентація на тему "Спирти"
Презентація розроблена з метою візуалізації навчального матеріалу за темою "Спирти".Вона містить як цікаві факти,так і завдання різного рівня,попередження з техніки безпеки.Яскраво і гармонійно проходить крізь лінію уроку.
Формує цифрової компетентність.












































Відгадай речовину.. - Ця речовина безбарвна.- Ця речовина не має запаху (якщо її не одорують етил- чи метилмеркаптаном).- Без цієї речовини не може обійтись промисловість нашої країни.- Ця речовина є причиною вибухів у шахтах.- Цю речовину називають ще «болотний газ».- Ця речовина є основним компонентом природного газу (98%), що дає нам змогу мати тепло в домівках зимою та допомагає в приготуванні їжі.
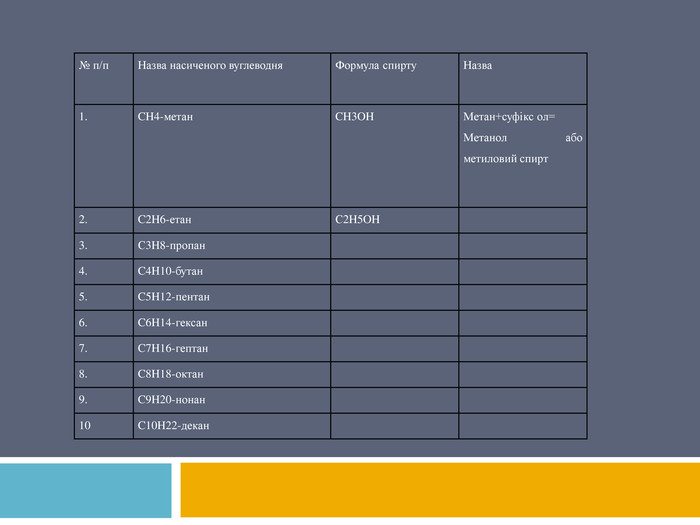
Назва спирту. Назву спирту утворюють від назви відповідного насиченого вуглеводню, додаючи до неї суфікс -ол. Якщо є потреба, указують номер атома Карбону , з яким зв’язана група -ОН. Крім того, часто використовують назви, в яких до слова спирт додають прикметник, що характеризує цей вуглеводень. СН3 ОН – метанол (метиловий спирт),С2 Н5 ОН – етанол (етиловий спирт).
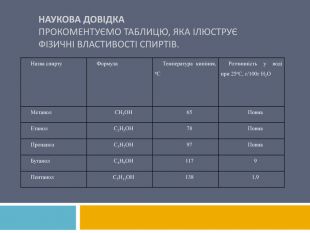
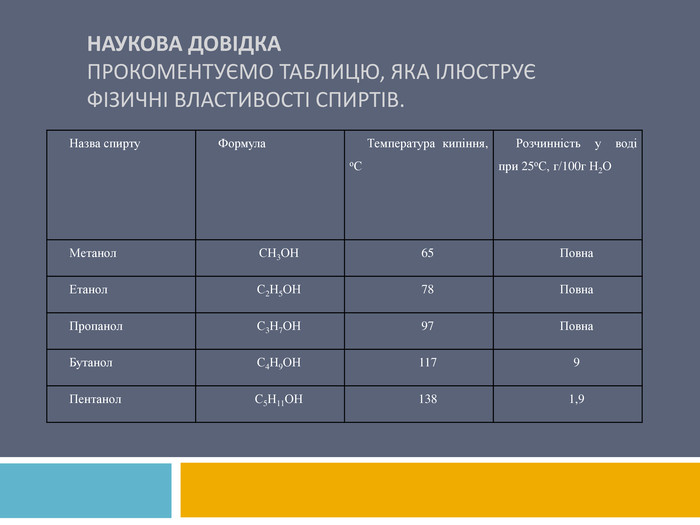
Наукова довідкапрокоментуємо таблицю, яка ілюструє фізичні властивості спиртів. Назва спирту. Формула. Температура кипіння, о. СРозчинність у воді при 25о. С, г/100г Н2 ОМетанол. СН3 ОН65 Повна. Етанол. С2 Н5 ОН78 Повна. Пропанол. С3 Н7 ОН97 Повна. Бутанол. С4 Н9 ОН1179 Пентанол. С5 Н11 ОН1381,9
Дослідна довідка. Хімічні властивості спиртів. Спирти, як і всі органічні сполуки, горять. Метанол і етанол миттєво спалахують при підпалюванні й горять синюватим, майже непомітним полум’ям із виділенням великої кількості теплоти. Відбувається реакція повного окиснення, продуктами якої є CO2 і H2 O: 2 CH3 OH + 3 O2 → 2 CO2 + 4 H2 O.
Під дією активних металів, таких як натрій, калій, магній, алюміній, відбувається заміщення атома Гідрогену на атом металу. Наприклад, у пробірку з етанолом покладемо шматочки натрію. Одразу відбувається реакція з виділенням газу. Це водень. Другим продуктом реакції є натрій етилат C2 H5 ONa: 2 C2 H5 OH + 2 Na → 2 C2 H5 ONa + H2.
Хід роботи. Дослід. У пробірку наливаю 2мл етанолу і поміщаю невеликий шматочок (розміром з горошину) металічного натрію. Учні спостерігають за проходженням реакції. Після закінчення реакції краплю добутого розчину переношу з пробірки на скло і випаровую. На склі виділяються білі кристали Натрій етилату.2 С2 Н5 ОН + 2 Na = 2 С2 Н5 ОNa + Н2
Спирти вступають в реакції дегідратації (відщеплення води). Так, якщо етанол нагріти вище 170 °С у присутності концентрованої сульфатної кислоти, відбувається реакція внутрішньомолекулярної дегідратації. Спирт перетворюється на ненасичений вуглеводень етилен: C2 H5 OH → CH2=CH2 + H2 O. Якщо етанол нагріти лише до температури 140 °С у присутності концентрованої сульфатної кислоти, відбувається реакція міжмолекулярної дегідратації. У результаті її утворюються діетиловий етер і вода: C2 H5 OH + HOC2 H5 → C2 H5 – O – C2 H5 + H2 O.
Увага! Іде демонстрація!Якісна реакція на гліцерин. У пробірку наллємо купрум (II) сульфат об’ємом 0,5 мл та натрій гідроксид об’ємом 1-2 мл. Випадає блакитний осад купрум (II) гідроксиду. До осаду добавимо гліцерин об’ємом 1-2 мл. Суміш енергійно змішаємо. Осад розчиняється. Розчин набуває яскраво-синього забарвлення.
Хімічна промисловість. Служить сировиною для одержання багатьох хімічних речовин, таких, як ацетальдегід, діетиловий ефір, тетраетилсвинець, оцтова кислота, хлороформ, етилацетат, етилен та ін. Широко застосовується як розчинник.Є компонентом антифризу і склоомивачів. У побутовій хімії етанол застосовується в чистячих і миючих засобах.Є розчинником для репелентів.
Медицинаяк антисептик як знезаражувачобробка операційного поля або в деяких методиках обробки рук хірурга; розчинник для лікарських засобів, для приготування настоянок, екстрактів з рослинної сировини та інконсервант настоянок і екстрактів піногасник при подачі кисню, штучної вентиляції легеньв зігріваючому компресі для фізичної охолодження при лихоманці (для розтирання) антидот при отруєнні етиленгліколем і метиловим спиртом; можливе застосування як компонента парентерального харчування (у вигляді 5% розчину) в ослаблених хворих з урахуванням високої енергетичної цінності речовини компонент загальної анестезії в ситуації дефіциту медикаментозних засобів
Підсумок-анкетування (на листочку)Прізвище та ім’я ________________1. Я дізнався (дізналася) про багато нового. (Так) (Ні)2. Мені це стане в пригоді в житті. (Так) (Ні)3. На уроці було про що подумати. (Так) (Ні)4. На всі запитання, що виникли на уроці, я одержав (-ла) відповіді. (Так) (Ні)5. На уроці я попрацював (-ла) сумлінно і мети уроку досяг (-ла). (Так) (Ні)
-
 Іщенко Ольга Василівна 09.01.2021 в 20:37Дякую! Презентація класна, структурована. Плюс в тому, що є слайди із завданнями для перевірки домашнього завдання та актуалізації опорних знань.Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Іщенко Ольга Василівна 09.01.2021 в 20:37Дякую! Презентація класна, структурована. Плюс в тому, що є слайди із завданнями для перевірки домашнього завдання та актуалізації опорних знань.Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0 -
 Фесенко Надежда 03.12.2020 в 20:15Презентація цікава, продумана ДякуюЗагальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Фесенко Надежда 03.12.2020 в 20:15Презентація цікава, продумана ДякуюЗагальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку