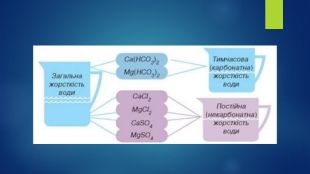
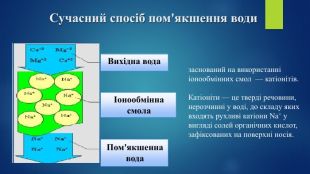
Презентація на тему: "Твердість води".
Про матеріал
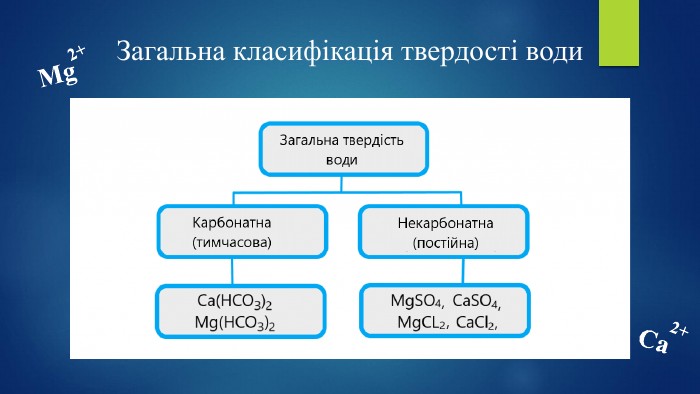
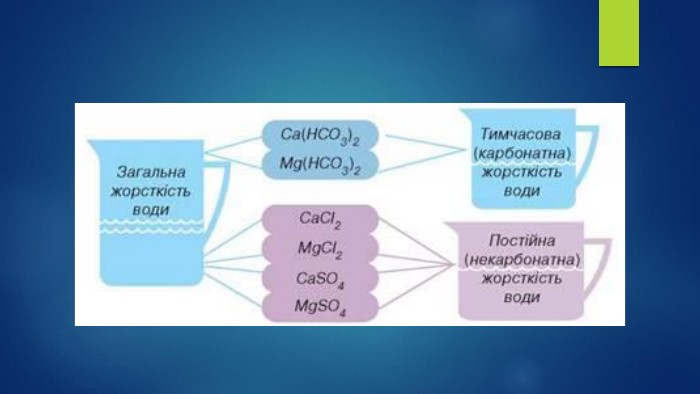
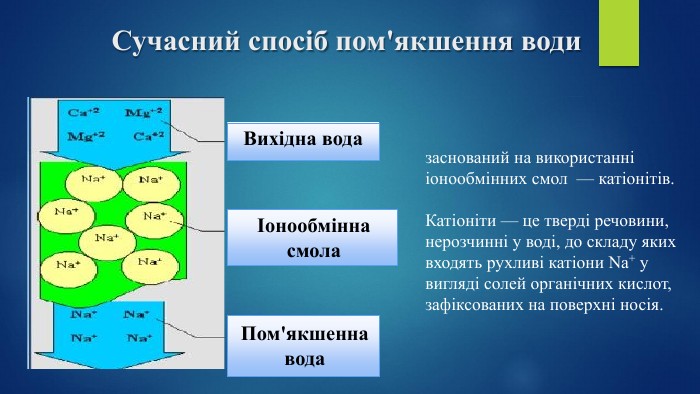
Дана презентація дозволить учням уявити чому саме цей стан відбувається в побуті і взагалі в природі. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку